名校
解题方法
1 . 下列说法中错误的是
| A.根据对角线规则,铍和铝的性质具有相似性 |
B.在H3O+、 和[Cu(NH3)4]2+中都存在配位键 和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.P4和CH4都是正四面体分子且都含有非极性键 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
| A.HClO的结构式:H—Cl—O |
| B.第二周期第一电离能介于B和N之间的元素有3种 |
C.根据元素在周期表的位置, 与 与 的性质更相似 的性质更相似 |
D.元素周期表每一周期元素原子的最外层电子排布均是从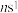 过渡到 过渡到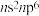 |
您最近一年使用:0次
名校
解题方法
3 . 下列理论解释不符合实验事实的是
| 选项 | 实验事实 | 理论解释 |
| A | Be和Al都能溶于NaOH溶液 | Be和Al在元素周期表中是对角线关系,性质相似 |
| B | 酸性:H2SO4>H2SO3 | H2SO4中非羟基氧原子个数更多,中心原子的正电性更高 |
| C | Fe2+比Fe3+的稳定性小 | Fe2+和Fe3+的价电子排布式分别为3d6、3d5,Fe3+的3d能级为半充满的稳定结构 |
| D | SiO2的熔点高于CO2 | SiO2的相对分子质量更大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂离子电池正极材料。回答下列问题:
(1)在周期表中,与Li化学性质最相似的邻族元素是_____ ,基态O原子的价电子轨道表示式为_____ 。
(2)原子核外电子有两种相反的自旋状态,分别用+ 和-
和- 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为_____ 。基态Fe元素的价电子排布式为_____ 。
(3)PO 的空间结构为
的空间结构为_____ 形,其中心原子的杂化轨道类型为_____ 。
(4)PH3和NH3相比,_____ 更易液化;C、N、O元素的第一电离能由大到小的顺序为_____ 。
(5)NH4H2PO4中,电负性最高的元素是_____ ;P的_____ 杂化轨道与O的2p轨道形成_____ 键。(填σ或π)
(6)CO 的空间构型为
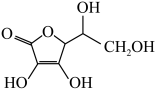
的空间构型为_____ (用文字描述);抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为_____ ;推测抗坏血酸在水中的溶解性:_____ (填“难溶于水”或“易溶于水”)。
(1)在周期表中,与Li化学性质最相似的邻族元素是
(2)原子核外电子有两种相反的自旋状态,分别用+
 和-
和- 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(3)PO
 的空间结构为
的空间结构为(4)PH3和NH3相比,
(5)NH4H2PO4中,电负性最高的元素是
(6)CO
 的空间构型为
的空间构型为
您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
5 . 元素的对角线规则
(1)在元素周期表中,某些_______ 族元素与其右下方的_______ 族元素(如图)的有些性质是相似的(如锂和镁在过量的氧气中燃烧均生成正常氧化物,而不是过氧化物),这种相似性被称为“_______ ”。

(2)处于“对角线”位置的元素,它们的_______ 具有相似性。
实例分析:
①锂和镁的相似性
A.锂与镁的沸点较为接近:
B.锂和镁在氧气中_______ 时只生成对应的氧化物,并且Li2O和MgO与水反应都十分缓慢。
4Li+O2 2Li2O、2Mg+O2
2Li2O、2Mg+O2 2MgO。
2MgO。
C.锂和镁与水的反应都十分缓慢,并且生成的氢氧化物_______ 溶于水,附着于金属表面阻碍反应的进行。
D.锂和镁都能直接与氮气反应生成相应的氮化物Li3N和Mg3N2。
E.锂和镁的氢氧化物在加热时,可分解为Li2O、H2O和MgO、H2O。
F.在碱金属的氟化物、碳酸盐和磷酸盐中,只有锂盐是_______ 溶于水的,相应的镁盐也_______ 溶于水。
②铍和铝的相似性
A.铍与铝都可与酸、碱反应放出_______ ,并且铍在浓硝酸中也发生_______ 化。
B.二者的氧化物和氢氧化物都既能溶于强酸又能溶于强碱溶液:
Al(OH)3+3HCl=_______ ,Al(OH)3+NaOH=_______ ;
Be(OH)2+2HCl=_______ ,Be(OH)2+2NaOH=_______ 。
C.二者的氧化物Al2O3和BeO的熔点和硬度都很高。
D.BeCl2和AlCl3都是共价化合物,易_______ 。
③硼和硅的相似性
A.自然界中B与Si均以化合物的形式存在。
B.B与Si的单质都易与强碱反应,且不与稀酸反应:
2B+2KOH+2H2O=_______ ,Si+2KOH+H2O=_______ 。
C.硼烷和硅烷的稳定性都比较差,且都易_______ 。
D.硼和硅的卤化物的熔、沸点比较低,易挥发,易水解。
(1)在元素周期表中,某些

(2)处于“对角线”位置的元素,它们的
实例分析:
①锂和镁的相似性
A.锂与镁的沸点较为接近:
| 元素 | Li | Na | Be | Mg |
| 沸点/℃ | 1 341 | 881.4 | 2 467 | 1 100 |
B.锂和镁在氧气中
4Li+O2
 2Li2O、2Mg+O2
2Li2O、2Mg+O2 2MgO。
2MgO。C.锂和镁与水的反应都十分缓慢,并且生成的氢氧化物
D.锂和镁都能直接与氮气反应生成相应的氮化物Li3N和Mg3N2。
E.锂和镁的氢氧化物在加热时,可分解为Li2O、H2O和MgO、H2O。
F.在碱金属的氟化物、碳酸盐和磷酸盐中,只有锂盐是
②铍和铝的相似性
A.铍与铝都可与酸、碱反应放出
B.二者的氧化物和氢氧化物都既能溶于强酸又能溶于强碱溶液:
Al(OH)3+3HCl=
Be(OH)2+2HCl=
C.二者的氧化物Al2O3和BeO的熔点和硬度都很高。
D.BeCl2和AlCl3都是共价化合物,易
③硼和硅的相似性
A.自然界中B与Si均以化合物的形式存在。
B.B与Si的单质都易与强碱反应,且不与稀酸反应:
2B+2KOH+2H2O=
C.硼烷和硅烷的稳定性都比较差,且都易
D.硼和硅的卤化物的熔、沸点比较低,易挥发,易水解。
您最近一年使用:0次
名校
解题方法
6 . “类推”是一种重要的学习方法,但有时会产生错误,下列类推得到的结论正确的是
A. 和 和 都只含极性键, 都只含极性键, 是极性分子,故 是极性分子,故 也是极性分子 也是极性分子 |
B. 和 和 都为正四面体形, 都为正四面体形, 中键角也为60°, 中键角也为60°, 中键角也为60° 中键角也为60° |
| C.根据对角线规则,元素Li和Mg的某些性质相似,则元素B和Si的某些性质也相似 |
D.氢化物沸点是: ;则ⅤA族元素氢化物沸点也是: ;则ⅤA族元素氢化物沸点也是: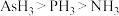 |
您最近一年使用:0次
名校
7 . 如表为长式周期表的一部分,其中的编号代表对应的元素。
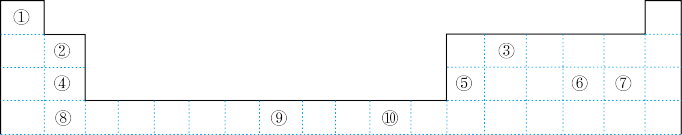
请回答下列问题:
(1)表中属于d区的元素是_______ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_______ 。
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为_______ ;该元素与元素①形成的分子X的立体构型为_______ ,与⑧在同一周期的元素中的未成对电子数目最多的元素的价电子排布式是_______ 。
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_______ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
8 . 下列各组离子中,可能能在所处环境中大量共存的是
A.在室温环境下c(OH-)=1×10-11的溶液中:Cr2+,SO ,NO ,NO ,Na+ ,Na+ |
B.在4℃的水溶液中:Be2+,K+,PO ,OH- ,OH- |
C.在漂白液中:OH-,Rb+,SO ,CO ,CO |
| D.在水玻璃中:H+,SCN-,Cl-,Cs+ |
您最近一年使用:0次
解题方法
9 . 下列关于原子结构和性质的叙述中,正确的为
①2p、3p、4p能级的轨道数依次增多
②ds区全部是金属元素
③在一个原子轨道中最多能容纳2个电子且自旋相反,称为洪特规则
④Be和Al在化学性质上具有一定的相似性
⑤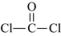 中的σ键与π键个数比为1:3
中的σ键与π键个数比为1:3
①2p、3p、4p能级的轨道数依次增多
②ds区全部是金属元素
③在一个原子轨道中最多能容纳2个电子且自旋相反,称为洪特规则
④Be和Al在化学性质上具有一定的相似性
⑤
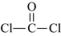 中的σ键与π键个数比为1:3
中的σ键与π键个数比为1:3| A.②④ | B.①②④ | C.②④⑤ | D.③④⑤ |
您最近一年使用:0次
22-23高二上·浙江·期末
解题方法
10 . 下列“类比”结果正确的是
| A.H2S晶体中一个H2S分子周围有12个H2S紧邻,则冰中一个水分子周围也有12个紧邻分子 |
| B.AlCl3中Al原子是sp2杂化,则Al2Cl6中Al原子也是sp2杂化 |
| C.Mg在过量氧气中燃烧生成MgO,则锂在过量氧气燃烧也生成Li2O |
| D.乙醇CH3CH2OH能与水互溶,则戊醇CH3CH2CH2CH2CH2OH也能与水互溶 |
您最近一年使用:0次



