名校
解题方法
1 . 短周期主族元素X、Y、Z、G、T的原子序数依次增大,Z、G是金属元素且G的氧化物属于两性氧化物,T的原子序数是Y的2倍且T、Y的最低化合价相同。这5种元素的价电子数之和等于20,含Z元素的物质的焰色呈黄色。回答下列问题:
(1)X的最高价氧化物对应水化物的化学式为___________ 。位于元素周期表中s区的元素为___________ (填元素符号)。
(2)Y、Z、G、T的电负性由小到大的顺序为___________ (填元素符号)。
(3) 分子是
分子是___________ (填“极性”或“非极性”)分子。 分子中T的价层电子对数为
分子中T的价层电子对数为___________ 。
(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为___________ 。
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型___________ 。
(6)T的一种单质的结构如图所示: ,T原子杂化类型是
,T原子杂化类型是________ 。32gT的这种单质含σ键的数目为________ 。这种单质易溶于 ,不溶于水,其原因是
,不溶于水,其原因是_________ 。
(1)X的最高价氧化物对应水化物的化学式为
(2)Y、Z、G、T的电负性由小到大的顺序为
(3)
 分子是
分子是 分子中T的价层电子对数为
分子中T的价层电子对数为(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型
(6)T的一种单质的结构如图所示:
 ,T原子杂化类型是
,T原子杂化类型是 ,不溶于水,其原因是
,不溶于水,其原因是
您最近一年使用:0次
2023-04-28更新
|
178次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高二下学期4月期中考试化学试题
名校
解题方法
2 . 2020年某科研团队经多次实验发现一种新型漂白剂(结构见图),可用于漂白蚕丝等织品,其组成元素均为短周期元素,W、X对应的简单离子核外电子排布相同,且W、Y、Z的最外层电子数之和等于X的最外层电子数,下列说法错误的是
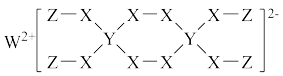

| A.四种元素中X的电负性最大 |
| B.该物质中各原子或离子均达到2或8电子稳定结构 |
| C.Y的最高价氧化物的水化物是一元弱酸 |
| D.离子半径:Z+ <X2- ˂W2+ |
您最近一年使用:0次
2021-11-06更新
|
430次组卷
|
3卷引用:广东省普宁市华侨中学2021-2022学年高二下学期期中考试化学试题
解题方法
3 . 几种短周期元素的原子半径及主要化合价如表。下列叙述正确的是
| 元素符号 | X | Y | Z | W | Q |
| 原子半径 | 160 | 143 | 70 | 66 | 102 |
| 主要化合物 | +2 | +3 | +5、—3 | —2 | +6、—2 |
| A.X、Y元素的金属性X<Y |
| B.一定条件下,W单质与Q的常见单质直接生成QW3 |
| C.Z的最高价氧化物对应的水化物是一种弱酸 |
| D.氢化物的沸点H2W>H2Q |
您最近一年使用:0次
名校
解题方法
4 . X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲俗称苛性钠,由X、Z、Q三种元素组成。Q是短周期中金属性最强的元素,W与Z同主族。请回答下列问题:
(1)W在周期表中的位置为_____ ,R的离子结构示意图为_____ ,Q2Z2的电子式为_____ ,化合物甲中含有的化学键为_____ 。
(2)Y元素是自然界各种生物体生命活动不可缺少的重要元素,其气态氢化物丙与最高价氧化物对应水化物丁能发生化合反应,则Y元素为_____ (填元素符号),过量铁粉与丁的稀溶液反应的离子方程式为____ ,丙与NO在一定条件下能反应生成无毒无污染的物质,该反应的化学方程式为_____ 。
(3)化合物W2R2(沸点:138℃)可与水反应生成一种能使品红溶液褪色的气体,0.1mol该物质参加反应时转移0.15mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为_____ 。
(1)W在周期表中的位置为
(2)Y元素是自然界各种生物体生命活动不可缺少的重要元素,其气态氢化物丙与最高价氧化物对应水化物丁能发生化合反应,则Y元素为
(3)化合物W2R2(沸点:138℃)可与水反应生成一种能使品红溶液褪色的气体,0.1mol该物质参加反应时转移0.15mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
5 . A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为_________________ 。写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式________________________________ 。
(2)由A、B两种元素组成的18电子微粒的分子式为____________________ 。
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_________________________________________ 。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是_________ L(标准状况下)。
(1)E元素在周期表中的位置为
(2)由A、B两种元素组成的18电子微粒的分子式为
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是
您最近一年使用:0次
名校
解题方法
6 . A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A_______ ,B________ ,C________ ,D________ ,E__________
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:____________ 。
(3)写出A、B两元素最高价氧化物的水化物相互反应的化学方程式:______________ 。
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示)_______________ 。
(1)写出下列元素符号:A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A、B两元素最高价氧化物的水化物相互反应的化学方程式:
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示)
您最近一年使用:0次
2019-06-23更新
|
106次组卷
|
2卷引用:黑龙江省牡丹江市第三高级中学2018-2019学年高一下学期期中考试化学试题
解题方法
7 . 在下述转化关系中,已知B、D都是淡黄色固体,且A与D为单质,并可反应生成离子化合物。试回答:
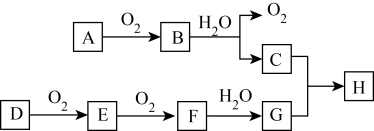
(1) G的化学式为________ ;
(2)写出B的电子式______________ 。
(3)写出B +水→C的化学反应方程式_______ 。
(4)B和E反应也可生成H,则该反应的化学方程式为____ 。

(1) G的化学式为
(2)写出B的电子式
(3)写出B +水→C的化学反应方程式
(4)B和E反应也可生成H,则该反应的化学方程式为
您最近一年使用:0次
名校
8 . 有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A与气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:B:________ E:________ 。
(2)写出EB4的化学式:__________ 。
(3)D2A2中含有的化学键类型为____________ 。
(4)由A、C、D三种元素组成的化合物M属于________ (填“离子”或“共价”)化合物,M溶于水后________ (填“能”或“不能”)发生化学变化,原因是(从化学键变化的角度解释):___________________________________ 。
(1)写出下列元素的名称:B:
(2)写出EB4的化学式:
(3)D2A2中含有的化学键类型为
(4)由A、C、D三种元素组成的化合物M属于
您最近一年使用:0次
2017-05-05更新
|
308次组卷
|
2卷引用:湖南省长沙市明德中学2015-2016学年高一(文化班)下学期期中考试化学试题
10-11高一下·安徽蚌埠·期中
解题方法
9 . 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。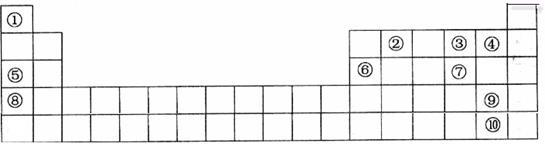
用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是_____________ ;
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是__________________________ ;
③、④、⑦氢化物稳定性由强到弱的顺序是___________________________________ ;
(3)①与⑤按原子个数1:1所成的化合物的电子式为__________________________ ;该化合物与水反应的离子方程式为________________________________________________ 。
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为__________________________ ;
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱:________________ 。

用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是
③、④、⑦氢化物稳定性由强到弱的顺序是
(3)①与⑤按原子个数1:1所成的化合物的电子式为
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱:
您最近一年使用:0次
解题方法
10 . 有A、B、C、D、E、F六种短周期元素,原子序数依次增大,B、C、D的阳离子、A的阴离子均具有与氖原子相同的电子层结构;A、B可形成离子化合物B2A;D的最高价氧化物既能与强酸反应,又能与强碱反应;E的原子结构示意图为: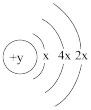 ;F的最外层电子数是电子层数的2倍。试回答下列各问题:
;F的最外层电子数是电子层数的2倍。试回答下列各问题:
(1)B元素为_________ (填元素符号)
(2)F元素位于元素周期表中第_______ 周期第______ 族
(3)化合物B2A的电子式____________________
(4)D的最高价氧化物与B的最高价氧化物对应的水化物溶液反应的离子方程式:________
(5)将C、D用导线相连浸入B的最高价氧化物对应的水化物的溶液中,形成原电池,正极的电极反应为_______________________
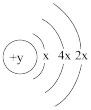 ;F的最外层电子数是电子层数的2倍。试回答下列各问题:
;F的最外层电子数是电子层数的2倍。试回答下列各问题:(1)B元素为
(2)F元素位于元素周期表中第
(3)化合物B2A的电子式
(4)D的最高价氧化物与B的最高价氧化物对应的水化物溶液反应的离子方程式:
(5)将C、D用导线相连浸入B的最高价氧化物对应的水化物的溶液中,形成原电池,正极的电极反应为
您最近一年使用:0次



