名校
解题方法
1 . 五种短周期元素在周期表中的位置如图所示。已知:W元素原子的最外层电子数是次外层的2倍,下列说法正确的是

| A.5种元素最高价氧化物的水化物都是酸 |
| B.WZ4、MX2中所含化学键类型相同,熔点都很高 |
| C.简单氢化物的稳定性:X>Y |
| D.只有一种X的氢化物与Y的氧化物发生反应生成强酸 |
您最近半年使用:0次
名校
解题方法
2 . 现有H、N、O、Na、S、Cl、Fe、Cu八种常见元素,回答下列问题:
(1)S在周期表中的位置____________ ;
(2)Na+ 离子的结构示意图为__________________ ;
(3)能说明非金属性Cl比S强的事实是_____________ (用化学方程式表示);
(4)物质A~L是由上述八种元素中的一种、二种或三种组成,A的摩尔质量166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E都为氢氧化物,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如图所示的关系(部分反应条件及产物已略去):
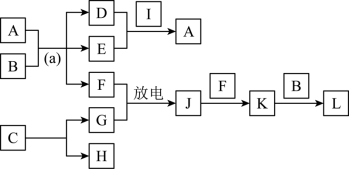
①C的化学式为____________________ ;
②D的电子式为____________________ ;
③L的稀溶液与H反应的离子方程式为___________________________________________ ;
④反应(a)的化学方程式为_________________________________________ 。
(1)S在周期表中的位置
(2)Na+ 离子的结构示意图为
(3)能说明非金属性Cl比S强的事实是
(4)物质A~L是由上述八种元素中的一种、二种或三种组成,A的摩尔质量166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E都为氢氧化物,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如图所示的关系(部分反应条件及产物已略去):

①C的化学式为
②D的电子式为
③L的稀溶液与H反应的离子方程式为
④反应(a)的化学方程式为
您最近半年使用:0次
名校
解题方法
3 . 短周期主族元素X、Y、Z、G、T的原子序数依次增大,Z、G是金属元素且G的氧化物属于两性氧化物,T的原子序数是Y的2倍且T、Y的最低化合价相同。这5种元素的价电子数之和等于20,含Z元素的物质的焰色呈黄色。回答下列问题:
(1)X的最高价氧化物对应水化物的化学式为___________ 。位于元素周期表中s区的元素为___________ (填元素符号)。
(2)Y、Z、G、T的电负性由小到大的顺序为___________ (填元素符号)。
(3) 分子是
分子是___________ (填“极性”或“非极性”)分子。 分子中T的价层电子对数为
分子中T的价层电子对数为___________ 。
(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为___________ 。
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型___________ 。
(6)T的一种单质的结构如图所示: ,T原子杂化类型是
,T原子杂化类型是________ 。32gT的这种单质含σ键的数目为________ 。这种单质易溶于 ,不溶于水,其原因是
,不溶于水,其原因是_________ 。
(1)X的最高价氧化物对应水化物的化学式为
(2)Y、Z、G、T的电负性由小到大的顺序为
(3)
 分子是
分子是 分子中T的价层电子对数为
分子中T的价层电子对数为(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型
(6)T的一种单质的结构如图所示:
 ,T原子杂化类型是
,T原子杂化类型是 ,不溶于水,其原因是
,不溶于水,其原因是
您最近半年使用:0次
2023-04-28更新
|
174次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高二下学期4月期中考试化学试题
名校
解题方法
4 . W、X、Y、Z、M、G、H七种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、G同主族,可形成GY2、GY3两种分子;X的气态氢化物与其最高价氧化物的水化物能反应;H不是稀有气体元素,W、X、Y、Z、M、G、H的最外层电子数之和等于29。请回答下列问题:
(1)Y在元素周期表中的位置为_______ 。
(2)Y、Z、G三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)上述元素的最高价氧化物对应水化物的碱性最强的是_______ (填化学式),Z、M最高价氧化物对应的水化物相互反应的离子方程式为_______ ,X的气态氢化物的催化氧化反应的化学方程式为_______ 。
(4)G的非金属性_______ (填“>”或“<”)H的非金属性,下列表述可以作为验证的证据的是_______ (填字母)。
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、FeH3
D.比较这两种元素单质与酸或碱反应的难易程度
(1)Y在元素周期表中的位置为
(2)Y、Z、G三种元素原子半径由大到小的顺序是
(3)上述元素的最高价氧化物对应水化物的碱性最强的是
(4)G的非金属性
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易程度
C.G和H单质分别与Fe反应生成FeG、FeH3
D.比较这两种元素单质与酸或碱反应的难易程度
您最近半年使用:0次
2023-04-27更新
|
430次组卷
|
2卷引用:广西示范性高中2022-2023学年高一下学期4月期中联合调研测试化学试题
名校
解题方法
5 . X、Y、Z是原子序数依次增大的短周期元素,可“组合”成一种具有高效催化性能的超分子,其结构如图(注:实线代表共价键,其他Y原子之间的重复单元中的W、X未展开标注),W、X、Z分别位于不同周期, Z是同周期中金属性最强的元素。下列说法不正确的是
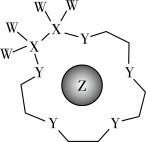
| A.Y位于第二周期第ⅥA族 |
| B.XW4形成的晶体堆积属于分子密堆积 |
| C.X单质不存在能导电的晶体 |
| D.Y与Z可组成阴阳离子数之比为1:2的离子晶体 |
您最近半年使用:0次
2022-05-02更新
|
934次组卷
|
5卷引用:山东省淄博市2021-2022学年高二下学期期中考试化学试题
山东省淄博市2021-2022学年高二下学期期中考试化学试题东北育才学校超常教育实验部(少32届)2022届高三第十次模拟考试化学试题辽宁省大连市第一〇三中学2022届高三第八次考试化学试题(已下线)河北省部分学校2022-2023学年高三上学期期末考试变式汇编(10-13)陕西省西安市第八十三中学2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
6 . 2020年某科研团队经多次实验发现一种新型漂白剂(结构见图),可用于漂白蚕丝等织品,其组成元素均为短周期元素,W、X对应的简单离子核外电子排布相同,且W、Y、Z的最外层电子数之和等于X的最外层电子数,下列说法错误的是
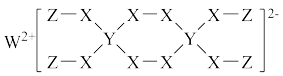

| A.四种元素中X的电负性最大 |
| B.该物质中各原子或离子均达到2或8电子稳定结构 |
| C.Y的最高价氧化物的水化物是一元弱酸 |
| D.离子半径:Z+ <X2- ˂W2+ |
您最近半年使用:0次
2021-11-06更新
|
429次组卷
|
3卷引用:广东省普宁市华侨中学2021-2022学年高二下学期期中考试化学试题
解题方法
7 . 几种短周期元素的原子半径及主要化合价如表。下列叙述正确的是
| 元素符号 | X | Y | Z | W | Q |
| 原子半径 | 160 | 143 | 70 | 66 | 102 |
| 主要化合物 | +2 | +3 | +5、—3 | —2 | +6、—2 |
| A.X、Y元素的金属性X<Y |
| B.一定条件下,W单质与Q的常见单质直接生成QW3 |
| C.Z的最高价氧化物对应的水化物是一种弱酸 |
| D.氢化物的沸点H2W>H2Q |
您最近半年使用:0次
名校
解题方法
8 . X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲俗称苛性钠,由X、Z、Q三种元素组成。Q是短周期中金属性最强的元素,W与Z同主族。请回答下列问题:
(1)W在周期表中的位置为_____ ,R的离子结构示意图为_____ ,Q2Z2的电子式为_____ ,化合物甲中含有的化学键为_____ 。
(2)Y元素是自然界各种生物体生命活动不可缺少的重要元素,其气态氢化物丙与最高价氧化物对应水化物丁能发生化合反应,则Y元素为_____ (填元素符号),过量铁粉与丁的稀溶液反应的离子方程式为____ ,丙与NO在一定条件下能反应生成无毒无污染的物质,该反应的化学方程式为_____ 。
(3)化合物W2R2(沸点:138℃)可与水反应生成一种能使品红溶液褪色的气体,0.1mol该物质参加反应时转移0.15mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为_____ 。
(1)W在周期表中的位置为
(2)Y元素是自然界各种生物体生命活动不可缺少的重要元素,其气态氢化物丙与最高价氧化物对应水化物丁能发生化合反应,则Y元素为
(3)化合物W2R2(沸点:138℃)可与水反应生成一种能使品红溶液褪色的气体,0.1mol该物质参加反应时转移0.15mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
您最近半年使用:0次
解题方法
9 . 甲是一种含结晶水的盐,由A、B、C、D、E五种原子序数依次增大的短周期元素组成。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。B元素原子核内质子数比C的少1,C、E处于同主族。用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中,向其中加入稀盐酸,无现象。再加入BaCl2溶液,出现白色沉淀。
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如图所示。
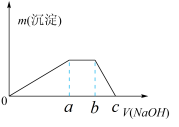
(1)D的元素符号是___________ E在周期表中的位置是___________ 。
(2)B、C、E的简单气态氢化物的沸点高低顺序为___________ (用化学式表示,下同);相同条件下,等物质的量浓度的B和E的最高价氧化物对应的水化物的水溶液,pH较小的是___________ 。
(3)经测定甲晶体的摩尔质量为453 g/mol,其中阳离子和阴离子物质的量之比为 ,则甲晶体的化学式为
,则甲晶体的化学式为___________ 。
(4)实验③中根据图象得V(Oa):V(ab):V(bc)=___________ 。
(5)B的最高价氧化物对应的水化物的极稀的溶液,与D的单质反应时,还原产物可用作化肥,该物质溶于水时会吸热。写出该反应的离子方程式___________ 。
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中,向其中加入稀盐酸,无现象。再加入BaCl2溶液,出现白色沉淀。
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如图所示。

(1)D的元素符号是
(2)B、C、E的简单气态氢化物的沸点高低顺序为
(3)经测定甲晶体的摩尔质量为453 g/mol,其中阳离子和阴离子物质的量之比为
 ,则甲晶体的化学式为
,则甲晶体的化学式为(4)实验③中根据图象得V(Oa):V(ab):V(bc)=
(5)B的最高价氧化物对应的水化物的极稀的溶液,与D的单质反应时,还原产物可用作化肥,该物质溶于水时会吸热。写出该反应的离子方程式
您最近半年使用:0次
名校
解题方法
10 . A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为_________________ 。写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式________________________________ 。
(2)由A、B两种元素组成的18电子微粒的分子式为____________________ 。
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_________________________________________ 。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是_________ L(标准状况下)。
(1)E元素在周期表中的位置为
(2)由A、B两种元素组成的18电子微粒的分子式为
(3)经测定A2W2为二元弱酸,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是
您最近半年使用:0次



