2022·浙江·模拟预测
解题方法
1 . 固体X是四种短周期元素组成的化合物,X的性质与铵盐相似。为探究固体X的组成,取3.28g X,与含NaOH 0.04mol的溶液恰好发生复分解反应,得溶液A(溶液A中含两种溶质,其中一种溶质的相对分子质量为33),将溶液A分成 和
和 两等份,完成如下实验(
两等份,完成如下实验( 与0.02mol硝酸恰好反应,无色气体B在标准状况下的体积为896mL,在空气中变成红棕色):
与0.02mol硝酸恰好反应,无色气体B在标准状况下的体积为896mL,在空气中变成红棕色):
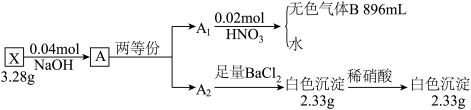
(1)组成X的四种元素是_________ (填元素符号),X的化学式为_________ 。
(2)A中某种溶质与AgBr反应可生成两种单质,化学方程式为_________ 。
(3)写出X的水溶液与 溶液反应生成白色沉淀的离子方程式:
溶液反应生成白色沉淀的离子方程式:_________ 。
(4)为探究 和NaOH的反应,设计实验方案如下:向含
和NaOH的反应,设计实验方案如下:向含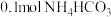 的溶液中加入0.1mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀生成,则
的溶液中加入0.1mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀生成,则 与NaOH的反应可能为
与NaOH的反应可能为_________ (写离子方程式);若无沉淀生成,则 与NaOH的反应可能为
与NaOH的反应可能为_________ (写离子方程式)。该实验方案有无不妥之处?若有,提出修正意见:_________ 。
 和
和 两等份,完成如下实验(
两等份,完成如下实验( 与0.02mol硝酸恰好反应,无色气体B在标准状况下的体积为896mL,在空气中变成红棕色):
与0.02mol硝酸恰好反应,无色气体B在标准状况下的体积为896mL,在空气中变成红棕色):
(1)组成X的四种元素是
(2)A中某种溶质与AgBr反应可生成两种单质,化学方程式为
(3)写出X的水溶液与
 溶液反应生成白色沉淀的离子方程式:
溶液反应生成白色沉淀的离子方程式:(4)为探究
 和NaOH的反应,设计实验方案如下:向含
和NaOH的反应,设计实验方案如下:向含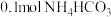 的溶液中加入0.1mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀生成,则
的溶液中加入0.1mol NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀生成,则 与NaOH的反应可能为
与NaOH的反应可能为 与NaOH的反应可能为
与NaOH的反应可能为
您最近一年使用:0次
解题方法
2 . 盐X只含四种短周期元素,按如下流程进行实验:
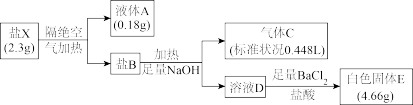
已知:气体C能使湿润红色石蕊变蓝。
请回答:
(1)盐X含_______ (填元素符号),气体C的VSEPR模型为_______ 。
(2)盐X与足量NaOH溶液在加热条件下的离子方程式_______ 。
(3)盐B对应的酸常温常压下为无色结晶性粉末,主要用于氧化剂、磺化剂及硝化反应中的脱水剂,制染料、炸药,石油产品精制和其他有机磺酸化合物。根据以上信息判断,下列物质中一定条件下能与该酸反应的是_______。
(4)工业上盐B重要的用途之一是溶解难溶氧化物生成常见的盐,请写出盐B与 反应的化学方程式
反应的化学方程式_______ 。

已知:气体C能使湿润红色石蕊变蓝。
请回答:
(1)盐X含
(2)盐X与足量NaOH溶液在加热条件下的离子方程式
(3)盐B对应的酸常温常压下为无色结晶性粉末,主要用于氧化剂、磺化剂及硝化反应中的脱水剂,制染料、炸药,石油产品精制和其他有机磺酸化合物。根据以上信息判断,下列物质中一定条件下能与该酸反应的是_______。
| A.甲苯 | B. | C. | D.Cu |
 反应的化学方程式
反应的化学方程式
您最近一年使用:0次
名校
解题方法
3 . 由团簇分子构成的物质X(由四种短周期元素组成)具有良好性能,为测定其组成进行如下实验(所加试剂均过量):
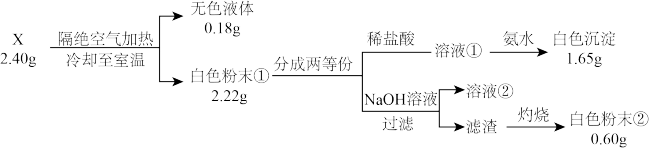
请回答下列问题:
(1)X的组成元素名称是_______ 。
(2)X的化学式为_______ 。
(3)溶液②中通入CO2时开始没有沉淀,过一段时间后生成白色沉淀,写出生成沉淀的离子方程式_______ 。过滤出此沉淀,与Na2CO3、HF气体共热到400-700℃,可生成NaxYF6(Y为沉淀中金属元素),写出此反应的化学方程式(需明确x的值)_______ 。
(4)白色沉淀可用于建筑材料的阻燃涂料,写出两条该沉淀用于阻燃的原因:______ ,_______ 。
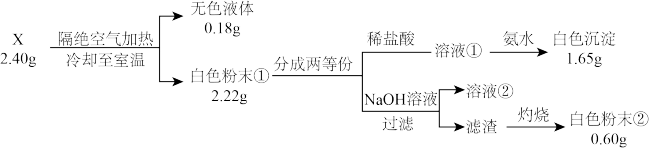
请回答下列问题:
(1)X的组成元素名称是
(2)X的化学式为
(3)溶液②中通入CO2时开始没有沉淀,过一段时间后生成白色沉淀,写出生成沉淀的离子方程式
(4)白色沉淀可用于建筑材料的阻燃涂料,写出两条该沉淀用于阻燃的原因:
您最近一年使用:0次
名校
4 . 固体X是由3种元素组成的化合物,它是某半导体材料的主要成分。某学习小组开展了如下实验进

已知:气体A能使品红试液褪色:白色固体H具有两性。
请回答:
(1)固体X所含的元素有_______ (填元素符号),固体混合物D的成分为_______ 。
(2)固体X在空气中灼烧的化学方程式为_______ ;白色固体H与NaOH溶液反应的离子方程式为_______ 。
(3)单质E在潮湿空气中发生腐蚀,生成一种不含结晶水的碱式盐,该盐中金属阳离子(+2价)与酸根离子物质的量之比为2:1,该反应的化学方程式为_______ 。

已知:气体A能使品红试液褪色:白色固体H具有两性。
请回答:
(1)固体X所含的元素有
(2)固体X在空气中灼烧的化学方程式为
(3)单质E在潮湿空气中发生腐蚀,生成一种不含结晶水的碱式盐,该盐中金属阳离子(+2价)与酸根离子物质的量之比为2:1,该反应的化学方程式为
您最近一年使用:0次
名校
5 . 有某固体化合物X(含有三种短周期元素)是一种络合氢化物储氢材料,X中某种元素的单质可用于制造信号弹。某实验员对固体化合物X作如图实验: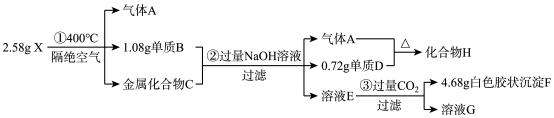
其中:X由三种短周期元素组成,且阴、阳离子个数比为2:1;金属互化物——全部由金属元素组成的化合物。请回答:
(1)化合物X的组成元素___________ ,写出H的电子式___________ 。
(2)X在400℃分解的化学方程式___________ 。
(3)溶液E和过量CO2发生反应的离子方程式为___________ 。
(4)金属互化物C分别与足量盐酸和足量氢氧化钠溶液反应产生的气体物质的量之比为___________ 。
(5)气体A与单质D制备化合物H的过程中,通常产物中会夹杂单质D,请设计实验方案,检验产品中是否含有单质D:___________ 。

其中:X由三种短周期元素组成,且阴、阳离子个数比为2:1;金属互化物——全部由金属元素组成的化合物。请回答:
(1)化合物X的组成元素
(2)X在400℃分解的化学方程式
(3)溶液E和过量CO2发生反应的离子方程式为
(4)金属互化物C分别与足量盐酸和足量氢氧化钠溶液反应产生的气体物质的量之比为
(5)气体A与单质D制备化合物H的过程中,通常产物中会夹杂单质D,请设计实验方案,检验产品中是否含有单质D:
您最近一年使用:0次
2022-08-26更新
|
510次组卷
|
3卷引用:浙江省舟山市舟山中学2022-2023学年国庆返校检测高三化学试题
浙江省舟山市舟山中学2022-2023学年国庆返校检测高三化学试题(已下线)第五章 物质结构 元素周期律(测)-2023年高考化学一轮复习讲练测(全国通用) 山东省青岛第五十八中学2022-2023学年高一下学期3月月考化学试题
解题方法
6 . 固体X由4种元素组成的化合物,它是一种重要的催化剂。某学习小组开展了如图实验进行探究:
实验一:
实验二:
已知:黄色溶液A和无色溶液F仅含一种溶质。
(1)X的组成元素___ ,X的化学式____ 。
(2)写出固体X与氢氧化钠溶液反应的化学方程式____ 。
(3)溶液B和溶液C均含有与冰晶石中结构类似的阴离子,写出B转化成C的离子方程式____ 。
(4)黄色溶液A中的水合金属阳离子为浅紫色,溶液A呈黄色的原因是____ 。为了观察溶液A中的水合金属阳离子为浅紫色,可以采取____ 的措施。
实验一:

实验二:

已知:黄色溶液A和无色溶液F仅含一种溶质。
(1)X的组成元素
(2)写出固体X与氢氧化钠溶液反应的化学方程式
(3)溶液B和溶液C均含有与冰晶石中结构类似的阴离子,写出B转化成C的离子方程式
(4)黄色溶液A中的水合金属阳离子为浅紫色,溶液A呈黄色的原因是
您最近一年使用:0次
名校
7 . 某化合物W由三种元素组成,其中一种为金属元素M,为测定其组成,某小组选择乙醚溶液为实验溶剂,进行如下实验:
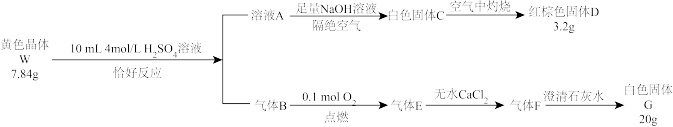
已知:气体B是由两种气体(其一为单质)组成的混合气体,皆可燃烧;气体F为常见温室气体。
请回答:
(1)气体E的组成是_______ (用化学式表示)
(2)经X射线衍射研究,W晶体的空间结构为三角双锥,中心原子M配位数为5,且满足18电子规则,即价层轨道全充满电子,由此进一步推写出W的化学式为_______ ,且在W晶体中M的化合价为_______ 。
(3)在丙酮中W可被氯化铜完全氧化,其产物中金属元素价态与溶液A中金属阳离子价态相同,同时生成一种气体,是气体B的组成成分之一,此外,还生成一种白色固体,该固体化学性质不稳定,在空气中会被迅速氧化;根据信息,写出该转化过程中的化学方程式:_______ 。
(4)若将白色固体C置于空气中较长一段时间,可观察到固体颜色发生如下转变:白色→颜色1→颜色2,请设计实验验证颜色1固体中存在的阳离子情况:_______ 。

已知:气体B是由两种气体(其一为单质)组成的混合气体,皆可燃烧;气体F为常见温室气体。
请回答:
(1)气体E的组成是
(2)经X射线衍射研究,W晶体的空间结构为三角双锥,中心原子M配位数为5,且满足18电子规则,即价层轨道全充满电子,由此进一步推写出W的化学式为
(3)在丙酮中W可被氯化铜完全氧化,其产物中金属元素价态与溶液A中金属阳离子价态相同,同时生成一种气体,是气体B的组成成分之一,此外,还生成一种白色固体,该固体化学性质不稳定,在空气中会被迅速氧化;根据信息,写出该转化过程中的化学方程式:
(4)若将白色固体C置于空气中较长一段时间,可观察到固体颜色发生如下转变:白色→颜色1→颜色2,请设计实验验证颜色1固体中存在的阳离子情况:
您最近一年使用:0次
8 . 短周期元素A、D、E、F、W原子序数依次递增,已知:
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
③W的各级电离能如图。
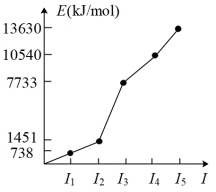
请回答:
(1)D、E、F三元素的第一电离能由大到小的顺序是___________ (用元素符号表示)。
(2)写出一种由上述元素形成氢键的表达式___________ 。
(3)元素W在周期表中的位置是___________ 。
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
③W的各级电离能如图。

请回答:
(1)D、E、F三元素的第一电离能由大到小的顺序是
(2)写出一种由上述元素形成氢键的表达式
(3)元素W在周期表中的位置是
您最近一年使用:0次
9 . 已知A、B、C、D、E都是周期表中前四周期的元素,原子序数依次增大,其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子,B、C的简单氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的简单氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_______ 。
(2)E的价层轨道表示式是_______ ECl3形成的配合物的化学式为_______ 。
(3)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是_______ 。
(4)化合物NH3与BF3可以通过配位键形成NH3∙BF3。写出NH3∙BF3的结构式 ,并用“→”标出配位键_______ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)E的价层轨道表示式是
(3)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
(4)化合物NH3与BF3可以通过配位键形成NH3∙BF3。写出NH3∙BF3的
您最近一年使用:0次
10 . 化合物X是由4种元素组成的盐,不含结晶水。某兴趣小组按如图流程进行实验(所加试剂均足量):
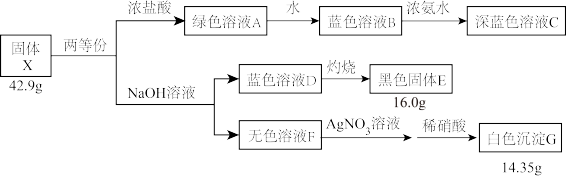
已知:溶液A、B、C中均含有结构相似的配离子,溶液F中的阳离子和酸根离子均只有一种(忽略水的电离)。
请回答:
(1)组成X的元素有____ ,X的化学式为____ 。
(2)根据A→B→C的现象,给出相应微粒与阳离子结合由弱到强的排序____ 。
(3)X与足量NaOH溶液反应的化学方程式是____ 。
(4)蓝色溶液B与Na2SO3作用,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀H(H为二元化合物)。
①写出该反应的离子方程式____ 。
②设计实验验证白色沉淀H的组成元素____ 。

已知:溶液A、B、C中均含有结构相似的配离子,溶液F中的阳离子和酸根离子均只有一种(忽略水的电离)。
请回答:
(1)组成X的元素有
(2)根据A→B→C的现象,给出相应微粒与阳离子结合由弱到强的排序
(3)X与足量NaOH溶液反应的化学方程式是
(4)蓝色溶液B与Na2SO3作用,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀H(H为二元化合物)。
①写出该反应的离子方程式
②设计实验验证白色沉淀H的组成元素
您最近一年使用:0次



