名校
解题方法
1 . X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,X元素可以组成M和N两种气态单质,常用反应:M+2I-+2H+=I2+N+H2O做M的鉴定反应,也可用带火星的木条检验M。
(1)写出实验室制取W2的离子方程式_______ 。
(2)某化学兴趣小组设计如图所示的实验装置(图中夹持和加热装置略去),分别探究YX2和W2的性质。
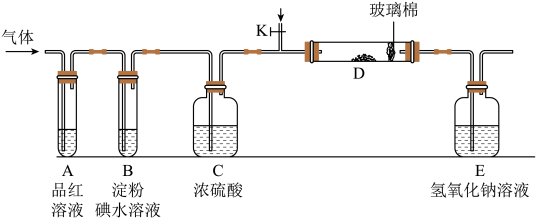
①若装置D中装的是铁粉,当通入W2时,灼热D时观察到_______ 现象。若装置D中装的是五氧化二钒(V2O5),当通入YX2时,打开K放入适量的氧气,灼热D装置,发生反应的化学方程式为_______ 。
②若装置B中装有5.0mL1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程为_______ 。
③某同学将足量的YX2通入一支装有BaCl2溶液的试管,未见沉淀生成,向该试管中加入适量_______ (填字母),可以看到白色沉淀产生。
A.氨水 B.稀盐酸 C.稀硝酸 D.CaCl2溶液
④物质Y2W2是有恶臭,毒性的液体,各原子满足8电子稳定结构,写出Y2W2的结构式_______ 。
(1)写出实验室制取W2的离子方程式
(2)某化学兴趣小组设计如图所示的实验装置(图中夹持和加热装置略去),分别探究YX2和W2的性质。

①若装置D中装的是铁粉,当通入W2时,灼热D时观察到
②若装置B中装有5.0mL1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程为
③某同学将足量的YX2通入一支装有BaCl2溶液的试管,未见沉淀生成,向该试管中加入适量
A.氨水 B.稀盐酸 C.稀硝酸 D.CaCl2溶液
④物质Y2W2是有恶臭,毒性的液体,各原子满足8电子稳定结构,写出Y2W2的结构式
您最近一年使用:0次
解题方法
2 . X、Y、Z、M为原子序数依次增大的短周期主族元素,这四种元素原子的最外层电子数之和等于12。A~G是由上述四种元素组成的化合物,其转化关系如图所示,其中C是一种强碱,焰色试验呈黄色。

回答下列问题:
(1)元素Y在元素周期表中的位置是___________ 。
(2)Y、Z、M三种元素的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)能说明Z的非金属性强于Y的依据是___________ (写一点即可)。
(4)写出反应①的离子方程式___________ 。
(5)去除A溶液中混有的少量B的方法是___________ 。
(6)3.9g固体D与足量F反应转移的电子数目为___________ 。
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是___________ (填标号)。
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng

回答下列问题:
(1)元素Y在元素周期表中的位置是
(2)Y、Z、M三种元素的原子半径由大到小的顺序为
(3)能说明Z的非金属性强于Y的依据是
(4)写出反应①的离子方程式
(5)去除A溶液中混有的少量B的方法是
(6)3.9g固体D与足量F反应转移的电子数目为
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng
您最近一年使用:0次
名校
3 . 有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于第_______ 周期第_______ 族。
(2)用电子式表示B与C形成化合物的过程:_______ 。
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是_______ (填化学式)。
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b. 既有氧化性又有还原性
既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为
d.非金属性比Cl元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,且其水溶液显碱性 |
| B | 单质在焰色试验中显黄色 |
| C | 单质是淡黄绿色气体,可用于自来水消毒 |
| D | -2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中位于第
(2)用电子式表示B与C形成化合物的过程:
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.
 既有氧化性又有还原性
既有氧化性又有还原性c.最高价氧化物对应的水化物的化学式为

d.非金属性比Cl元素的强
您最近一年使用:0次
解题方法
4 . A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3:5,请回答:
(1)F的元素符号为_______ 。
(2)D在元素周期表中的位置_______ 。
(3)用电子式表示由元素B和F组成的化合物的形成过程:_______ 。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关反应的离子方程式为_______ 、_______ 。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物 。该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
。该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为_______ 。
(1)F的元素符号为
(2)D在元素周期表中的位置
(3)用电子式表示由元素B和F组成的化合物的形成过程:
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关反应的离子方程式为
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物
 。该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
。该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
您最近一年使用:0次
5 . X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是(含硫)化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液能使酚酞溶液变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1∶1在水溶液中能发生反应,离子方程式为_______ 。
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是_______ (填化学式);该反应是氧化还原反应,则其中的氧化剂是_______ (填化学式)。
(3)写出Z与水的反应的化学方程式_______ ,此反应中氧化剂与还原剂的物质的量之比_______ 。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1∶1在水溶液中能发生反应,离子方程式为
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是
(3)写出Z与水的反应的化学方程式
您最近一年使用:0次
2022-07-02更新
|
129次组卷
|
2卷引用:河南省许昌市2021-2022学年高一下学期期末教学质量检测化学试题
解题方法
6 . 几种元素的主要化合价如下表所示。
已知B、C、D位于同周期。
请回答下列问题:
(1)C的简单离子的结构示意图为_______ 。A是_______ (填元素名称)。
(2)D的简单氢化物的电子式为_______ 。
(3)D的简单氢化物与D的氧化物能发生氧化还原反应,在该反应中氧化产物与还原产物的物质的量之比为2:1,该反应的化学方程式为_______ 。
(4)已知:化合物BA在熔融状态下能导电,则化合物BA是_______ (填“共价”或“离子”)化合物。
(5)B的单质在O2中燃烧的产物能和A的简单氧化物反应,其离子方程式为_______ 。
(6)设计实验证明B元素原子的失电子能力比C的强:_______ (简要叙述实验过程、现象)。
| 元素代号 | A | B | C | D |
| 原子半径/nm | 0.030 | 0.186 | 0.143 | 0.106 |
| 主要化合价 | +1,—1 | +1 | +3 | +6,—2 |
请回答下列问题:
(1)C的简单离子的结构示意图为
(2)D的简单氢化物的电子式为
(3)D的简单氢化物与D的氧化物能发生氧化还原反应,在该反应中氧化产物与还原产物的物质的量之比为2:1,该反应的化学方程式为
(4)已知:化合物BA在熔融状态下能导电,则化合物BA是
(5)B的单质在O2中燃烧的产物能和A的简单氧化物反应,其离子方程式为
(6)设计实验证明B元素原子的失电子能力比C的强:
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如表:
(1)元素X的原子中能量最高的电子其电子云在空间有____ 方向;它的氢化物的电子式是____ 。
(2)元素Y位于元素周期表的位置为____ 。
(3)W的基态原子核外电子排布式是____ 。
(4)元素Y与元素Z相比,非金属性较强的是____ (用元素符号表示),下列表述中能证明这一事实的是____ 。
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且最高能级是半充满状态 |
| Y | 第三周期元素,它的单质是良好的半导体材料 |
| Z | Z和Y同周期,Z是本周期原子半径最小的主族元素 |
| W | W的一种核素的质量数为63,中子数为34 |
(1)元素X的原子中能量最高的电子其电子云在空间有
(2)元素Y位于元素周期表的位置为
(3)W的基态原子核外电子排布式是
(4)元素Y与元素Z相比,非金属性较强的是
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
您最近一年使用:0次
解题方法
8 . X、Y、Z、W为原子序数依次增大的短周期主族元素,X2-和Y+具有相同的电子层结构;Z、W为同周期元素,Z元素原子核外电子总数是最外层电子数的3倍;W元素原子最外层有一个未成对电子。回答下列问题:
(1)上述四种元素基态原子的未成对电子数最多的是_______ (填元素符号),其中基态Z原子的核外电子排布式为_______ 。
(2)X有两种常见的同素异形体,其中沸点较高的是_______ (填化学式),其沸点较高的原因是_______ ;X和Y的氢化物所属的晶体类型分别为_______ 和_______ 。
(3)Z和W可按原子个数比1:3形成化合物E,E分子的空间构型为_______ ,中心原子的杂化轨道类型为_______ 。
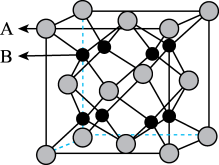
(4)X和Y能够形成化合物F。其晶胞结构如图所示,晶胞参数为anm,F的化学式为_______ ;晶体中X原子的配位数为_______ ;晶体F的密度为_______ g·cm-3(NA为阿伏加德罗常数的值,列出式子即可)。
(1)上述四种元素基态原子的未成对电子数最多的是
(2)X有两种常见的同素异形体,其中沸点较高的是
(3)Z和W可按原子个数比1:3形成化合物E,E分子的空间构型为
(4)X和Y能够形成化合物F。其晶胞结构如图所示,晶胞参数为anm,F的化学式为

您最近一年使用:0次
解题方法
9 . 现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大,其中Z、Q在同一周期。相关信息如下表:
回答下列问题:
(1)X元素的名称是_______ 。元素周期表中X元素与铝元素处于对角线位置,性质相似,请写出X元素的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式_______ 。
(2)Y、Q两种元素能形成化合物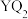 ,其化学键类型与Y元素的氧化物
,其化学键类型与Y元素的氧化物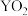 相同,请写出
相同,请写出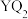 的电子式
的电子式_______ 。
(3)将Q元素的低价氧化物通入到 溶液中,无明显变化,再向其中加入Z的最高价氧化物对应的水化物,可观察到的现象是
溶液中,无明显变化,再向其中加入Z的最高价氧化物对应的水化物,可观察到的现象是_______ ,发生反应的离子方程式是_______ 。
| 元素 | 相关信息 |
| X | 最外层电子数是核外电子总数的一半 |
| Y | 最高化合价与最低化合价之和为零 |
| Z | 同周期元素中原子半径最大 |
| Q | 单质为淡黄色固体,常存在于火山喷口附近 |
(1)X元素的名称是
(2)Y、Q两种元素能形成化合物
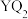 ,其化学键类型与Y元素的氧化物
,其化学键类型与Y元素的氧化物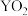 相同,请写出
相同,请写出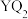 的电子式
的电子式(3)将Q元素的低价氧化物通入到
 溶液中,无明显变化,再向其中加入Z的最高价氧化物对应的水化物,可观察到的现象是
溶液中,无明显变化,再向其中加入Z的最高价氧化物对应的水化物,可观察到的现象是
您最近一年使用:0次
名校
10 . 原子序数由小到大排列的四种短周期元素 、
、 、
、 、
、 ,其中
,其中 、
、 、
、 与氢元素可组成
与氢元素可组成 、
、 和
和 三种共价化合物;
三种共价化合物; 与氧元素可组成
与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。
(1)写出 的电子式:
的电子式:___________ 。其中含有的化学键是___________ 。
(2)用电子式表示 的形成过程
的形成过程___________ 。
(3) 、
、 、
、 三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是___________ (填化学式)。
(4) 、
、 和
和 三种化合物,其中一种与另外两种都能反应的是
三种化合物,其中一种与另外两种都能反应的是___________ (填化学式)。
(5)由 、
、 组成的化合物分子中,
组成的化合物分子中, 、
、 原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式___________ 。
 、
、 、
、 、
、 ,其中
,其中 、
、 、
、 与氢元素可组成
与氢元素可组成 、
、 和
和 三种共价化合物;
三种共价化合物; 与氧元素可组成
与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。(1)写出
 的电子式:
的电子式:(2)用电子式表示
 的形成过程
的形成过程(3)
 、
、 、
、 三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是(4)
 、
、 和
和 三种化合物,其中一种与另外两种都能反应的是
三种化合物,其中一种与另外两种都能反应的是(5)由
 、
、 组成的化合物分子中,
组成的化合物分子中, 、
、 原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
您最近一年使用:0次
2022-04-01更新
|
203次组卷
|
13卷引用:河南省新野县第一高级中学校2021-2022学年高一下学期第三次考试化学试题
河南省新野县第一高级中学校2021-2022学年高一下学期第三次考试化学试题四川省成都市树德中学2021-2022学年高一下学期5月阶段性测试化学试题2015-2016学年江西省金溪一中高一下期中化学试卷2015-2016学年中国石油天然气管道局中学高一下第二次月考化学试卷2016-2017学年辽宁省庄河高级中学高二上开学测化学试卷2018版化学(苏教版)高考总复习专题五课时跟踪训练--微粒之间的相互作用力与物质的多样性山西省运城市康杰中学2017-2018学年高一下学期期中考试化学试题北京四中2017-2018学年高一下学期第二次月考化学试题新疆自治区和田地区和田县喀什塔什乡中学2019届高三年级四月调研考试理综化学试题百所名校联考-必修二模块综合检测黑龙江省哈尔滨市尚志市尚志中学2021届高三10月月考化学试题(已下线)第8单元 原子结构 元素周期律(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷海南省华中师范大学海南附属中学2021届高三上学期第四次月考化学试题



