名校
1 . X、Y、Z、W均为短周期主族元素,X、Y、Z原子的最外层电子数之和为10。X与Z同族,Y最外层电子数等于X次外层电子数,且Y原子半径大于Z。W的最外层电子数等于X的核外电子总数,且W单质常温下为固体。请回答下列问题:
(1)X、Y、Z三种元素对应的原子半径大小关系为____________ (填元素符号)。
(2)Y与X的最高价氧化物在点燃条件下的现象是剧烈燃烧,放出大量热,产生耀眼的白光,生成白色固体和黑色粉末,则该反应的化学方程式为___________ 。
(3)下列说法正确的是_______ 。
A.W的氢化物,所有原子均满足8e-稳定结构
B.最高价氧化物对应的水化物的酸性W>Z
C.由于Z的氧化物ZO2既可与酸反应,又能与碱反应,所以ZO2为两性氧化物
D.W的氧化物WO2,具有还原性,能使酸性KMnO4溶液褪色
(4)足量的单质Y与一定量的W的最高价氧化物对应的水化物的浓溶液,在一定条件下充分反应,所得气体的成分为_______ 。
(1)X、Y、Z三种元素对应的原子半径大小关系为
(2)Y与X的最高价氧化物在点燃条件下的现象是剧烈燃烧,放出大量热,产生耀眼的白光,生成白色固体和黑色粉末,则该反应的化学方程式为
(3)下列说法正确的是
A.W的氢化物,所有原子均满足8e-稳定结构
B.最高价氧化物对应的水化物的酸性W>Z
C.由于Z的氧化物ZO2既可与酸反应,又能与碱反应,所以ZO2为两性氧化物
D.W的氧化物WO2,具有还原性,能使酸性KMnO4溶液褪色
(4)足量的单质Y与一定量的W的最高价氧化物对应的水化物的浓溶液,在一定条件下充分反应,所得气体的成分为
您最近一年使用:0次
名校
解题方法
2 . X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次增大的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1,且溶于水呈碱性;W的质子数是X、Y、Z、M四种元素质子数之和的 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.简单离子半径:W+>Y3->Z2->M+ |
| B.W2Z2可用于作供氧剂 |
| C.1 mol WM溶于足量水中完全反应,共转移2 mol电子 |
| D.由X、Y、Z、M四种元素形成的化合物中不可能含有离子键 |
您最近一年使用:0次
2022-04-21更新
|
118次组卷
|
2卷引用:四川省什邡中学2021-2022学年高一下学期第二次月考化学试题
名校
3 . A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A原子M层电子数是L层的一半,B是同周期第一电离能最小的元素,C在同周期中未成对电子数最多,E的外围电子排布式为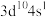 。回答下列问题:
。回答下列问题:
(1)A的基态原子中的电子有_______ 种不同的能量状态,B的基态原子中有_______ 种不同运动状态的电子。
(2)上述元素中最高价氧化物对应水化物酸性最弱的与碱性最强的物质发生反应的方程式是_______ 。
(3)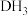 分子的
分子的 模型为
模型为_______ ,E元素在周期表的位置是_______ 。
(4)C与D的简单氢化物熔点相比后者的高,解释原因_______ ,A与碳形成的某晶体可用作打磨砂轮原料,1mol该晶体含有的共价键为_______ 个。
(5)C可形成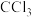 、
、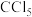 ,D只能形成
,D只能形成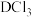 解释原因
解释原因_______ 。
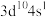 。回答下列问题:
。回答下列问题:(1)A的基态原子中的电子有
(2)上述元素中最高价氧化物对应水化物酸性最弱的与碱性最强的物质发生反应的方程式是
(3)
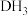 分子的
分子的 模型为
模型为(4)C与D的简单氢化物熔点相比后者的高,解释原因
(5)C可形成
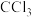 、
、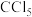 ,D只能形成
,D只能形成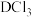 解释原因
解释原因
您最近一年使用:0次
名校
4 . 原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成 、
、 和HW三种共价化合物:Y与氧元素可组成
和HW三种共价化合物:Y与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。
(1)写出 的电子式:
的电子式:_______ ,其中含有的化学键是_______ 。
(2)用电子式表示 的形成过程
的形成过程_______ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是_______ (填化学式)。
(4) 、
、 和HW三种化合物,其中一种与另外两种都能反应的是
和HW三种化合物,其中一种与另外两种都能反应的是_______ (填化学式)
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式_______ 。
 、
、 和HW三种共价化合物:Y与氧元素可组成
和HW三种共价化合物:Y与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。(1)写出
 的电子式:
的电子式:(2)用电子式表示
 的形成过程
的形成过程(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
(4)
 、
、 和HW三种化合物,其中一种与另外两种都能反应的是
和HW三种化合物,其中一种与另外两种都能反应的是(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
您最近一年使用:0次
解题方法
5 . 化合物W可用于农药生产,其结构如图所示,其中X、Y、Z、M、N是原子序数依次增大的短周期主族元素,Y与N同主族。下列说法正确的是
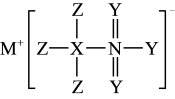
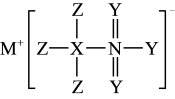
| A.非金属性:Z>Y>X |
| B.简单离子半径:N>M>Y |
| C.元素Z和M形成共价化合物 |
| D.元素Y和M形成的二元化合物都具有强氧化性 |
您最近一年使用:0次
名校
解题方法
6 . 科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,其分子结构示意图如下图,W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大。
下列说法不正确的是
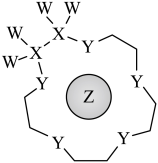
下列说法不正确的是
| A.Y单质的氧化性在同主族中最强 | B.离子半径:Z<Y |
| C.Z与Y可组成多种离子化合物 | D.氢化物的热稳定性:Y<X |
您最近一年使用:0次
2022-10-17更新
|
207次组卷
|
4卷引用:北京市北京师范大学附属实验中学2022-2023学年高三上学期月考化学试题
北京市北京师范大学附属实验中学2022-2023学年高三上学期月考化学试题黑龙江省富锦市第一中学2022-2023学年高一下学期第二次考试化学试题(已下线)20231218+12月月考1737051759696343040北京师范大学实验中学2023-2024学年高三上学期12月月考化学试卷
名校
7 . 下图是元素周期表的一部分。按要求填写下列空白:

(1)元素⑦在周期表中的位置为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物中所含的化学键为_______ ;③的氢化物的电子式为_______ 。
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素⑦在周期表中的位置为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物中所含的化学键为
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
2023-01-31更新
|
192次组卷
|
2卷引用:湖南省永州市第一中学2022-2023学年高一上学期期末阶段性考试化学试题
名校
8 . 原子序数由小到大排列的四种短周期元素 、
、 、
、 、
、 ,其中
,其中 、
、 、
、 与氢元素可组成
与氢元素可组成 、
、 和
和 三种共价化合物;
三种共价化合物; 与氧元素可组成
与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。
(1)写出 的电子式:
的电子式:___________ 。其中含有的化学键是___________ 。
(2)用电子式表示 的形成过程
的形成过程___________ 。
(3) 、
、 、
、 三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是___________ (填化学式)。
(4) 、
、 和
和 三种化合物,其中一种与另外两种都能反应的是
三种化合物,其中一种与另外两种都能反应的是___________ (填化学式)。
(5)由 、
、 组成的化合物分子中,
组成的化合物分子中, 、
、 原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式___________ 。
 、
、 、
、 、
、 ,其中
,其中 、
、 、
、 与氢元素可组成
与氢元素可组成 、
、 和
和 三种共价化合物;
三种共价化合物; 与氧元素可组成
与氧元素可组成 和
和 两种离子化合物。
两种离子化合物。(1)写出
 的电子式:
的电子式:(2)用电子式表示
 的形成过程
的形成过程(3)
 、
、 、
、 三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是(4)
 、
、 和
和 三种化合物,其中一种与另外两种都能反应的是
三种化合物,其中一种与另外两种都能反应的是(5)由
 、
、 组成的化合物分子中,
组成的化合物分子中, 、
、 原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
您最近一年使用:0次
2022-04-01更新
|
206次组卷
|
13卷引用:2015-2016学年江西省金溪一中高一下期中化学试卷
2015-2016学年江西省金溪一中高一下期中化学试卷2015-2016学年中国石油天然气管道局中学高一下第二次月考化学试卷2016-2017学年辽宁省庄河高级中学高二上开学测化学试卷2018版化学(苏教版)高考总复习专题五课时跟踪训练--微粒之间的相互作用力与物质的多样性山西省运城市康杰中学2017-2018学年高一下学期期中考试化学试题北京四中2017-2018学年高一下学期第二次月考化学试题新疆自治区和田地区和田县喀什塔什乡中学2019届高三年级四月调研考试理综化学试题百所名校联考-必修二模块综合检测黑龙江省哈尔滨市尚志市尚志中学2021届高三10月月考化学试题(已下线)第8单元 原子结构 元素周期律(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷海南省华中师范大学海南附属中学2021届高三上学期第四次月考化学试题河南省新野县第一高级中学校2021-2022学年高一下学期第三次考试化学试题四川省成都市树德中学2021-2022学年高一下学期5月阶段性测试化学试题
名校
解题方法
9 . 常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH和原子半径、原子序数的关系如图所示。下列说法不正确的是
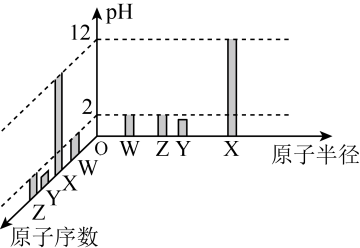

A.第一电离能: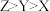 |
B.简单离子的半径: |
| C.W的氢化物空间构型不一定是三角锥形 |
| D.Z的单质具有强氧化性和漂白性 |
您最近一年使用:0次
10 . 已知X、Y、Z、W是同一短周期主族元素。单质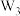 具有强氧化性,可用于杀菌消毒。四种元素与锂离子组成的盐是一种新型的锂离子电池的电解质,结构如图所示(“→”表示配位键)。下列说法正确的是
具有强氧化性,可用于杀菌消毒。四种元素与锂离子组成的盐是一种新型的锂离子电池的电解质,结构如图所示(“→”表示配位键)。下列说法正确的是
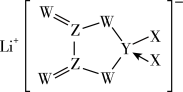
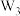 具有强氧化性,可用于杀菌消毒。四种元素与锂离子组成的盐是一种新型的锂离子电池的电解质,结构如图所示(“→”表示配位键)。下列说法正确的是
具有强氧化性,可用于杀菌消毒。四种元素与锂离子组成的盐是一种新型的锂离子电池的电解质,结构如图所示(“→”表示配位键)。下列说法正确的是
| A.原子半径:X>Y>Z>W |
| B.Y的最高价氧化物的水化物为强酸 |
C.单质氧化性: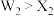 |
| D.阴离子中四种元素的原子均满足8电子稳定结构 |
您最近一年使用:0次



