名校
1 . X、Y、Z为短周期主族元素,且原子序数依次增大,其中Y的最外层电子数是其内层电子数的1.5倍,Z的简单氢化物与其最高价氧化物的水化物反应得到一种盐,这三种元素组成的某化合物的结构如图所示。下列说法错误的是
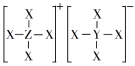
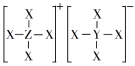
| A.原子半径:Y>Z>X |
| B.Z对应的氧化物均为酸性氧化物 |
| C.Y的最高价氧化物对应的水化物的酸性在同主族元素中最强 |
D.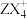 中所有原子都达到稳定结构 中所有原子都达到稳定结构 |
您最近半年使用:0次
名校
2 . A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和D2具有相同的电子数。请回答以下问题:
(1)F位于第_______ 周期第_______ 族。
(2)F的单质与E的氢化物H2E反应的离子方程式_______ 。
(3)用电子式表示D2的形成过程:_______ 。
(4)由A、E、F三种元素形成的化合物的电子式为_______ 。
(5)由A、G组成的化合物的结构式是_______ 。
(1)F位于第
(2)F的单质与E的氢化物H2E反应的离子方程式
(3)用电子式表示D2的形成过程:
(4)由A、E、F三种元素形成的化合物的电子式为
(5)由A、G组成的化合物的结构式是
您最近半年使用:0次
名校
3 . 下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
(1)写出序号对应的元素符号:①________ ;④__________ ;⑤_________ ;
(2)在①~⑨元素中,最活泼的金属元素是________ ,最活泼的非金属元素是_______ 。
(3)在①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是___________ ,呈两性的是____________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | He | ||||||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)写出序号对应的元素符号:①
(2)在①~⑨元素中,最活泼的金属元素是
(3)在①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是
您最近半年使用:0次
2020-12-02更新
|
506次组卷
|
2卷引用:吉林省长春外国语学校2020-2021学年高一上学期期末考试(文科)化学试题
名校
4 . 短周期主族元素R、X、Y和Z在周期表中相对位置如图所示。已知这四种元素的质子数之和等于55。下列说法错误的是
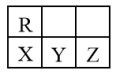

| A.简单阴离子结合氢离子的能力:Y>Z |
| B.常温常压下,R单质呈气态 |
| C.Z的氧化物对应水化物一定是强酸 |
| D.Y和Z组成的化合物是共价化合物 |
您最近半年使用:0次
2020-10-28更新
|
346次组卷
|
4卷引用:吉林省吉林市第二中学2020-2021学年高三上学期11月月考化学试题
名校
解题方法
5 . A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A__________ ,B___________ ;
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:__________ ;
(3)写出A与氧元素形成的原子个数比为1:1的化合物的电子式__________ ;
(4)C、D、E的最高价氧化物水化物的酸性由强到弱的顺序(用化学式表示):________ ;
(5)A、B、D、E形成的简单离子的半径由大到小的顺序(用离子符号表示):_________ ;
(6)A的最高价氧化物的水化物中含有的化学键类型(填离子键、极性键、非极性键)_______ 。
(1)写出下列元素符号:A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A与氧元素形成的原子个数比为1:1的化合物的电子式
(4)C、D、E的最高价氧化物水化物的酸性由强到弱的顺序(用化学式表示):
(5)A、B、D、E形成的简单离子的半径由大到小的顺序(用离子符号表示):
(6)A的最高价氧化物的水化物中含有的化学键类型(填离子键、极性键、非极性键)
您最近半年使用:0次
名校
6 . 下表为元素周期表的一部分, 请参照元素①~@在表中的位置,用化学用语作答:

(1)元素⑤、⑥、⑦、⑨的离子半径由大到小的顺序为_______________ (填离子符号) ;
(2)元素⑧、⑨、⑩的最高价含氧酸的酸性由强到弱的顺序为___________ (用化学式表示);
(3)写出⑥在空气中加热燃烧后产物的电子式:____________________ 。
(4)已知某些不同族元素的性质也有一定的相似性,如元素②与元素⑦的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式:__________________________ 。
(5)已知砷(As)为第VA族元素,位于元素⑧的下一周期,它的化合物可用于杀虫及医疗。
①As的原子结构示意图为________________ 。
②Y是由④⑥⑩三种元素组成的化合物,是生活中常见的消海剂。砷的氢化物可与Y的水溶液反应,生成砷的最高价含氧酸,则该反应的化学方程式为___________________ 。消耗l mol 还原剂时,转移电子的物质的量为_____________ mol。

(1)元素⑤、⑥、⑦、⑨的离子半径由大到小的顺序为
(2)元素⑧、⑨、⑩的最高价含氧酸的酸性由强到弱的顺序为
(3)写出⑥在空气中加热燃烧后产物的电子式:
(4)已知某些不同族元素的性质也有一定的相似性,如元素②与元素⑦的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式:
(5)已知砷(As)为第VA族元素,位于元素⑧的下一周期,它的化合物可用于杀虫及医疗。
①As的原子结构示意图为
②Y是由④⑥⑩三种元素组成的化合物,是生活中常见的消海剂。砷的氢化物可与Y的水溶液反应,生成砷的最高价含氧酸,则该反应的化学方程式为
您最近半年使用:0次
名校
解题方法
7 . 现有七种短周期主族元素,其原子序数按A、B、C、D、E、F、G的顺序递增。A元素的最高正化合价和最低负化合价的代数和等于0,且A的氧化物能够造成温室效应;A、B、C三种元素都能形成10电子分子,且C与F位于同一主族;D与C可形成离子化合物DC;E的简单阳离子是同周期元素所形成的简单离子中半径最小的。回答下列问题:
(1)B位于周期表第______ 周期第______ 族。
(2)请写出B的氢化物可能的电子式_________ 、_________ 。
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为__________ (用化学式表示)。
(4)A的单质与F的最高价氧化物的水化物浓溶液反应的化学方程式为:_________ 。
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为__________ (用化学式表示)。
(6)下列实验方法能证明D与E的金属性强弱关系的是____ (填字母序号)。
A.比较D和E的单质分别与等浓度的稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物的价态
D.比较D和E最高价氧化物的水化物的碱性强弱
(7)4 mol D 单质与含有10 mol B的最价氧化物的水化物溶液恰好完全,则含有B元素的还原产物可能是_______ 、_________ (写出化学式)。
(1)B位于周期表第
(2)请写出B的氢化物可能的电子式
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为
(4)A的单质与F的最高价氧化物的水化物浓溶液反应的化学方程式为:
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为
(6)下列实验方法能证明D与E的金属性强弱关系的是
A.比较D和E的单质分别与等浓度的稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物的价态
D.比较D和E最高价氧化物的水化物的碱性强弱
(7)4 mol D 单质与含有10 mol B的最价氧化物的水化物溶液恰好完全,则含有B元素的还原产物可能是
您最近半年使用:0次
名校
8 . 被誉为“矿石熊猫”的香花石,是由我国地质学家首次发现,它由前20号元素中的6种主族元素组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同一主族,Y、Z、R、T位于同一周期,R元素原子的最外层电子数是次外层电子数的3倍,T无正价,X与R的原子序数之和是W的2倍。下列说法错误的是( )
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.最高价氧化物对应水化物的碱性:X>Z |
| D.XR2、WR2两种化合物中R的化合价相同 |
您最近半年使用:0次
2020-09-07更新
|
2884次组卷
|
51卷引用:吉林省梅河口市第五中学2022届高三上学期第一次月考化学试题
吉林省梅河口市第五中学2022届高三上学期第一次月考化学试题(已下线)2011届浙江省学军中学高三高考模拟考试(理综)化学部分(已下线)2012届浙江省慈溪中学高三上学期期中考试化学试卷(已下线)2014届浙江省六校(省一级重点校)高三3月联考化学试卷(已下线)2013-2014河南省商丘市高三第三次模拟考试理综化学试卷(已下线)2013-2014江西省宜春市高三模拟考试理综化学试卷2015届河南省三门峡市陕州中学高三高考仿真训练(一)化学试卷2016届广东省肇庆市高三上学期期末质检理综化学试卷2015-2016学年山西省临汾一中高一下4月月考化学试卷2016届江西省八所重点中学盟校高三联合模拟考试理综化学试卷2016届安徽省六安市一中高三下综合训练十一理综化学试卷2016届四川省宜宾县高三第一次适应性测试理综化学试卷2015-2016学年中国石油天然气管道局中学高二下第二次月考化学试卷2016-2017学年河北正定中学高二上开学考试化学卷2017届河北省武邑中学高三上调研四化学试卷2017届辽宁省铁岭市协作体高三上联考四化学试卷2017届广东省清远市第三中学高三下学期第一次模拟考试理综化学试卷2016-2017学年江西省九江第一中学高一下学期第一次月考化学试卷2017届天津市和平区高三第二次质量调查(二模)化学试卷河北省衡水中学2017届高三下学期七调理科综合化学试题江西省九江市第一中学2016-2017学年高一下学期第一次月考化学试题云南省曲靖市2018届高三第一次复习统一检测理科综合化学试题福建省莆田第六中学2017-2018学年高一6月月考B化学试题【全国百强校】重庆市西南大学附属中学校2018届高三第六次月考(3月)理科综合化学试题四川省射洪县射洪中学2018-2019学年高二上学期开学考试化学试题云南省民族大学附属中学2019届高三上学期期中考试化学试题【全国百强校】四川省成都外国语学校2018-2019学年高一下学期3月月考化学试题(已下线)【新东方】高中化学140河南省鹤壁市高级中学2018-2019学年高一下学期第一次段考化学试题2020届高三化学知识点强化训练-元素周期表第一章物质结构元素周期律 模拟高考湖北省黄冈市黄梅县第一中学2019-2020学年高一下学期期中考试化学试题山西省晋中市平遥中学2019-2020高一下学期在线学习质量检测化学试题内蒙古赤峰二中2019-2020学年高一下学期第二次月考(6月)化学试题江苏省南京师范大学附属中学2020届高三下学期六月押题化学试题江西省南昌市八一中学2019-2020学年高一下学期期末考试化学试题湖北省应城市第一高级中学2019-2020学年高一下学期复学摸底测试化学试题(已下线)第14讲 元素周期表和元素周期律-2021年高考化学一轮复习名师精讲练苏教版(2020)高一必修第一册专题5第一单元 综合训练人教版(2019)高一必修第一册第四章 物质结构 元素周期律 高考挑战区人教版(2019)高一必修第一册 第四章 第二节综合训练鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律章末综合检测卷人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第二节 元素周期律内蒙古自治区呼伦贝尔阿荣旗第一中学2019-2020学年高一下学期期末考试化学试题专题5 第一单元 元素周期律和元素周期表 第2课时 元素周表及其应用-高中化学苏教2019版必修第一册甘肃省兰州市第五十五中学2020-2021学年高一下学期3月月考化学试题四川省成都市树德中学2020-2021学年高一下学期4月月考化学试题宁夏石嘴山市第三中学2021届高三上学期第三次月考(期末)化学试题湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期期中考试化学试题山东省菏泽市郓城县第一中学2021-2022学年高一下学期3月阶段性检测化学试题山东省青岛一中2023-2024学年高一下学期4月月考化学试卷
9 . X、Y、Z三种短周期元素,X的原子半径小于周期表中任何其他元素原子的半径,Y的最外层电子数是次外层电子数的两倍,Z的单质是空气中体积分数最大的气体。下列说法正确的是
| A.X的气体单质可以在Z的气体单质中燃烧 |
| B.Y 原子的半径大于Z原子的半径 |
| C.Y 与Z形成的化合物中,Z元素显正价 |
| D.Z与X形成的简单化合物为离子化合物 |
您最近半年使用:0次
10 . X、Y、Z为短周期元素,X的最外层电子数是Y原子最外层电子数的2倍,Y的原子序数比X的原子序数多5,Z原子的最外层电子数比Y多3。下列叙述正确的是( )
| A.原子半径的大小顺序:Z>X>Y |
| B.Z单质与X单质直接反应可生成两种化合物 |
| C.工业上,电解X和Y形成的化合物制取Y单质 |
| D.Y、Z元素的最高价氧化物的水化物不能互相反应 |
您最近半年使用:0次
2020-04-29更新
|
218次组卷
|
2卷引用:吉林省延边市长白山第一高级中学2019-2020学年高二下学期验收考试化学试卷



