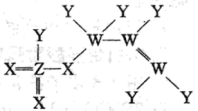
1 . 短周期主族元素W、X、Y、Z的原子序数依次增大,X、Z同主族,由四种元素形成的一种化合物的结构式如图。下列说法正确的是

| A.非金属性:X>Y>Z>W |
| B.Y、Z分别与钠元素形成的化合物均为离子化合物 |
| C.X分别与W、Y、Z形成化合物时,X的化合价相同 |
| D.图示化合物分子中的四种原子均满足8电子稳定结构 |
您最近半年使用:0次
名校
解题方法
2 . 短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B原子的最外层电子数是次外层电子数的2倍,C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)D在周期表中的位置是___ ,写出实验室制备单质F的离子方程式___ 。
(2)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:___ 。
(3)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是__ (用元素离子符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性___ 于F(填“强”或“弱”),并用化学方程式证明上述结论__ 。
II.以CA3代替氢气研发燃料电池是当前科研的一个热点。
(5)CA3燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为: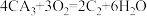 .该电池负极的电极反应式为
.该电池负极的电极反应式为___ ;每消耗3.4gCA3转移的电子数目为___ 。
(1)D在周期表中的位置是
(2)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:
(3)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是
(4)元素B和F的非金属性强弱,B的非金属性
II.以CA3代替氢气研发燃料电池是当前科研的一个热点。
(5)CA3燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:
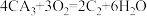 .该电池负极的电极反应式为
.该电池负极的电极反应式为
您最近半年使用:0次
2021-05-27更新
|
249次组卷
|
2卷引用:黑龙江省大庆市铁人中学2020-2021学年高一下学期期中考试化学试题
名校
3 . P(化学式为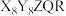 )是一种广谱的防霉抗菌缓和剂的原料,结构如下图,其中X、Y、Z、Q和R是原子序数依次增大的短周期元素,Z与Q元素可以形成原子个数比为1∶1、1∶2的两种化合物。
)是一种广谱的防霉抗菌缓和剂的原料,结构如下图,其中X、Y、Z、Q和R是原子序数依次增大的短周期元素,Z与Q元素可以形成原子个数比为1∶1、1∶2的两种化合物。
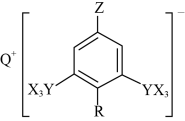
下列说法错误的是
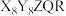 )是一种广谱的防霉抗菌缓和剂的原料,结构如下图,其中X、Y、Z、Q和R是原子序数依次增大的短周期元素,Z与Q元素可以形成原子个数比为1∶1、1∶2的两种化合物。
)是一种广谱的防霉抗菌缓和剂的原料,结构如下图,其中X、Y、Z、Q和R是原子序数依次增大的短周期元素,Z与Q元素可以形成原子个数比为1∶1、1∶2的两种化合物。
下列说法错误的是
A.Z与Q元素的简单离子半径: |
| B.Z与其他四种元素均可至少形成两种化合物 |
| C.可用X、Z或Q、Z形成的化合物制备Z的单质 |
| D.R的一种含氧酸具有较强的杀菌能力 |
您最近半年使用:0次
2021-05-21更新
|
975次组卷
|
6卷引用:黑龙江省哈尔滨市第九中学2021-2022学年高三上学期期末考试理科综合化学试题
黑龙江省哈尔滨市第九中学2021-2022学年高三上学期期末考试理科综合化学试题河南省顶尖计划2021届高三毕业班第三次考试理综化学试题(已下线)第16讲 元素周期律和元素周期表(精练)-2022年高考化学一轮复习讲练测(已下线)专题05 元素周期律-【微专题·大素养】备战2022年高考化学讲透提分要点(已下线)卷06 物质结构和元素周期律综合推断-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)2024届重庆市高三下学期二模考试化学试题
名校
4 . 某元素X最高价含氧酸的相对分子质量为98,且X的氢化物的分子式不是H2X,则下列说法正确的是
| A.X的最高价含氧酸的分子式可表示为H3XO4 |
| B.X是第二周期ⅤA族元素 |
| C.X是第二周期ⅥA族元素 |
| D.X的最高正化合价为+4 |
您最近半年使用:0次
2021-04-19更新
|
344次组卷
|
19卷引用:黑龙江省齐齐哈尔市第八中学2018-2019学年高一下学期3月月考化学试题
黑龙江省齐齐哈尔市第八中学2018-2019学年高一下学期3月月考化学试题(已下线)2012年鲁科版高中化学必修2 1.2元素周期律和元素周期表练习卷(已下线)2013-2014学年山东省济宁市嘉祥一中高一3月质检化学试卷2014-2015学年湖北省荆州市松滋四中高二下学期6月月考化学试卷河北省唐山市开滦第二中学2017-2018学年高一4月月考化学试题【全国市级联考】山东省菏泽市2017-2018学年高二下学期期中考试(B卷)化学试题【全国百强校】河北省邢台市第一中学2018-2019学年高一下学期第一次月考化学试题福建省福州市福清市华侨中学2018-2019学年高一下学期期中考试化学试题【校级联考】江西省赣州市五校协作体2018-2019学年高一下学期期中联考化学试题甘肃省武威第十八中学2018-2019学年高一下学期期中考试化学试题新疆石河子第二中学2018-2019学年高一下学期第一次月考化学试题苏教版高一化学必修2专题1《微观结构与物质的多样性》测试卷人教版高一化学必修2第一章物质结构与元素周期律单元检测试题浙江省宁波市慈溪中学高一化学《物质结构 元素周期律》单元检测(实验班)福建省漳州市第一中学2019-2020学年高一3月在线测试(实验班)化学试题新疆乌鲁木齐市第八中学2020-2021学年高一下学期第一阶段考试化学试题云南省通海县一中2020-2021学年高一下学期期中考试化学试题(已下线)5.1.4 元素周期表的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)天津市实验中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
| A.A、B简单离子半径大小关系为:B3+>A2+ |
| B.简单气态氢化物沸点:D>E |
| C.简单气态氢化物的稳定性:D<C |
| D.最高价氧化物对应的水化物的酸性:C>E |
您最近半年使用:0次
2020-12-08更新
|
301次组卷
|
3卷引用:黑龙江省大庆市东风中学2020-2021学年高一下学期开学考试化学试题
名校
6 . 黝帘石的化学式是 E2C3AD3B13, A 、B、C 、D、E 为五种不同主族的原子序数依次增大的前20 号元素; 其中A 、B 、C、E 四种位于不同周期,这五种元素原子序数和为 56,B 的最外层电子数为其电子层数的三倍。下列说法错误的是
| A.最简单氢化物的热稳定性:B>D |
| B.氯元素分别和D、B 形成的化合物均为共价化合物 |
| C.B 、C 、E 的简单离子半径:E>B>C |
| D.C 的最高价氧化物对应的水化物是强碱 |
您最近半年使用:0次
2020-11-07更新
|
123次组卷
|
2卷引用:黑龙江省绥化市海伦市第一中学2021届高三上学期12月月考化学试题
名校
解题方法
7 . 化合物甲是一种常见无机物,其结构如图所示(图中的“—”可表示单键或双键),其中W、X、Y、Z为元素周期表中的短周期主族元素,且原子序数依次增大,W和Y、X和Z分别为同主族元素,这四种元素原子的最外层电子数之和为14,甲的水溶液显酸性。下列叙述不正确的是
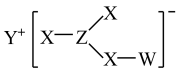
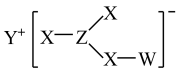
| A.W与X、W与Z均可形成18电子分子 |
| B.X、Y形成的离子化合物中可能含共价键 |
C.X、Y、Z三种元素的简单离子半径大小顺序为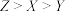 |
D.甲的水溶液中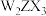 的分布分数大于 的分布分数大于 的分布分数 的分布分数 |
您最近半年使用:0次
2020-10-11更新
|
840次组卷
|
3卷引用:黑龙江省哈尔滨市第六中学2021届高三12月月考化学试题
名校
8 . X、Y、Z、R是短周期主族元素,X元素是形成有机化合物的必需元素,Y元素原子的最外层电子数是次外层的三倍,Z元素的原子半径是短周期主族元素中最大的,R原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述不正确的是( )
| A.X、R元素的非金属性:R>X |
| B.XY2是形成酸雨的主要污染物 |
| C.X、Z分别与R形成的化合物中化学键类型不同 |
| D.含有X、Y、Z三种元素的化合物的溶液可能显碱性 |
您最近半年使用:0次
2020-09-07更新
|
346次组卷
|
4卷引用:黑龙江省大庆市东风中学2020-2021学年高一下学期开学考试化学试题
解题方法
9 . A、B、C、D、E五种元素,已知:
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的最外层上的电子数比最内层多5。
②常温下B2是气体,它的相对分子质量是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F,F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第___ 周期___ 族;
(2)C的离子结构示意图是_____ ,F中的化学键为______ ;
(3)AB2的电子式为___ ; F和AB2反应的化学方程式为_______ ;
(4)C、D、E三种元素的原子半径从小到大的顺序为___ ; (用元素符号回答)
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为__________ 。
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的最外层上的电子数比最内层多5。
②常温下B2是气体,它的相对分子质量是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F,F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第
(2)C的离子结构示意图是
(3)AB2的电子式为
(4)C、D、E三种元素的原子半径从小到大的顺序为
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为
您最近半年使用:0次
名校
10 . 下图为某漂白剂的结构。已知:W、Y、Z是不同周期、不同主族的短周期元素,W、Y、Z原子最外层电子数之和等于X原子最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述错误的是
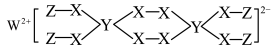
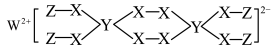
| A.W、X对应的简单离子的半径:X>W |
| B.Y元素在周期表中的位置为二周期第IVA族 |
| C.将W的氯化物的水溶液加热蒸干并灼烧可得到W的氧化物 |
| D.该漂白剂结构中,Y、X原子的最外层均满足8电子结构。 |
您最近半年使用:0次
2020-05-04更新
|
566次组卷
|
6卷引用:黑龙江省哈尔滨市第三中学校2021-2022学年高三上学期期中考试化学试题
黑龙江省哈尔滨市第三中学校2021-2022学年高三上学期期中考试化学试题四川省南充高级中学2020届高三下学期4月月考理综化学试题浙江省杭州高级中学2021届高三上学期期中考试化学试题(已下线)【浙江新东方】116(已下线)【浙江新东方】高中化学20210513-042【2021】【高二下】四川省遂宁中学校2019-2020学年高二下学期第二次月考化学试题



