1 . 通过复习总结,下列归纳正确的是
| A.简单非金属阴离子只有还原性,而金属阳离子一定只有氧化性 |
B.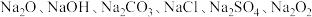 都属于钠的含氧化合物 都属于钠的含氧化合物 |
C.日本福岛核电站爆炸时释放的两种放射性同位素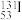 与 与 的中子数相等 的中子数相等 |
D.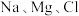 是海水中的重要元素,从海水中制备这三种元素单质的反应都是氧化还原反应 是海水中的重要元素,从海水中制备这三种元素单质的反应都是氧化还原反应 |
您最近一年使用:0次
解题方法
2 . 硒(34Se)是人和动物体中一种必需的微量元素,存在于地球所有环境介质中,其同位素可有效示踪硒生物地球化学循环过程及其来源,下列说法不正确 的是
| A.Se位于周期表中第四周期第VIA族 |
| B.可用质谱法区分Se的两种同位素78Se和80Se |
| C.第一电离能:34Se>33As |
| D.SeO2既具有氧化性又具有还原性 |
您最近一年使用:0次
名校
3 . 硒(Se)和铬(Cr)元素都是人体必需的微量元素,请回答下列问题:
(1)硒与氧为同主族元素,属于第四周期元素,画出硒的原子结构示意图为______________ ;
(2)已知核内有48个中子的硒的同位素,下列表示该核素的符号正确的是________
(3)由硒在周期表中的位置分析判断下列说法正确的是________
(4)二硫化硒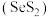 具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。
具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。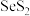 中硫元素的化合价为负价,请从元素周期律角度解释原因:
中硫元素的化合价为负价,请从元素周期律角度解释原因:_________________ 。
(5)人体内产生的活性氧能加速人体衰老,被称为“生命杀手”,化学家尝试用 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出____________ 性。
(1)硒与氧为同主族元素,属于第四周期元素,画出硒的原子结构示意图为
(2)已知核内有48个中子的硒的同位素,下列表示该核素的符号正确的是________
A.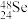 | B. | C.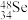 | D.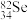 |
A.热稳定性: | B.还原性: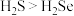 |
C.酸性: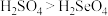 | D.原子半径: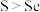 |
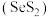 具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。
具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。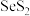 中硫元素的化合价为负价,请从元素周期律角度解释原因:
中硫元素的化合价为负价,请从元素周期律角度解释原因:(5)人体内产生的活性氧能加速人体衰老,被称为“生命杀手”,化学家尝试用
 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出
您最近一年使用:0次
名校
4 . 含氮化合物( 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。
Ⅰ.苯酚( )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在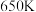 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。
(1)已知



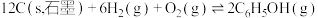
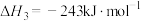
则

___________ 。
Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
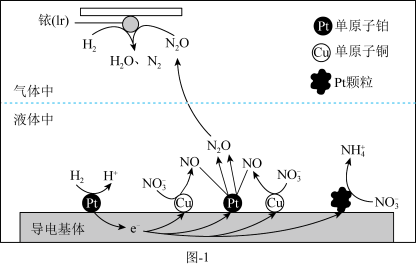
(2) 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,___________ 。
(3)若导电基体上的Pt颗粒增多,造成的后果是___________ 。
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有___________ 。
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。

(5)该装置可以生成大量氧化性更强的 ,
, 去除
去除 的离子方程式为
的离子方程式为___________ 。
(6)相比于传统的二维电极反应系统,三维电极的优点有___________ 。
 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。Ⅰ.苯酚(
 )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在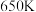 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。(1)已知




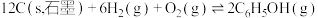
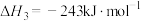
则


Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的
 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
(2)
 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,(3)若导电基体上的Pt颗粒增多,造成的后果是
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的
 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。
(5)该装置可以生成大量氧化性更强的
 ,
, 去除
去除 的离子方程式为
的离子方程式为(6)相比于传统的二维电极反应系统,三维电极的优点有
您最近一年使用:0次
5 . 将“84”消毒液和洁厕灵同时使用会发生反应: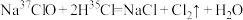 。下列有关说法中正确的是
。下列有关说法中正确的是
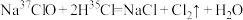 。下列有关说法中正确的是
。下列有关说法中正确的是A.该反应生成 的摩尔质量为 的摩尔质量为 |
B. 和 和 所含中子数之比为35∶37 所含中子数之比为35∶37 |
C.该反应中,体现了 的酸性和氧化性 的酸性和氧化性 |
| D.该反应涉及的物质中有4种物质含共价键 |
您最近一年使用:0次
名校
解题方法
6 . 碘(I)在元素周期表中位于ⅦA族,是人体必需的微量元素之一。
(1) 可用于治疗甲亢。
可用于治疗甲亢。 的原子核内中子数为
的原子核内中子数为___________ 。
(2)①碘元素的非金属性比氯元素的弱,其原因是由于同主族元素从上到下原子核外电子层数依次增多,___________ 逐渐增大,___________ 能力逐渐减弱。
②下列事实能够用“碘的非金属性比氯的弱”来解释的是___________ (填序号)。
a.碘单质的熔点高于氯单质
b.高氯酸的酸性强于高碘酸
c. 与
与 的化合比
的化合比 与
与 的化合更容易
的化合更容易
(3)氢碘酸是HI的水溶液,是一种酸性比盐酸强的酸。
资料:ⅰ.盐酸和氢碘酸均可使氢氧化铁溶解,后者得到的产物中含有 。
。
ⅱ.KI溶液不能溶解氢氧化铁,KI溶液与 溶液反应的产物中含有
溶液反应的产物中含有 。
。
①盐酸与氢氧化铁发生反应的离子方程式是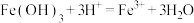 ;氢碘酸与氢氧化铁发生反应的离子方程式是
;氢碘酸与氢氧化铁发生反应的离子方程式是___________ 。
②结合上述资料,由物质性质解释①中两反应的异同:___________ 。
(1)
 可用于治疗甲亢。
可用于治疗甲亢。 的原子核内中子数为
的原子核内中子数为(2)①碘元素的非金属性比氯元素的弱,其原因是由于同主族元素从上到下原子核外电子层数依次增多,
②下列事实能够用“碘的非金属性比氯的弱”来解释的是
a.碘单质的熔点高于氯单质
b.高氯酸的酸性强于高碘酸
c.
 与
与 的化合比
的化合比 与
与 的化合更容易
的化合更容易(3)氢碘酸是HI的水溶液,是一种酸性比盐酸强的酸。
资料:ⅰ.盐酸和氢碘酸均可使氢氧化铁溶解,后者得到的产物中含有
 。
。ⅱ.KI溶液不能溶解氢氧化铁,KI溶液与
 溶液反应的产物中含有
溶液反应的产物中含有 。
。①盐酸与氢氧化铁发生反应的离子方程式是
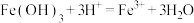 ;氢碘酸与氢氧化铁发生反应的离子方程式是
;氢碘酸与氢氧化铁发生反应的离子方程式是②结合上述资料,由物质性质解释①中两反应的异同:
您最近一年使用:0次
2023-01-05更新
|
300次组卷
|
2卷引用:北京市东城区2022-2023学年高一上学期期末统一检测化学试卷
名校
解题方法
7 . 2022年诺贝尔化学奖授予对点击化学和生物正交化学做出贡献的三位科学家。我国科学家合成一种点击化学试剂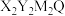 ,X分别与Y、Z、M形成原子个数为3、6、4的
,X分别与Y、Z、M形成原子个数为3、6、4的 分子,
分子,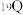 衰变方程:
衰变方程: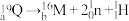 。下列说法错误的是
。下列说法错误的是
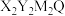 ,X分别与Y、Z、M形成原子个数为3、6、4的
,X分别与Y、Z、M形成原子个数为3、6、4的 分子,
分子,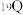 衰变方程:
衰变方程: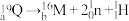 。下列说法错误的是
。下列说法错误的是| A.Q2与XQ均为无色气体 | B.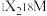 与 与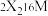 的相对分子质量相同 的相对分子质量相同 |
| C.同一周期中,Z的最高价含氧酸酸性最强 | D.Y、M形成简单氢化物的还原性:Y>M |
您最近一年使用:0次
2023-04-27更新
|
603次组卷
|
5卷引用:山东省德州市2022-2023学年高一下学期4月期中考试化学试题
山东省德州市2022-2023学年高一下学期4月期中考试化学试题(已下线)押题密卷 02-【热题狂飙】2023年高考化学样卷(全国卷专用)(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练湖北省武汉市第二中学2023-2024学年高三上学期10月月考化学试题2023届江西省南昌市第十九中学高三下学期第四次模拟考试理科综合试卷-高中化学
解题方法
8 . 卢瑟福发现质子的核反应原理为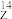 X+
X+ He→
He→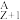 Y+1H。其中Y元素的一种同素异形体可吸收紫外线。下列说法错误的是
Y+1H。其中Y元素的一种同素异形体可吸收紫外线。下列说法错误的是
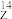 X+
X+ He→
He→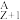 Y+1H。其中Y元素的一种同素异形体可吸收紫外线。下列说法错误的是
Y+1H。其中Y元素的一种同素异形体可吸收紫外线。下列说法错误的是A.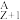 Y的中子数为9 Y的中子数为9 |
| B.X的最高价含氧酸的浓溶液具有强氧化性 |
| C.相同条件下气体密度:Y2>X2 |
| D.X、Y的单质均为非极性分子 |
您最近一年使用:0次
9 . 元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法错误的是
| A.由水溶液的酸性:HClO4>H2SO4,可推断出元素的非金属性:Cl>S |
| B.元素原子的得电子能力越强,其对应气态氢化物水溶液的酸性越强 |
| C.若aX2+和bY-的核外电子层结构相同,则原子序数:a=b+3 |
| D.根据P和As在元素周期表中的位置,可推断气态氢化物的还原性:PH3<AsH3 |
您最近一年使用:0次
2022-05-13更新
|
249次组卷
|
3卷引用:山东省高密市第三中学2022-2023学年高一下学期3月月考化学试题
山东省高密市第三中学2022-2023学年高一下学期3月月考化学试题山东省潍坊安丘市、高密市、诸城市2021-2022学年高一下学期期中考试化学试题(已下线)北京市海淀区2023届高三上学期期末考试变式汇编(1-7)
名校
解题方法
10 . Ⅰ.根据所学知识,完成下列问题
(1)元素周期表的主要发现者是谁?_______
(2)关于俄罗斯科学家找到的第119号元素,下列说法正确的是_______
(3)格致中学前身格致书院的创始人之一徐寿把化学元素译成汉字,作为这个元素的汉字名称。Ts是第117号元素的缩写,汉字名称为“石田”,其中对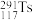 中数字的叙述正确的是_______
中数字的叙述正确的是_______
Ⅱ.下表是元素周期表的一部分,表中的每个编号表示一种元素。根据下表回答题:
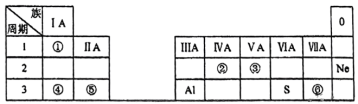
(4)元素⑥在元素周期表中的位置是___________ ,其最高价氧化物的水化物酸性与 的酸性相比,
的酸性相比,___________ (填写化学式)更强。
(5)元素②的原子结构示意图是___________ 。
(6)元素③最简单氢化物的电子式是___________ 。
(7)比较④和⑤两种元素的金属性:④___________ ⑤(选填“<”或“>”),以下能够用于判断④和⑤金属性强弱关系的依据是___________ 。
A.相同条件下,比较两者与水反应的难易程度 B.比较两者的电子层数
C.比较两者的气态氢化物稳定性 D.比较两者最高价氧化物水化物碱性
(1)元素周期表的主要发现者是谁?_______
| A.道尔顿 | B.门捷列夫 | C.阿伏伽德罗 | D.凯库勒 |
| A.该元素原子的质量数为119 | B.119号元素的原子一定含119个中子 |
| C.该元素的原子量可能为119 | D.119号元素应在周期表第ⅠA族 |
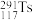 中数字的叙述正确的是_______
中数字的叙述正确的是_______| A.291是Ts元素的相对原子质量 | B.291是Ts元素的质量数 |
C.117是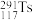 的质子数 的质子数 | D.117是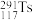 的中子数 的中子数 |
Ⅱ.下表是元素周期表的一部分,表中的每个编号表示一种元素。根据下表回答题:

(4)元素⑥在元素周期表中的位置是
 的酸性相比,
的酸性相比,(5)元素②的原子结构示意图是
(6)元素③最简单氢化物的电子式是
(7)比较④和⑤两种元素的金属性:④
A.相同条件下,比较两者与水反应的难易程度 B.比较两者的电子层数
C.比较两者的气态氢化物稳定性 D.比较两者最高价氧化物水化物碱性
您最近一年使用:0次



