1 . 下列各物质的晶体中,化学键类型完全相同,晶体类型也相同的是
| A.SiF4与SiC | B.HCOOCH3与NH4NO3 |
| C.CaO与Na2O2 | D.NF3与CS2 |
您最近一年使用:0次
名校
2 . 表中相关物质的信息都正确的一项是
| 选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
| A |  | 离子键、共价键 | 强氧化性 | 消毒液 |
| B |  | 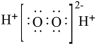 | 不稳定,易分解 | 医用消毒剂 |
| C | W(钨) | 金属键 | 银白色,具有金属光泽 | 制成灯丝 |
| D |  | 离子键 | 受热易分解 | 治疗胃酸过多 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X和Z位于同一主族,Y的原子半径是短周期元素中最大的,由X、Y、Z三种元素形成的化合物M结构如图所示。下列叙述错误的是


| A.离子半径:Z>W>X>Y |
| B.化合物M、WX2、ZX2、YWX均为漂白剂,四者漂白原理相同 |
| C.在化合物M中,存在极性共价键、非极性共价键、配位键和离子键 |
| D.由X、Y、Z形成的化合物的水溶液可能呈碱性 |
您最近一年使用:0次
名校
解题方法
4 . 明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载,锌是生命体必需的微量元素,被称为“生命之花”。
(1)基态Zn原子核外的最高能层符号是___________ 。
(2)乳酸锌(如图)是一种很好的食品锌强化剂,其中存在的作用力有___________ (填编号),乳酸锌中C原子的杂化方式有___________ 。
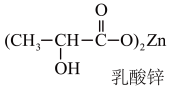
A离子键 B.极性共价键 C.金属键 D.配位键 E.范德华力
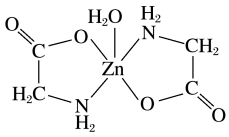
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是___________ , 的配位数为
的配位数为___________ ;甘氨酸易溶于水,试从结构角度解释___________ 。
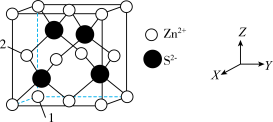
(4)Zn与S形成某种化合物的晶胞如图所示。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为___________ 。
②已知晶胞参数为apm,阿伏伽德罗常数为 ,求该晶胞的密度
,求该晶胞的密度
___________  (写计算表达式)。
(写计算表达式)。
(1)基态Zn原子核外的最高能层符号是
(2)乳酸锌(如图)是一种很好的食品锌强化剂,其中存在的作用力有

A离子键 B.极性共价键 C.金属键 D.配位键 E.范德华力
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是
 的配位数为
的配位数为
(4)Zn与S形成某种化合物的晶胞如图所示。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为
②已知晶胞参数为apm,阿伏伽德罗常数为
 ,求该晶胞的密度
,求该晶胞的密度
 (写计算表达式)。
(写计算表达式)。
您最近一年使用:0次
名校
解题方法
5 . 下列说法中,正确的一组是
①两种元素组成的共价化合物的分子中的化学键都是极性键
②两种不同非金属元素的原子之间形成的化学键都是极性键
③2p能级上有两个未成对电子的简单氢化物属于非极性分子
④氯化铵和五水硫酸铜都属于配合物
⑤离子化合物中一定含有离子键
⑥分子内可能没有共价键
⑦非金属单质都是非极性分子
⑧σ键和π键可以都单独存在
①两种元素组成的共价化合物的分子中的化学键都是极性键
②两种不同非金属元素的原子之间形成的化学键都是极性键
③2p能级上有两个未成对电子的简单氢化物属于非极性分子
④氯化铵和五水硫酸铜都属于配合物
⑤离子化合物中一定含有离子键
⑥分子内可能没有共价键
⑦非金属单质都是非极性分子
⑧σ键和π键可以都单独存在
| A.②⑤⑥⑦ | B.②⑤⑥ | C.①②③⑤⑥⑧ | D.②③⑤⑥⑦ |
您最近一年使用:0次
名校
6 . 下列过程中化学键被破坏的是
①碘升华②溴蒸气被木炭吸附③酒精溶于水④HCl气体溶于水⑤MgCl2溶解于水
①碘升华②溴蒸气被木炭吸附③酒精溶于水④HCl气体溶于水⑤MgCl2溶解于水
| A.全部 | B.②③④⑤ | C.④⑤ | D.⑤ |
您最近一年使用:0次
名校
7 . 已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是宇宙中含量最丰富的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法不正确的是
| A.Y的最高价氧化物对应的水化物是弱酸 |
| B.最简单氢化物的热稳定性:R>W |
| C.R与X形成的化合物同W与Z形成的化合物的化学键类型完全相同 |
| D.原子半径:Z>W>R |
您最近一年使用:0次
名校
8 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W是元素周期表中原子半径最小的元素,Z的最外层电子数是W和X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述错误的是
| A.原子半径:Y>Z>X>W |
| B.Y的氧化物为酸性氧化物,溶于氨水 |
| C.W、X和Z可形成既含有离子键又含有共价键的化合物 |
| D.W与X的二元化合物可以使湿润的红色石蕊试纸变蓝 |
您最近一年使用:0次
名校
解题方法
9 . 配合物Na2[Fe(CN)5(NO)]可用于离子检验,下列说法不正确的是
| A.此配合物中存在离子键、配位键、极性键 |
| B.配离子为[Fe(CN)5(NO)]2-,中心离子为Fe3+,配位数为6 |
| C.1mol 配合物中σ键数目为10NA |
| D.该配合物为离子化合物,易电离,1mol 配合物电离共得到3 NA阴、阳离子 |
您最近一年使用:0次
2021-12-10更新
|
761次组卷
|
4卷引用:四川省绵阳南山中学2021-2022学年高二上学期12月月考化学试题
四川省绵阳南山中学2021-2022学年高二上学期12月月考化学试题(已下线)第3.4讲 配合物与超分子-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)广东省东莞市东华高级中学2021-2022学年高二下学期月考化学试题新疆乌鲁木齐市第八中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
10 . 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程: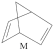
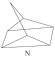 ΔH=+88.6 kJ/mol ,则M、N相比,较稳定的是
ΔH=+88.6 kJ/mol ,则M、N相比,较稳定的是___________ 。
(2)已知CH3OH(1)的燃烧热为-726.5 kJ ·mol-1,CH3OH(1)+ O2(g)=CO2(g)+ 2H2O(g) ΔH=-a kJ·mol-1,则a
O2(g)=CO2(g)+ 2H2O(g) ΔH=-a kJ·mol-1,则a___________ 726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应生成1 mol CO2时的热化学方程式:___________ 。
(4)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于___________ 晶体,CO与N2属于等电子体,则CO的结构式为___________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程:

 ΔH=+88.6 kJ/mol ,则M、N相比,较稳定的是
ΔH=+88.6 kJ/mol ,则M、N相比,较稳定的是(2)已知CH3OH(1)的燃烧热为-726.5 kJ ·mol-1,CH3OH(1)+
 O2(g)=CO2(g)+ 2H2O(g) ΔH=-a kJ·mol-1,则a
O2(g)=CO2(g)+ 2H2O(g) ΔH=-a kJ·mol-1,则a(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应生成1 mol CO2时的热化学方程式:
(4)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于
您最近一年使用:0次



