名校
1 . 已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是宇宙中含量最丰富的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法不正确的是
| A.Y的最高价氧化物对应的水化物是弱酸 |
| B.最简单氢化物的热稳定性:R>W |
| C.R与X形成的化合物同W与Z形成的化合物的化学键类型完全相同 |
| D.原子半径:Z>W>R |
您最近一年使用:0次
2 . 一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大且总和为24。下列有关叙述错误的是


| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质既能与苯酚反应,也可与甲醇反应 |
| C.W与Y既可以形成分子晶体,也可以形成离子晶体 |
| D.X的氟化物中原子均为8电子稳定结构 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法中正确的是
| A.金属晶体由金属阳离子和自由电子构成,它们都位于晶胞的一定位置上 |
| B.范德华力实质上是一种静电作用,所以范德华力是一种特殊的化学键 |
| C.配位键属于共价键,氢键不属于化学键 |
| D.共价晶体中只存在非极性共价键 |
您最近一年使用:0次
2023·山东聊城·三模
4 . 某平面形分子常用于感光复印纸的生产,其结构如图所示,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,且仅X、Y位于同一周期;Z原子的核外电子数是其次外层电子数的2倍。下列说法正确的是


A.原子半径: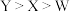 | B.元素 的含氧酸是强酸 的含氧酸是强酸 |
C.该分子中 、 、 原子的杂化类型均为 原子的杂化类型均为 | D. 、 、 、 、 形成的化合物不会含有离子键 形成的化合物不会含有离子键 |
您最近一年使用:0次
5 . 下列各组物质中,化学键类型完全相同,晶体类型也相同的是
A. 和 和 | B. 和 和 |
C. 和 和 | D.晶体硅和 |
您最近一年使用:0次
名校
解题方法
6 . 向由0.1 mol CrCl3·6H2O配成的溶液中加入足量AgNO3溶液,产生0.2 mol沉淀。配合物CrCl3·6H2O的配位数为6,下列说法错误的是
| A.该配合物的中心离子是Cr3+ |
| B.该配合物的配体是H2O和Cl− |
| C.每1 mol配离子[Cr(H2O)5Cl]2+中含有6NA个共价键 |
| D.该配合物中存在的化学键有:共价键、配位键、离子键 |
您最近一年使用:0次
7 . 国家速滑馆的建设应用了智慧建造技术,减少使用钢材。采用非常环保的二氧化碳跨临界直接制冰技术,通过压力变化使二氧化碳汽化实现制冷。下列说法中不正确的是


| A.钢材属于金属材料 |
| B.CO2分子含有非极性共价键 |
| C.二氧化碳跨临界直接制冰技术利用了其物理性质 |
| D.应用二氧化碳跨临界直接制冰技术符合“绿色奥运”理念 |
您最近一年使用:0次
2023-05-02更新
|
77次组卷
|
2卷引用:甘肃省兰州市教育局第四片区2022-2023学年高二下学期期末考试化学试题
名校
8 . 研究物质的结构,用来探寻物质的性质,是我们学习化学的重要方法。回答下列问题:
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为___________ 。
(2)氰酸铵( )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式___________ 。
(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因___________ 。

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是___________ 。(已知电负性:H-2.1 Be-1.5 B -2.0 N-3.0 O-3.5 Al-1.5 Si-1.8)
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石( )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。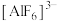 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是___________ 个。
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为
(2)氰酸铵(
 )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石(
 )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。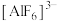 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
您最近一年使用:0次
9 .  与丁二酮肟反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验
与丁二酮肟反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验 。
。
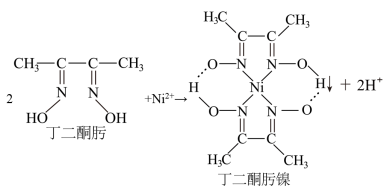
下列说法正确的是
 与丁二酮肟反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验
与丁二酮肟反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验 。
。
下列说法正确的是
A. 的配位数为4 的配位数为4 |
B.基态 的核外电子排布式为 的核外电子排布式为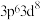 |
| C.由丁二酮肟生成丁二酮肟镍的过程中镍的化合价升高 |
| D.丁二酮肟镍分子内存在的化学键有离子键、配位键、共价键和氢键 |
您最近一年使用:0次
名校
解题方法
10 . X、Y、Z、W、E均为短周期主族元素,原子序数依次增大,且E与其他元素均不在同一周期。这五种元素组成的一种化合物的结构如图所示。下列说法不正确的是
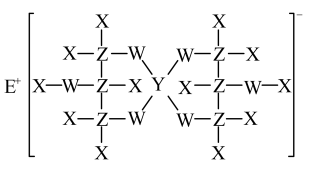

| A.W和E形成的化合物中可能存在共价键 |
| B.第一电离能:W>Z>Y |
| C.沸点:EX>X2W>ZX4 |
| D.Y的氟化物YF3中所有原子均为8电子稳定结构 |
您最近一年使用:0次
2023-04-28更新
|
801次组卷
|
3卷引用:安徽省合肥市庐江县2022-2023学年高二下学期7月期末考试化学试题



