1 . 按要求回答问题。
(1)1 mol HCHO分子中含有σ键的数目为___________ NA。
(2)CS2分子中,共价键的类型有___________ 。
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是___________ (填序号,下同),只存在非极性键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在极性共价键的是___________ ,既存在离子键又存在非极性共价键的是___________ 。
(4)第一电离能比较Mg___________ Al,解释原因___________ 。
(1)1 mol HCHO分子中含有σ键的数目为
(2)CS2分子中,共价键的类型有
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是
(4)第一电离能比较Mg
您最近一年使用:0次
名校
2 . 多酚氧化酶是自然界中分布极广的一种金属蛋白酶,与植物的抗病性有关。配合物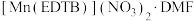 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。___________ 组峰,上述反应的反应类型为___________ ; 是碱性官能团,从结构角度解释原因:
是碱性官能团,从结构角度解释原因:___________ 。
(2)已知EDTA的相对分子质量为292,熔点为250℃,烃 (无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是
(无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是___________ 。
(3)图中有机物在镍催化及加热条件下,不能与 反应的是
反应的是___________ 。EDTA中存在的化学键有___________ (填字母)。
A.离子键 B. 键 C.非极性键 D.氢键
键 C.非极性键 D.氢键
(4)EDTB中氮原子的杂化类型是___________ ,X的VSEPR模型名称是___________ 。
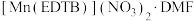 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。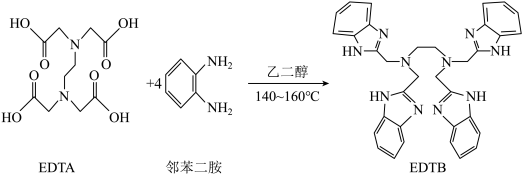 +8X
+8X
 是碱性官能团,从结构角度解释原因:
是碱性官能团,从结构角度解释原因:(2)已知EDTA的相对分子质量为292,熔点为250℃,烃
 (无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是
(无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是(3)图中有机物在镍催化及加热条件下,不能与
 反应的是
反应的是A.离子键 B.
 键 C.非极性键 D.氢键
键 C.非极性键 D.氢键(4)EDTB中氮原子的杂化类型是
您最近一年使用:0次
名校
3 . 以下是中学化学中熟悉的物质:①NH4NO3 ②Cl2 ③HCl ④Na2O2 ⑤MgCl2 ⑥CO2 ⑦AlCl3,请回答下列问题:
(1)只含离子键的是_______ 。
(2)含极性键的离子化合物是_______ 。
(3)由极性键构成的非极性分子的是_______ 。
(4)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是上述中的______ (填序号),用化学方程式来表示吸收原理:_______ 。
(5)羰基硫(COS)与CO2的结构相似,羰基硫(COS)分子的结构式为_______ 。
(6)NH4NO3中 的空间构型为
的空间构型为_______ 。
(1)只含离子键的是
(2)含极性键的离子化合物是
(3)由极性键构成的非极性分子的是
(4)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是上述中的
(5)羰基硫(COS)与CO2的结构相似,羰基硫(COS)分子的结构式为
(6)NH4NO3中
 的空间构型为
的空间构型为
您最近一年使用:0次
4 .  能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(1)向 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。
①画出配离子 中的配位键
中的配位键_______________ 。
② 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有_____________ (填序号)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2) 可以与乙二胺
可以与乙二胺 形成配离子:
形成配离子:_____________________ 。
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(1)向
 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。①画出配离子
 中的配位键
中的配位键②
 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)
 可以与乙二胺
可以与乙二胺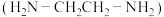 形成配离子:
形成配离子: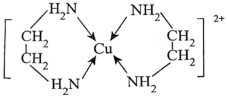
您最近一年使用:0次
5 . 完成下列问题
(1)氨气极易溶于水,原因是___________
(2) 的VSEPR理想模型名称为
的VSEPR理想模型名称为___________ ,离子空间结构名称为___________ ,中心原子有___________ 个杂化轨道;
(3) 中存在的化学键类型有
中存在的化学键类型有___________
①离子键 ②极性共价键 ③非极性共价键 ④氢键
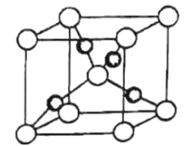
(4)一个 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为___________ 。
(1)氨气极易溶于水,原因是
(2)
 的VSEPR理想模型名称为
的VSEPR理想模型名称为(3)
 中存在的化学键类型有
中存在的化学键类型有①离子键 ②极性共价键 ③非极性共价键 ④氢键
(4)一个
 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为
您最近一年使用:0次
6 . Ⅰ.食品添加剂能改善食物色香味、延长保质期、调整营养结构。我国对食品添加剂的品种、适用范围、最大用量及残留量都制定了严格的标准。
(1)下列关天食品添加剂的说法正确的是________ 。
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为________ 。
(3)与SO2所含化学键类型相同的是________。
(4)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是________(双选)。
(5)保鲜时若SO2不慎用量过大,会使水果表面明显褪色,上述现象说明SO2________ 。
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。
已知:ω(SO2残留量) =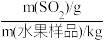 。
。
(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标______ (写出计算过程)。
(1)下列关天食品添加剂的说法正确的是
A制作豆腐时,加入石膏做凝固剂
B.制作糕点时,加入小苏打做防腐剂
C.生产加碘食盐时,加入碘单质作补碘剂
Ⅱ.SO2是葡萄、荔枝等水果储存时常用的保鲜剂,能降低水果腐烂率,提高维生素C留存率。
(2)硫原子的结构示意图为
(3)与SO2所含化学键类型相同的是________。
| A.NH4Cl | B.CaCl2 | C.AlCl3 | D.NaOH |
| A.热稳定性:H2S>SiH4 | B.溶解度:SO2> SiO2 |
| C.单质的熔点:Si > S | D.酸性:H2SO4> H2SiO3 |
A.易溶于水B.是酸性氧化物C.具有漂白作用
Ⅲ.《食品安全国家标准·食品添加剂使用标准》(GB 2760-2014)中规定,水果中SO2残留量不得高于0.05g/kg。某种测定水果中残留SO2的方法所涉及的主要反应有:SO2+ H2O2=H2SO4、
 +Ba2+=BaSO4↓。
+Ba2+=BaSO4↓。已知:ω(SO2残留量) =
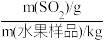 。
。(6)称取某水果样品2 kg,经过一系列处理后,最终得到BaSO4,沉淀的质量为0.233 g。通过计算,判断该水果样品中SO2残留量是否超标
您最近一年使用:0次
7 . 所有的分子中都存在化学键。( )
您最近一年使用:0次
解题方法
8 . 判断化学键的类型。
(1)一般来说,如果两种成键元素的电负性差值大于1.7,它们之间通常形成__________ 。
(2)一般来说,如果两种成键元素的电负性差值小于1.7,它们之间通常形成__________ 。
(1)一般来说,如果两种成键元素的电负性差值大于1.7,它们之间通常形成
(2)一般来说,如果两种成键元素的电负性差值小于1.7,它们之间通常形成
您最近一年使用:0次
名校
9 . 研究物质的结构,用来探寻物质的性质,是我们学习化学的重要方法。回答下列问题:
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为___________ 。
(2)氰酸铵( )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式___________ 。
(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因___________ 。

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是___________ 。(已知电负性:H-2.1 Be-1.5 B -2.0 N-3.0 O-3.5 Al-1.5 Si-1.8)
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石( )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。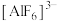 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是___________ 个。
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为
(2)氰酸铵(
 )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石(
 )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。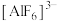 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
您最近一年使用:0次
名校
解题方法
10 . 按要求完成下列填空:
Cu2+能与NH3、H2O、OH-、Cl-等形成配位数为4的配合物
(1)向CuSO4溶液中加入过量NaOH溶液可生成 。
。
①画出配离子 的结构:
的结构:_______ 。
②写出该过程生成 的化学方程式
的化学方程式_______ 。
③ 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有_______ 。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)Cu2+可以与乙二胺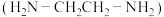 形成配离子(如图):
形成配离子(如图):
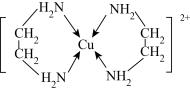
①乙二胺分子中N原子成键时采取的杂化类型是_______ 。
②乙二胺沸点高于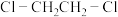 的主要原因是
的主要原因是_______ 。
Cu2+能与NH3、H2O、OH-、Cl-等形成配位数为4的配合物
(1)向CuSO4溶液中加入过量NaOH溶液可生成
 。
。①画出配离子
 的结构:
的结构:②写出该过程生成
 的化学方程式
的化学方程式③
 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)Cu2+可以与乙二胺
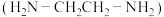 形成配离子(如图):
形成配离子(如图):
①乙二胺分子中N原子成键时采取的杂化类型是
②乙二胺沸点高于
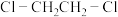 的主要原因是
的主要原因是
您最近一年使用:0次
2023-04-27更新
|
256次组卷
|
3卷引用:吉林省长春市第十七中学2022-2023学年高二下学期4月月考化学试题



