名校
1 . 检验微量砷的原理为 。AsH3常温下为无色气体。下列说法正确的是
。AsH3常温下为无色气体。下列说法正确的是
 。AsH3常温下为无色气体。下列说法正确的是
。AsH3常温下为无色气体。下列说法正确的是| A.As的基态核外电子排布式为[Ar]4s24p3 | B.H2O的VSEPR空间构型为V型 |
| C.固态AsH3属于共价晶体 | D.AgNO3中含有离子键和极性键 |
您最近一年使用:0次
名校
解题方法
2 . 甲酸在纳米级磁性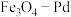 表面分解为活性
表面分解为活性 和
和 ,经下列历程实现
,经下列历程实现 方的催化还原,从而减少污染。已知:分子中的大
方的催化还原,从而减少污染。已知:分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )。下列说法错误的是
)。下列说法错误的是
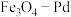 表面分解为活性
表面分解为活性 和
和 ,经下列历程实现
,经下列历程实现 方的催化还原,从而减少污染。已知:分子中的大
方的催化还原,从而减少污染。已知:分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )。下列说法错误的是
)。下列说法错误的是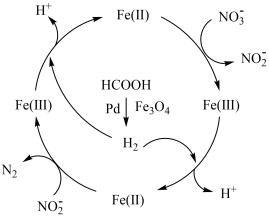
A.纳米级磁性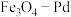 可以降低甲酸分解反应的活化能 可以降低甲酸分解反应的活化能 |
B.反应中 转化为 转化为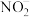 大 大 键的变化表示为 键的变化表示为 |
C.反应历程中生成的 可调节体系 可调节体系 ,有增强 ,有增强 氧化性的作用 氧化性的作用 |
D.总反应方程式为 |
您最近一年使用:0次
解题方法
3 . 蛋氨酸铜的结构式如图。
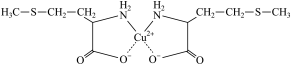
| A.配位键 | B.氢键 | C.离子键 | D.金属键 |
您最近一年使用:0次
解题方法
4 . 部分含钠或硫的“价类二维图”如下图所示。下列推断合理的是

| A.b、c均具有还原性 | B.d、g、h中均存在共价键 |
| C.a可与氧气一步生成d或e | D.f一定可用做膨松剂 |
您最近一年使用:0次
解题方法
5 . 能引起痛风的某有机物的结构如图所示,其中短周期元素Q、X、Y、Z、M的原子序数依次增大,Q、M同主族,X、Y、Z三种元素位于同一周期相邻主族。下列说法正确的是
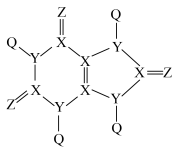
| A.Y的基态原子有3个单电子 | B.简单离子半径: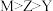 |
C.元素的电负性: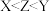 | D.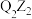 与 与 中的化学键类型相同 中的化学键类型相同 |
您最近一年使用:0次
名校
6 . 很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物II,化合物Ⅲ也是一种汞解毒剂。化合物IV是一种强酸。下列说法不正确的是
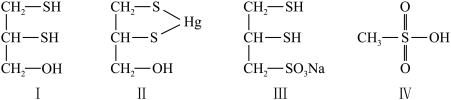
| A.在I中S原子采取sp3杂化 | B.在II中S元素的电负性最大 |
| C.在III中存在离子键与共价键 | D.在IV中硫氧键的键能均相等 |
您最近一年使用:0次
7 . W、X、Y、Z为族序数依次增大的前四周期主族元素,Y、Z、X、W的原子序数依次增大,它们分别能形成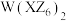 、
、 等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是
等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是
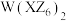 、
、 等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是
等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是A.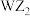 含有共价键 含有共价键 | B.原子半径:W>Z>Y>X |
| C.最简单氢化物的沸点:Y>Z>X | D.X元素最高价氧化物对应的水化物为强酸 |
您最近一年使用:0次
名校
解题方法
8 . 孔雀石是一种碳酸盐矿物,主要成分为Cu2(OH)2CO3,其形成过程的主要化学方程式为2CuSO4+2CaCO3+H2O= Cu2(OH)2CO3+2CaSO4+CO2↑。NA是阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol/L的CuSO4溶液中所含Cu2+的数目小于0.1NA |
| B.常温常压下,18gH2O中所含共用电子对的数目为2NA |
C.1molCaCO3晶体中所含 的数目小于NA 的数目小于NA |
| D.44gCO2溶于水所得溶液中所含H2CO3分子的数目为NA |
您最近一年使用:0次
9 . 化学助力蓝天保卫战。工业上可利用氨水吸收SO2尾气,生成NH4HSO3,再将其氧化得到(NH4)2SO4化肥。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4LNH3所含的分子数目为NA |
| B.64gSO2中所含的σ键数目为2NA |
C.2mol 完全氧化生成 完全氧化生成 ,转移的电子数目为2NA ,转移的电子数目为2NA |
D.1L0.1mol/L(NH4)2SO4溶液中所含的 数目为0.2NA 数目为0.2NA |
您最近一年使用:0次
名校
解题方法
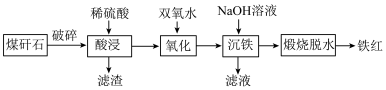
10 . 由煤矸石(主要成分为 及铁铝的氧化物,还含有少量
及铁铝的氧化物,还含有少量 )制备铁红的工艺流程如图,下列说法错误的是
)制备铁红的工艺流程如图,下列说法错误的是
 及铁铝的氧化物,还含有少量
及铁铝的氧化物,还含有少量 )制备铁红的工艺流程如图,下列说法错误的是
)制备铁红的工艺流程如图,下列说法错误的是
| A.使用硝酸酸浸会产生污染环境的气体 |
B.氧化过程的反应为 |
C. 溶液中存在的化学键有离子键、共价键、氢键 溶液中存在的化学键有离子键、共价键、氢键 |
| D.煅烧氢氧化铁前,需洗去表面吸附的杂质 |
您最近一年使用:0次
2024-04-01更新
|
335次组卷
|
2卷引用:辽宁省锦州市渤海大学附属高级中学2023-2024学年高三下学期3月摸底考试化学试题



