解题方法
1 . 金属钛( )密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。
)密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。
(1) 元素在周期表中的分区是位于
元素在周期表中的分区是位于___________ 区。基态 原子中含有的未成对电子数是
原子中含有的未成对电子数是___________ 。
(2)金红石主要成分是钛的氧化物,该氧化物的晶胞形状为长方体,边长分别为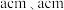 和
和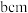 ,结构如下图所示。
,结构如下图所示。___________ , 位于距离最近的
位于距离最近的 构成的
构成的___________ 中心(填字母序号,下同)。
a.三角形 b.四面体 c.六面体 d.八面体
②该氧化物的晶体熔点为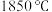 ,其晶体类型
,其晶体类型最不可 能是___________ 。
a.共价晶体 b.离子晶体 c.分子晶体
③若已知 该氧化物晶体体积为
该氧化物晶体体积为 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为___________  。
。
(3)以钓铁矿 为原料,用美还原法冶炼金属钓的生产流程图如下:
为原料,用美还原法冶炼金属钓的生产流程图如下: 元素在元素周期表中的位置是
元素在元素周期表中的位置是___________ 。
②“高温氯化”时还得到一种可燃性气体,写出反应的化学方程式:___________ 。
③结合流程及下表数据,“分离”时所需控制的最低温度应为___________  。
。
④已知 和
和 的晶胞类型相同,
的晶胞类型相同, 和
和 的离子半径大小相近,解释
的离子半径大小相近,解释 熔点高于
熔点高于 的原因:
的原因:___________ 。
 )密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。
)密度小,强度高,抗腐蚀性能好。含钛的矿石主要有金红石和铁铁矿。(1)
 元素在周期表中的分区是位于
元素在周期表中的分区是位于 原子中含有的未成对电子数是
原子中含有的未成对电子数是(2)金红石主要成分是钛的氧化物,该氧化物的晶胞形状为长方体,边长分别为
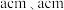 和
和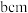 ,结构如下图所示。
,结构如下图所示。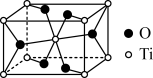
 位于距离最近的
位于距离最近的 构成的
构成的a.三角形 b.四面体 c.六面体 d.八面体
②该氧化物的晶体熔点为
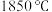 ,其晶体类型
,其晶体类型a.共价晶体 b.离子晶体 c.分子晶体
③若已知
 该氧化物晶体体积为
该氧化物晶体体积为 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为 。
。(3)以钓铁矿
 为原料,用美还原法冶炼金属钓的生产流程图如下:
为原料,用美还原法冶炼金属钓的生产流程图如下:
 元素在元素周期表中的位置是
元素在元素周期表中的位置是②“高温氯化”时还得到一种可燃性气体,写出反应的化学方程式:
③结合流程及下表数据,“分离”时所需控制的最低温度应为
 。
。 |  |  | |
熔点/ | 1668 | 651 | 714 |
沸点/ | 3287 | 1107 | 1412 |
 和
和 的晶胞类型相同,
的晶胞类型相同, 和
和 的离子半径大小相近,解释
的离子半径大小相近,解释 熔点高于
熔点高于 的原因:
的原因:
您最近一年使用:0次
2 . 按要求回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是___ ,占据该能层电子的电子云轮廓图形状____ 。
(2)Fe成为阳离子时首先失去_______ 轨道电子,写出Fe2+简化核外电子排布_______ 。
(3)P位于元素周期表中第三周期_______ 族,基态P原子核外未成对电子有_______ 个。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)Fe成为阳离子时首先失去
(3)P位于元素周期表中第三周期
您最近一年使用:0次
2024-04-24更新
|
55次组卷
|
2卷引用:陕西省兴平市南郊高级中学2023-2024学年高二上学期第三次化学质量检测题
3 . 原子轨道
(1)定义
_____ 称为原子轨道。
(2)原子轨道的形状
s电子原子轨道是_____ 形的,p电子原子轨道是_____ 形的。
(1)定义
(2)原子轨道的形状
s电子原子轨道是
您最近一年使用:0次
名校
解题方法
4 . 下列关于物质结构或性质及解释都正确的是
| 物质结构或性质 | 解释 | |
| A | 键角: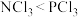 | N的电负性比P大,孤电子对对成键电子对的斥力比较大 |
| B | 稳定性:HF>HCl | HF分子间可以形成氢键,HCl没有氢键 |
| C | 配位键的稳定性: |  中O电负性更大,因而形成的配位键更稳定 中O电负性更大,因而形成的配位键更稳定 |
| D | 电子云半径:2s<4s | 4s电子能量高,在离核更远的区域出现的概率大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列说法不正确的是
A.H只能形成 键,O可以形成 键,O可以形成 键和 键和 键 键 |
B.氧原子可以形成 、 、 ,也可以形成 ,也可以形成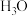 |
| C.共价键的成键原子可以是非金属原子也可以是金属原子 |
D. 键和 键和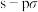 键的电子云形状的对称性相同 键的电子云形状的对称性相同 |
您最近一年使用:0次
6 . 完成下列问题
(1)As元素在周期表中的位置为___________ ,基态硫原子核外电子的空间运动状态有___________ 种。
(2)基态镍原子价电子排布图为___________ ,Cu形成 失去
失去___________ 轨道电子。
(3)下列状态的镁,电离最外层一个电子所需能量最大的是___________ (填标号);当镁从B状态变到C状态,形成的是___________ 光谱(选填“发射”或“吸收”)。
A. B.
B. C.
C.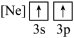 D.
D.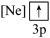
(1)As元素在周期表中的位置为
(2)基态镍原子价电子排布图为
 失去
失去(3)下列状态的镁,电离最外层一个电子所需能量最大的是
A.
 B.
B. C.
C. D.
D.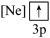
您最近一年使用:0次
2024-01-30更新
|
327次组卷
|
2卷引用:浙江省义乌市义亭中学2023-2024学年高二上学期化学期末模拟试题(一)
名校
解题方法
7 . 对原子结构的认识是理解元素周期律和元素周期性的理论基础。下列说法错误的是。
| A.s电子的电子云轮廓图是球形 |
| B.同一原子中,3s电子的能量大于4s电子的能量 |
| C.处于最低能量状态的原子叫基态原子 |
| D.同一原子中,3p能级的轨道数等于4p能级的轨道数 |
您最近一年使用:0次
解题方法
8 . 下列说法不正确的是
| A.从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道 |
| B.原子核外电子排布,先排满K层再排L层、先排满M层再排N层 |
| C.2p、3p、4p的轨道形状均为哑铃形 |
D.能层含有的原子轨道数为 (n为能层序数) (n为能层序数) |
您最近一年使用:0次
9 . 下列有关化学用语表示错误的是
A.氯气的共价键电子云轮廓图: |
| B.二氧化硅的分子式为SiO2 |
C.N2H4的电子式: |
D.基态氧原子电子轨道表示式为: |
您最近一年使用:0次
2024-01-11更新
|
1028次组卷
|
3卷引用:辽宁省重点高中沈阳市郊联体2023-2024学年高二上学期期末考试化学试题
名校
10 . 依据原子结构知识回答下列问题。
(1)下列有关说法错误的是___________。
(2)基态V原子中具有____ 种不同能量的电子,具有_____ 种不同空间运动状态的电子,具有____ 种不同运动状态的电子。
(3)基态Cr原子的简化电子排布式为_________ ,基态Se原子的价电子轨道表示式为______ 。
(4)元素Cu在元素周期表中的位置_____ ,属于_____ 区,化合物 在加热条件下容易转化为
在加热条件下容易转化为 ,从原子结构的角度解释原因
,从原子结构的角度解释原因___________ 。
(5) 是离子晶体,其形成过程中的能量变化如图所示。
是离子晶体,其形成过程中的能量变化如图所示。
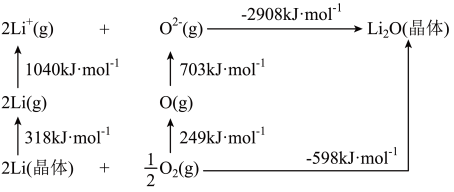
可知,Li原子的第一电离能为____  ,
, 键键能为
键键能为_____  。
。
(1)下列有关说法错误的是___________。
A.简单离子的还原性: |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(2)基态V原子中具有
(3)基态Cr原子的简化电子排布式为
(4)元素Cu在元素周期表中的位置
 在加热条件下容易转化为
在加热条件下容易转化为 ,从原子结构的角度解释原因
,从原子结构的角度解释原因(5)
 是离子晶体,其形成过程中的能量变化如图所示。
是离子晶体,其形成过程中的能量变化如图所示。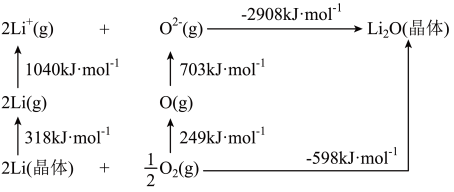
可知,Li原子的第一电离能为
 ,
, 键键能为
键键能为 。
。
您最近一年使用:0次



