名校
解题方法
1 . 2023年6月,科学家首次合成含铍-铍能的固态化合物,相关成果发表于《科学》杂质。该分子入选2023年最“炫”分子榜单,其结构如图所示,回答下列问题: 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为_____ (填序号)。
A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
(3)“固态双铍化合物的化学式为_____ ,它不含_____ (填标号)。
A.极性键 B.非极性键 C.金属键 D. 键
键
(4)卤化铍的熔点如表所示:
① 中
中 原子的杂化方式为
原子的杂化方式为_____ ;
②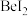
_____ (填“能”或“不能)溶于四氯化碳:
③ 、
、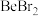 、
、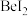 的熔点依次升高的原因是
的熔点依次升高的原因是_____ 。
(5) 易形成配离子
易形成配离子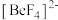 ,其中心阳离子的配位数为
,其中心阳离子的配位数为_____ ,配体是_____ (填化学符号),配离子的空间构型为_____ 。
(6)离子晶体中稳定配位多面体的理论半径比如表所示:
已知铍离子、氧离子的半径分别为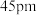 、
、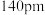 ,
, 的配位多面体是
的配位多面体是_____ 。
(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为_____ ;设晶胞参数为 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为_____  (用含a和
(用含a和 的式子表示)。
的式子表示)。
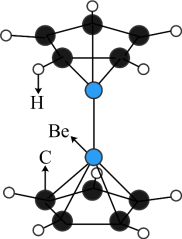
 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
A.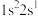 | B. | C.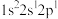 | D. |
(3)“固态双铍化合物的化学式为
A.极性键 B.非极性键 C.金属键 D.
 键
键(4)卤化铍的熔点如表所示:
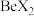 | 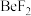 |  | 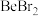 | 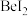 |
熔点/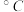 | 552 | 399 | 488 | 510 |
 中
中 原子的杂化方式为
原子的杂化方式为②
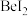
③
 、
、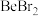 、
、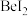 的熔点依次升高的原因是
的熔点依次升高的原因是(5)
 易形成配离子
易形成配离子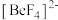 ,其中心阳离子的配位数为
,其中心阳离子的配位数为(6)离子晶体中稳定配位多面体的理论半径比如表所示:
| 配位多面体 | 配位数 | 半径比(r+/r-) |
| 平面三角形 | 3 | 0.15~0.225 |
| 四面体 | 4 | 0.225~0.414 |
| 八面体 | 6 | 0.414~0.732 |
| 立方体 | 8 | 0.732~1.000 |
| 立方八面体 | 12 | 1.000 |
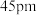 、
、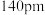 ,
, 的配位多面体是
的配位多面体是(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为
 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为 (用含a和
(用含a和 的式子表示)。
的式子表示)。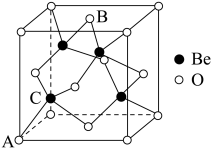
您最近半年使用:0次
名校
2 . 前四周期元素W、X、Y、Z的原子序数依次增大,且互相不同周期不同族。其中W是宇宙中含量最多的元素;X元素基态原子最高能级的不同轨道都有电子,并且自旋方向相同:Y元素基态原子最外层电子数等于其能层数:Z元素基态原子核外未成对电子数同周期最多。下列说法正确的是
| A.Y元素最高价氧化物对应的水化物为强碱 | B.基态X原子核外电子有7种空间运动状态 |
C.基态原子中未成对电子数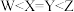 | D.Z形成的两种含氧酸根在溶液中存在着化学平衡 |
您最近半年使用:0次
解题方法
3 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可形成多种化合物。某化合物是潜在热电材料之一,其晶胞结构如图甲所示,晶胞参数为apm,沿x、y、z轴方向的投影均如图乙所示。
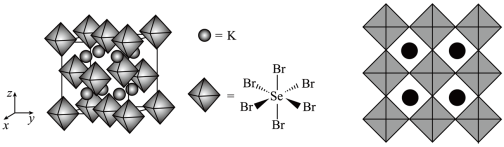
下列说法错误的是

下列说法错误的是
| A.基态钾原子核外电子有10种空间运动状态 |
B.Se和K的最短距离为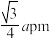 |
C.该化合物的化学式为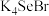 。 。 |
| D.距离Se最近的Se有12个 |
您最近半年使用:0次
解题方法
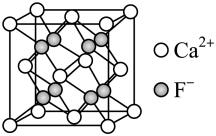
4 . 萤石是制作光学玻璃的原料之一,其主要成分氟化钙的晶胞结构如图所示。已知:原子中电子有两种相反的自旋状态,一种用 表示,另一种用
表示,另一种用 表示。下列说法错误的是
表示。下列说法错误的是
 表示,另一种用
表示,另一种用 表示。下列说法错误的是
表示。下列说法错误的是
A. 位于 位于 构成的四面体空隙 构成的四面体空隙 |
B.每个 周围距离最近且等距的 周围距离最近且等距的 有8个 有8个 |
| C.基态氟原子核外电子的原子轨道有四种伸展方向 |
D.基态F原子的电子自旋量子数的代数和为 |
您最近半年使用:0次
名校
解题方法
5 . 配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。Ni(CO)4为______ (填“极性”或“非极性”)分子,______ (“能”或“不能”)判断该分子的构型为平面正四边形。
(2)茜草中的茜素与Al3+、Ca2+生成的红色配合物X是最早的媒染染料。

基态Ca2+的核外电子的运动状态有______ 种,配合物X中Al3+的配体除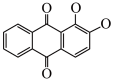 外还有
外还有______ ,茜素水溶性较好的主要原因是______ 。
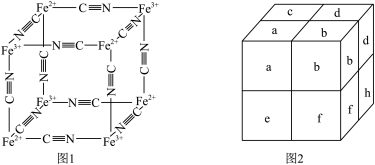
(3)向FeSO4溶液中滴加K3[Fe(CN)6]溶液后,经提纯、结晶可得到KFe[Fe(CN)6]普鲁士蓝蓝色晶体。实验表明,CN-、Fe2+、Fe3+通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体g未标出)。
①通过______ 实验,可确定该晶体结构(填标号)。
a.核磁共振 b.红外光谱 c.X射线衍射 d.质谱
②已知铁的电离能数据如表:
则,铁的I4大于I3的可能原因是:______ (写2条)。
③可溶性氰化物(如KCN)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是______ 。
④若Fe2+位于II型立方结构的棱心和体心上,则Fe3+位于II型立方结构的______ 上;一个II型立方结构中含______ 个K+;若KFe[Fe(CN)6]的摩尔质量为Mg/mol,该蓝色晶体密度为ρg/cm3,II型立方结构的边长为anm,则阿伏加德罗常数的值可表示为_______ 。
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。Ni(CO)4为
(2)茜草中的茜素与Al3+、Ca2+生成的红色配合物X是最早的媒染染料。

基态Ca2+的核外电子的运动状态有
 外还有
外还有(3)向FeSO4溶液中滴加K3[Fe(CN)6]溶液后,经提纯、结晶可得到KFe[Fe(CN)6]普鲁士蓝蓝色晶体。实验表明,CN-、Fe2+、Fe3+通过配位键构成了晶体的骨架。其局部结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为II型立方结构,下层左后的小立方体g未标出)。

①通过
a.核磁共振 b.红外光谱 c.X射线衍射 d.质谱
②已知铁的电离能数据如表:
| 电离能/(kJ•mol-1) | I1 | I2 | I3 | I4 | …… |
| Fe | 759 | 1561 | 2597 | 2597 | …… |
③可溶性氰化物(如KCN)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是
④若Fe2+位于II型立方结构的棱心和体心上,则Fe3+位于II型立方结构的
您最近半年使用:0次
解题方法
6 . 主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,从该矿渣中回收六水合硫酸镍晶体的工艺流程如图:

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。
(1)28Ni位于元素周期表_____ 区(填“s”“p”“d”或“ds”),其基态原子核外电子的空间运动状态有_____ 种。
(2)“焙烧”中,SiO2几乎不发生反应,NiO、CaO、FeO转化为相应的硫酸盐。NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为______ 。
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有______ (填化学式),为检验浸出液中是否含有Fe3+,可选用的化学试剂是______ 。
(4)“浸出液”中c(Ca2+)=1.0×10-3mol•L-1,加NaF固体时,忽略溶液体积变化,当除钙率达到99%时,除钙后的溶液中c(F-)=______ 。[已知Ksp(CaF2)=4.0×10-11]
(5)“萃取”时发生反应Mn+(水相)+nRH(有机相) MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与
MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与 的关系如图所示,V0/VA的最佳取值为
的关系如图所示,V0/VA的最佳取值为______ ;“反萃取”能使有机相再生而循环使用,可在有机相中加入______ ,待充分反应后再分液。

(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
从NiSO4溶液获得稳定的NiSO4•H2O晶体的操作是:______ 、______ 、过滤、洗涤、干燥等多步操作。

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。
(1)28Ni位于元素周期表
(2)“焙烧”中,SiO2几乎不发生反应,NiO、CaO、FeO转化为相应的硫酸盐。NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有
(4)“浸出液”中c(Ca2+)=1.0×10-3mol•L-1,加NaF固体时,忽略溶液体积变化,当除钙率达到99%时,除钙后的溶液中c(F-)=
(5)“萃取”时发生反应Mn+(水相)+nRH(有机相)
 MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与
MRn(有机相)+nH+(水相)(Mn+为金属离子,RH为萃取剂),萃取率与 的关系如图所示,V0/VA的最佳取值为
的关系如图所示,V0/VA的最佳取值为
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
| 温度 | 低于30.8℃ | 30.8~53.8℃ | 53.8~280℃ | 高于280℃ |
| 晶体形态 | NiSO4•7H2O | NiSO4•H2O | 多种结晶水合物 | NiSO4 |
您最近半年使用:0次
7 . 73号元素钽(Ta)与砷(As)形成的晶体在室温下拥有超高的空穴迁移率和较低的电子迁移率,其长方体晶胞结构如图所示。下列说法错误的是
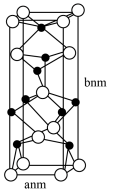

| A.基态As原子核外N层有4种空间运动状态不同的电子 |
| B.该晶胞中As的配位数为4 |
| C.该晶体的化学式为TaAs |
D.TaAs的晶体密度 |
您最近半年使用:0次
名校
解题方法
8 . 观察下列模型或图谱,结合有关信息进行判断,下列说法正确的是
A | B | C | D | |
模型或图谱 |  | 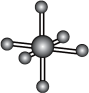 | 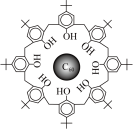 |  |
| H原子的电子云图 |  分子球棍模型 分子球棍模型 |  可装入空腔大小适配的“杯酚” 可装入空腔大小适配的“杯酚” |  X射线衍射图谱 X射线衍射图谱 |
| A.由图可见H原子核外靠近核运动的电子多 |
B. 是由极性键构成的非极性分子 是由极性键构成的非极性分子 |
C.超分了“杯酚”与 形成氢键而识别 形成氢键而识别 |
D.从图中可知a是晶态 粉末的X射线衍射图谱 粉末的X射线衍射图谱 |
您最近半年使用:0次
2023-04-22更新
|
293次组卷
|
3卷引用:广东省广州中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
9 . 许多物质中同一元素可以存在多种化合价, 或是可以看成存在多种化合价,这样有助于把握某些反应的本质。元素R是最高化合价为+6的短周期元素,Na2R2O8是一种极强的氧化剂,该物质的某种元素可以看成存在多种化合价。注:回答下列问题时,必须用R元素的真实元素符号作答。
(1)R元素的基态原子中,具有_______ 种不同空间运动状态的电子,具有_______ 种不同运动状态的电子。
(2)已知氧化性: >
> >I2。若将Na2R2O8溶液逐滴滴加到淀粉KI试纸上,则可以看到
>I2。若将Na2R2O8溶液逐滴滴加到淀粉KI试纸上,则可以看到_______ 的现象。该过程中被还原的元素是_______ 。
(3)加热Na2R2O8溶液,可以放出一种无色无味气体,结合上述信息,写出该反应的化学方程式_______ 。
(1)R元素的基态原子中,具有
(2)已知氧化性:
 >
> >I2。若将Na2R2O8溶液逐滴滴加到淀粉KI试纸上,则可以看到
>I2。若将Na2R2O8溶液逐滴滴加到淀粉KI试纸上,则可以看到(3)加热Na2R2O8溶液,可以放出一种无色无味气体,结合上述信息,写出该反应的化学方程式
您最近半年使用:0次
名校
10 . 钛(22Ti)和钛的合金大量用于航空工业,有“空间金属”之称,制备钛的一种流程如下。
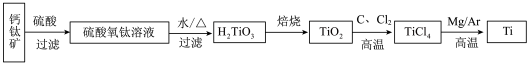
(1)基态Ti原子核外有_______ 种运动状态不同的电子
(2)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图。

化合物乙的沸点明显高于化合物甲,主要原因是_______ 。
(3)SO 的VSEPR模型名称为
的VSEPR模型名称为_______ ,硫酸氧钛晶体中,阳离子为链状聚合形式的离子,结构如图所示,则硫酸氧钛化学式为_______ 。
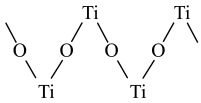
(4)如图是硫的四种含氧酸根的结构,根据组成和结构推断,能在酸性溶液中能将Mn2+转化为MnO 的是_______(填标号)。
的是_______(填标号)。

(1)基态Ti原子核外有
(2)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图。

化合物乙的沸点明显高于化合物甲,主要原因是
(3)SO
 的VSEPR模型名称为
的VSEPR模型名称为
(4)如图是硫的四种含氧酸根的结构,根据组成和结构推断,能在酸性溶液中能将Mn2+转化为MnO
 的是_______(填标号)。
的是_______(填标号)。A. | B.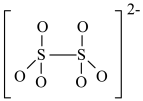 |
C.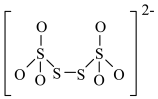 | D.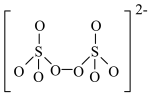 |
您最近半年使用:0次



