1 . 完成下列问题
(1)As元素在周期表中的位置为___________ ,基态硫原子核外电子的空间运动状态有___________ 种。
(2)基态镍原子价电子排布图为___________ ,Cu形成 失去
失去___________ 轨道电子。
(3)下列状态的镁,电离最外层一个电子所需能量最大的是___________ (填标号);当镁从B状态变到C状态,形成的是___________ 光谱(选填“发射”或“吸收”)。
A. B.
B. C.
C.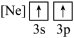 D.
D.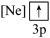
(1)As元素在周期表中的位置为
(2)基态镍原子价电子排布图为
 失去
失去(3)下列状态的镁,电离最外层一个电子所需能量最大的是
A.
 B.
B. C.
C. D.
D.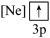
您最近一年使用:0次
2024-01-30更新
|
327次组卷
|
2卷引用:浙江省义乌市义亭中学2023-2024学年高二上学期化学期末模拟试题(一)
2 . A、B、C、D代表4种元素。请填空:
(1)A原子序数为24的元素原子中有___________ 个电子层,___________ 个能级,___________ 个未成对电子,位于元素周期表的___________ 区。
(2)B原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子的价电子排布图:___________ 。
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D元素基态原子的电子排布式为___________ ,其单质在一定条件下能与浓硫酸反应,试写出该反应的化学方程式:___________ 。
(1)A原子序数为24的元素原子中有
(2)B原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子的价电子排布图:
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D元素基态原子的电子排布式为
您最近一年使用:0次
解题方法
3 . 人类文明的发展历程,也是化学物质的认识和发现历程。
(1)基态O原子中能量最高的电子所占据的原子轨道形状为___________ ,高温下 比
比 更稳定,试从核外电子排布的角度解释其原因:
更稳定,试从核外电子排布的角度解释其原因:___________ 。
(2) 分子中C元素的化合价为
分子中C元素的化合价为___________ 。类卤素 对应的酸有两种,理论上硫氰酸
对应的酸有两种,理论上硫氰酸 的沸点低于异硫氰酸
的沸点低于异硫氰酸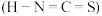 的沸点,其原因是
的沸点,其原因是___________ 。
(3) 中
中 的键角比
的键角比 的键角小,其原因为
的键角小,其原因为___________ 。
(4)在高温超导领域中,有一种化合物叫钙钛矿,其晶胞结构如图所示。
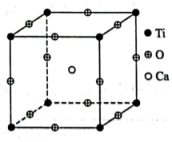
①钙钛矿的化学式为___________ ,距每个钛离子最近的氧离子的数目有___________ 个。
②设阿伏加德罗常数的值为 ,晶胞的边长为
,晶胞的边长为 ,则该晶胞的密度为
,则该晶胞的密度为
___________ 。
(1)基态O原子中能量最高的电子所占据的原子轨道形状为
 比
比 更稳定,试从核外电子排布的角度解释其原因:
更稳定,试从核外电子排布的角度解释其原因:(2)
 分子中C元素的化合价为
分子中C元素的化合价为 对应的酸有两种,理论上硫氰酸
对应的酸有两种,理论上硫氰酸 的沸点低于异硫氰酸
的沸点低于异硫氰酸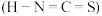 的沸点,其原因是
的沸点,其原因是(3)
 中
中 的键角比
的键角比 的键角小,其原因为
的键角小,其原因为(4)在高温超导领域中,有一种化合物叫钙钛矿,其晶胞结构如图所示。

①钙钛矿的化学式为
②设阿伏加德罗常数的值为
 ,晶胞的边长为
,晶胞的边长为 ,则该晶胞的密度为
,则该晶胞的密度为
您最近一年使用:0次
4 . 地壳中含量最多的元素的基态原子的轨道表示式_____ ,能量最是高的电子所在的轨道呈_____ 形。
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题:
(1)某元素原子的基态电子排布式为[Ar]3d104s24p1,该元素处于元素周期表的位置______ 。
(2)Ti基态原子的电子排布式为______ ,Ti元素位于____ 区,基态Ti原子核外有_____ 种不同运动状态的电子。
(3)铝原子核外电子云有_____ 种不同的伸展方向,其基态电子有_____ 种空间运动状态。
(4)基态Fe2+与Fe3+离子中未成对的电子数之比为______ 。与H2O分子互为等电子体一种阴离子为______ (填化学式)。
(1)某元素原子的基态电子排布式为[Ar]3d104s24p1,该元素处于元素周期表的位置
(2)Ti基态原子的电子排布式为
(3)铝原子核外电子云有
(4)基态Fe2+与Fe3+离子中未成对的电子数之比为
您最近一年使用:0次
6 . 某国产电动汽车推出的“刀片电池”具有强环境适应性,更安全可靠。“刀片电池”正极材料使用了磷酸亚铁锂(LiFePO4)。磷酸亚铁锂(LiFePO4)由Li2CO3、C6H12O6和FePO4在高温条件下制备。
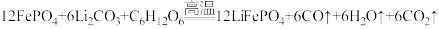
(1)铁是26号元素,它是___________ 。(选填编号)
a.主族元素b.副族元素c.短周期元素d.长周期元素
磷元素的原子核外有___________ 种运动状态不同的电子。
(2)上述方程式中,CO2的电子式为___________ ,属于第二周期的元素,原子半径由小到大排列___________ 。
(3)反应中的氧化剂是___________ ;当有0.1molLiFePO4生成时,转移电子的数目为___________ 个。
磷酸亚铁锂也可以用(CH3COO)2Fe、NH4H2PO4和LiOH为原料制备。
(4)NH4H2PO4溶于水形成的溶液中存在:c(H+)+c( )=c(OH-)+c(H2PO
)=c(OH-)+c(H2PO )+
)+___________ 。
(5)请解释(CH3COO)2Fe溶于水显酸性的原因___________ 。
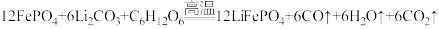
(1)铁是26号元素,它是
a.主族元素b.副族元素c.短周期元素d.长周期元素
磷元素的原子核外有
(2)上述方程式中,CO2的电子式为
(3)反应中的氧化剂是
磷酸亚铁锂也可以用(CH3COO)2Fe、NH4H2PO4和LiOH为原料制备。
(4)NH4H2PO4溶于水形成的溶液中存在:c(H+)+c(
 )=c(OH-)+c(H2PO
)=c(OH-)+c(H2PO )+
)+(5)请解释(CH3COO)2Fe溶于水显酸性的原因
您最近一年使用:0次
7 . 黑火药的爆炸反应原理为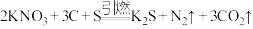 。请回答下列问题:
。请回答下列问题:
(1)基态 原子核外有
原子核外有___________ 种空间运动状态的电子。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为___________ 。
(3)K位于周期表的___________ 区;基态钾离子的电子占据的最高能层符号是___________ 。
(4) 与
与 具有相同的电子构型,
具有相同的电子构型,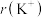 小于
小于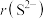 ,原因是
,原因是___________ 。
(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是___________ 。
a.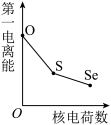 b.
b.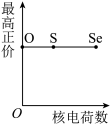 c.
c.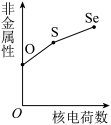 d.
d.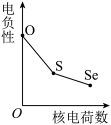
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能 。
。 的Born-Haber循环如图所示。
的Born-Haber循环如图所示。

由图可知, 原子的第二电离能为
原子的第二电离能为___________  ;
; 键的键能为
键的键能为___________  ;氧原子的第一电子亲和能为
;氧原子的第一电子亲和能为___________  ;
; 的晶格能为
的晶格能为___________  。
。
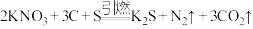 。请回答下列问题:
。请回答下列问题:(1)基态
 原子核外有
原子核外有(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为(3)K位于周期表的
(4)
 与
与 具有相同的电子构型,
具有相同的电子构型,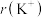 小于
小于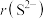 ,原因是
,原因是(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是
a.
 b.
b. c.
c. d.
d.
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能
 。
。 的Born-Haber循环如图所示。
的Born-Haber循环如图所示。
由图可知,
 原子的第二电离能为
原子的第二电离能为 ;
; 键的键能为
键的键能为 ;氧原子的第一电子亲和能为
;氧原子的第一电子亲和能为 ;
; 的晶格能为
的晶格能为 。
。
您最近一年使用:0次
名校
解题方法
8 . 合成氨有助于解决地球上粮食不足问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态N原子中,能量最高的电子的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(2)我国科研人员研制出了“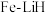 ”催化剂,使得合成氨温度和压强分别降到了350℃,
”催化剂,使得合成氨温度和压强分别降到了350℃, ,这是近年来合成氨反应研究中心的重要突破。
,这是近年来合成氨反应研究中心的重要突破。
①第三电离能
_______ 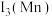 (填“>”或“<”),原因是
(填“>”或“<”),原因是_______ 。
②比较 与
与 的半径大小关系:
的半径大小关系: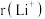
_______  (填“>”或“<”)。
(填“>”或“<”)。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将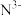 转化为NH2,反应过程如图所示:
转化为NH2,反应过程如图所示:
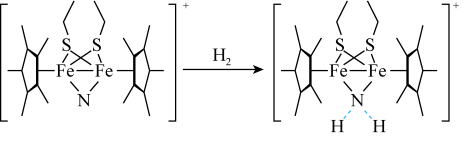
产物中 原于的杂化轨道类型为
原于的杂化轨道类型为_______ 。
(1)基态N原子中,能量最高的电子的电子云在空间有
(2)我国科研人员研制出了“
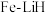 ”催化剂,使得合成氨温度和压强分别降到了350℃,
”催化剂,使得合成氨温度和压强分别降到了350℃, ,这是近年来合成氨反应研究中心的重要突破。
,这是近年来合成氨反应研究中心的重要突破。①第三电离能

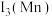 (填“>”或“<”),原因是
(填“>”或“<”),原因是②比较
 与
与 的半径大小关系:
的半径大小关系: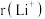
 (填“>”或“<”)。
(填“>”或“<”)。(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将
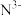 转化为NH2,反应过程如图所示:
转化为NH2,反应过程如图所示:
产物中
 原于的杂化轨道类型为
原于的杂化轨道类型为
您最近一年使用:0次
名校
9 . 回答下列问题:
(1)下面是s能级与p能级的原子轨道图:
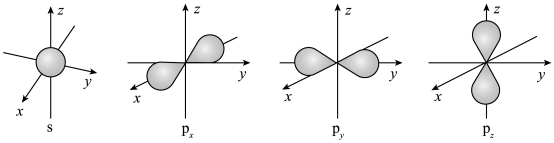
请回答下列问题:
①s电子的原子轨道呈_______ 形,每个s能级有_______ 个原子轨道;
②p电子的原子轨道呈_______ 形,每个p能级有_______ 个原子轨道。
(2)写出下列元素基态原子的电子排布式。
①Co:_______ ;
②Cu:_______ 。
(3)画出下列元素基态原子的轨道表示式。
①P:_______ ;
②F:_______ 。
(1)下面是s能级与p能级的原子轨道图:

请回答下列问题:
①s电子的原子轨道呈
②p电子的原子轨道呈
(2)写出下列元素基态原子的电子排布式。
①Co:
②Cu:
(3)画出下列元素基态原子的轨道表示式。
①P:
②F:
您最近一年使用:0次
2023-02-27更新
|
408次组卷
|
3卷引用:黑龙江省伊春市伊美区第二中学2022-2023学年高二下学期期初考试化学试题
2022高二上·四川·学业考试
10 . 下表列出了①~④四种元素在周期表中的位置.
回答下列问题:
(1)①的元素符号为_____________ 。
(2)②的基态原子电子排布式为__________________________ 。
(3)③和④中原子半径较大的是_____________ (填元素符号)。
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为_____________ 形;每个p能级都有_____________ 个相互垂直的电子云。

| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ||||||
| 4 | ④ |
回答下列问题:
(1)①的元素符号为
(2)②的基态原子电子排布式为
(3)③和④中原子半径较大的是
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为

您最近一年使用:0次



