名校
解题方法
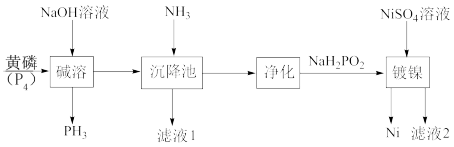
1 . 次磷酸钠(NaH2PO2)是具有珍珠光泽的晶体或白色结晶性粉末,易溶于水、乙醇、甘油,微溶于氨水,不溶于乙醚。次磷酸钠(NaH2PO2)广泛应用于化学镀镍,其制备与镀镍过程如下图所示:
(1)基态Ni原子的核外电子排布式为_____ ,PH3的分子空间构型为_____ 。
(2)“碱溶”过程中,发生反应化学方程式为_____ 。
(3)“沉降池”中通入氨气的目的是_____ ,“净化”操作需要过滤、洗涤、干燥,洗涤时,选用的洗涤剂为_____ 。
(4)“滤液2”经分离提纯可以得H3PO2,写出“镀镍”过程发生的离子反应方程式_____ ,充分反应后,向“滤液2”中,加入适量 悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
_____ [已知: ,
, ]
]
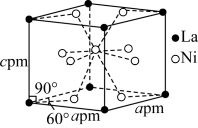
(5)Ni和La的合金是目前使用广泛的储氢材料,该合金的晶胞结构如图所示。_____ 。
②已知该晶体晶胞底面边长为apm,高为cpm,设 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为_____  (用含a、c、
(用含a、c、 的代数式表示)
的代数式表示)
(1)基态Ni原子的核外电子排布式为
(2)“碱溶”过程中,发生反应化学方程式为
(3)“沉降池”中通入氨气的目的是
(4)“滤液2”经分离提纯可以得H3PO2,写出“镀镍”过程发生的离子反应方程式
 悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
 ,
, ]
](5)Ni和La的合金是目前使用广泛的储氢材料,该合金的晶胞结构如图所示。
②已知该晶体晶胞底面边长为apm,高为cpm,设
 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为 (用含a、c、
(用含a、c、 的代数式表示)
的代数式表示)
您最近一年使用:0次
2023-09-15更新
|
136次组卷
|
2卷引用:甘肃省酒泉市瓜州县第一中学2023-2024学年高三上学期期末化学试题
解题方法
2 . 近年来我国科学家发现了一系列意义重大的铁系超导材料,其中含有Fe、As、Ti等元素。回答下列问题:
(1)Fe转化为阳离子时首先失去__ 轨道电子,基态Fe3+核外电子排布式为__ 。
(2)AsH3中心原子杂化类型为__ 。
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是__ ,理由是___ 。
(4)Ti金属晶体的堆积模型为__ ,配位数为__ ,基态Ti3+中未成对电子数有_ 个。
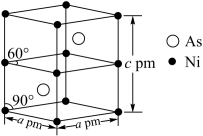
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=__ g·cm-3。
(1)Fe转化为阳离子时首先失去
(2)AsH3中心原子杂化类型为
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是
(4)Ti金属晶体的堆积模型为
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=

您最近一年使用:0次
解题方法
3 . 有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。

请回答下列问题:
(1)E元素原子基态时的电子排布式为________ 。
(2)A2F分子中F原子的杂化类型是________ ,F的氧化物FO3分子空间构型为________ 。
(3)CA3极易溶于水,其原因主要是______________ ,试判断CA3溶于水后,形成CA3·H2O的合理结构:________ (填字母代号)。

(4)从图中可以看出,D跟B形成的离子化合物的化学式为________ ;该离子化合物晶体的密度为ag·cm-3,相对分子质量为M,则晶胞的体积是____________ (写出表达式即可)。

请回答下列问题:
(1)E元素原子基态时的电子排布式为
(2)A2F分子中F原子的杂化类型是
(3)CA3极易溶于水,其原因主要是

(4)从图中可以看出,D跟B形成的离子化合物的化学式为
您最近一年使用:0次



