名校
解题方法
1 . 有A、B、C、D、E五种元素。其中A为第三周期主族元素,与D可形成原子个数比为1∶1和2∶1的化合物;B为第4周期过渡金属元素,且未成对电子数最多,最高化合价为+6价;C和A是同周期的元素,最高化合价为+7;D原子的价电子排布为nsnnpn+2,E元素的基态原子核外有7个原子轨道填充了电子。
(1)写出下面三种元素的元素符号:A___________ 、B___________ 、C___________ 。
(2)写出D2-的电子排布式:___________ 。基态E原子的外围电子排布图___________ 。
(3)C位于___________ 族,B位于___________ 区。
(1)写出下面三种元素的元素符号:A
(2)写出D2-的电子排布式:
(3)C位于
您最近一年使用:0次
名校
2 . 根据要求回答下列问题:
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是_________ 。
(2)①O2- ②Al3+ ③Cl- ④Ca2+的半径由大到小排列为:________ (用序号表示)。
(3)下列属于氧原子激发态的轨道表示式的有___________ (填字母)。_________ ,位于在周期表______ 区(填s、p、d或ds)。
(5)基态Si原子中,电子占据的最高能层符号为________ 。
(6)基态S原子的原子核外电子有______ 种空间运动状态,其能量最高的电子电子云轮廓图为______ 形。
(7)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:________ 。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①O2- ②Al3+ ③Cl- ④Ca2+的半径由大到小排列为:
(3)下列属于氧原子激发态的轨道表示式的有
a.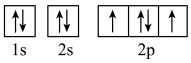 b.
b.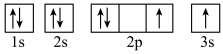
c.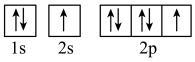 d.
d.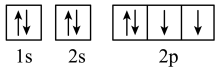
(5)基态Si原子中,电子占据的最高能层符号为
(6)基态S原子的原子核外电子有
(7)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
您最近一年使用:0次
2024-02-07更新
|
328次组卷
|
3卷引用:四川省成都石室中学2023-2024学年高二上学期期中考试化学试卷
3 . 下列说法或有关化学用语的表达正确的是
| A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
B.基态Fe原子的外围电子排布图为: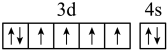 |
| C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素 |
您最近一年使用:0次
2024-02-04更新
|
203次组卷
|
62卷引用:四川省南充市阆中中学2020-2021学年高二上学期期中考试化学试题
四川省南充市阆中中学2020-2021学年高二上学期期中考试化学试题四川省遂宁市第二中学校2021-2022学年高二上学期期中考试化学试题四川省广元中学2022-2023学年高二下学期5月期中考试化学试题2014-2015学年宁夏宁大附中高二上学期期中考试化学试卷2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷2015-2016学年贵州省思南中学高二下期中化学试卷2015-2016学年辽宁省五校协作体高二下学期期中考试化学试卷四川省广安市第二中学校2017-2018学年高二下学期第二次月考化学试题内蒙古自治区第一机械制造(集团)有限公司第一中学2018-2019学年高二下学期期中考试化学试题四川省广安第二中学校2017-2018学年高二下学期第一次月考化学试题陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题吉林省长春市第二十九中学2019-2020学年高二下学期期中考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省莆田市仙游县第二中学2019-2020学年高二下学期期中考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期期中考试化学试题天津市实验中学滨海学校2020-2021学年高二下学期期中化学试题甘肃省武威第十八中学2020-2021学年高二下学期期中考试化学试题安徽省合肥市肥东县综合高中2021-2022学年高二下学期期中考试化学试题四川省广安市邻水县二中 2022-2023学年高三上学期9月考化学试题福建省泉州科技中学2021-2022学年高二下学期期中考试化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题安徽省安庆市第二中学2022-2023学年高二下学期期中考试化学试题(已下线)2013-2014宁夏银川一中高二下学期期末考试化学试卷2015-2016学年山西省大同一中高二下3月月考化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷山西省大同市第一中学2016-2017学年高二5月月考化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题贵州省思南中学2016-2017学年高二下学期期末考试化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题山西省沁县中学2018-2019学年高二下学期第一次月考化学试题吉林省扶余市第一中学2018-2019学年高二下学期第一次月考化学试题山东省聊城市2019-2020学年高三化学一轮复习《物质结构与性质(》模拟测试辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题安徽省蚌埠第三中学2019-2020学年高二下学期期末考试化学试题(已下线)模块同步卷12 综合检测卷(提升卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记山东省济南市济阳区闻韶中学2020-2021学年高三(3班)12月第一次模拟考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题(已下线)作业02 原子结构与元素的性质-2021年高二化学暑假作业(人教版2019)新疆昌吉教育共同体2020-2021学年高二下学期期末质量检测化学试题福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题宁夏银川市第六中学2020-2021学年高二下学期期末考试化学试题辽宁省本溪市第二高级中学2021-2022学年高二上学期期末考试化学试题山西省长治市沁源县第一中学等名校2021-2022学年高二下学期5月联考化学试题吉林地区普通高中友好学校联合体2021-2022学年高二下学期期末考试化学试题第一章 本章复习提升1云南省石屏县第一中学2021-2022学年高二下学期3月份考试化学试题福建省莆田市第一中学2021-2022学年高二下学期期末考试化学试题甘肃省庆阳市第六中学2021-2022学年高二下学期期末考试化学试题新疆克拉玛依市高级中学2021-2022学年高二下学期期末考试化学试题重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题山东省新泰市第一中学2022-2023学年高二下学期第一次大单元考试化学试题山东省青岛第十九中学2022-2023学年高二下学期4月月考化学试题河北省唐山市开滦一中2022-2023学年高二下学期期末考试化学试题吉林省普通高中友好学校联合体2023-2024学年高二上学期第三十七届基础年段期末联考化学试题湖南省长郡中学2023-2024学年高二下学期寒假检测(开学考试)化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题(已下线)猜想01 原子结构与性质 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
名校
解题方法
4 . 下列化学用语表达正确的是
A. 的结构示意图: 的结构示意图: |
B. 的电子式: 的电子式: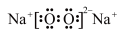 |
C.中子数为32、质子数为26的核素符号: |
D.基态C原子的价层电子轨道表示式: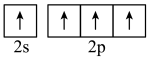 |
您最近一年使用:0次
2024-01-20更新
|
209次组卷
|
3卷引用:四川省阆中中学校2023-2024学年高二下学期4月期中化学试题
名校
解题方法
5 . 下列化学用语或图示表达正确的是
A.羟基的电子式: |
B. 的VSEPR模型: 的VSEPR模型: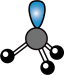 |
C.基态S原子的电子排布图: |
D.乙醇分子的空间填充模型 |
您最近一年使用:0次
2023-07-16更新
|
112次组卷
|
3卷引用:四川省南充市嘉陵第一中学2023-2024学年高二下学期4月期中考试化学试题
四川省南充市嘉陵第一中学2023-2024学年高二下学期4月期中考试化学试题河南省商丘名校联考2022-2023学年高二下学期7月期末考试化学试题(已下线)题型01 分子的空间构型及杂化类型的判断-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
名校
6 . 哈尔滨工业大学的李惠等人和加州大学洛杉矶分校的黄昱、段镶锋合作合成了具备超轻、高力学强度和超级隔热三大特点的氮化硼(hBNAGs)以及碳化硅( -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
(1)硅原子的价电子排布图为___________ 。B、N、O、Al的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。
① 从原子结构分析B容易与配体形成配位键的原因___________ 。
② 下列有关硼酸及其相关化合物的说法正确的是___________ (填标号)。
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
① 下列有关氨硼烷(NH3BH3)的说法中错误的是___________ (填标号)。
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷的电子式为___________ ,氨硼烷中H−N−H的键角___________ (填“>”“<”或“=”)H−B−H的键角。
 -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:(1)硅原子的价电子排布图为
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF
 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。① 从原子结构分析B容易与配体形成配位键的原因
② 下列有关硼酸及其相关化合物的说法正确的是
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
| 元素符号 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
① 下列有关氨硼烷(NH3BH3)的说法中错误的是
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷的电子式为
您最近一年使用:0次
名校
解题方法
7 . 下列说法或有关化学用语的表达正确的是
| A.乙醇比甲醚的沸点高是因为乙醇的分子间的范德华力更强 |
| B.基态Fe原子的价电子排布图为:3d64s2 |
C.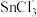 的几何构型为三角锥形,其中心离子的杂化方式为sp3杂化 的几何构型为三角锥形,其中心离子的杂化方式为sp3杂化 |
| D.CHClBrCH2F分子中不含手性碳原子 |
您最近一年使用:0次
名校
8 .  、
、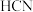 与
与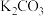 在一定条件下发生如下反应:
在一定条件下发生如下反应: 。下列说法错误的是
。下列说法错误的是
 、
、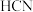 与
与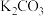 在一定条件下发生如下反应:
在一定条件下发生如下反应: 。下列说法错误的是
。下列说法错误的是A.此化学方程式中涉及的主族元素的非金属性由大到小的顺序为 >H >H |
B.配合物 的中心离子的价电子排布图为 的中心离子的价电子排布图为 ,该中心离子的配位数是 ,该中心离子的配位数是 |
C.配合物 的配体为CN-,配位原子为N 的配体为CN-,配位原子为N |
D.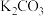 中阴离子的空间构型为平面三角形,其中碳原子的价层电子对数为 中阴离子的空间构型为平面三角形,其中碳原子的价层电子对数为 |
您最近一年使用:0次
9 . 下列所述的粒子 1~20号元素
1~20号元素 ,按半径由大到小的顺序排列正确的是
,按半径由大到小的顺序排列正确的是 基态
基态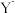 的价电子排布式为
的价电子排布式为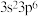
 基态
基态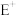 的最高能级的电子对数等于其最高能层序数
的最高能级的电子对数等于其最高能层序数
 1~20号元素
1~20号元素 ,按半径由大到小的顺序排列正确的是
,按半径由大到小的顺序排列正确的是 基态
基态 原子的结构示意图为
原子的结构示意图为
 基态
基态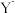 的价电子排布式为
的价电子排布式为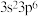
 基态
基态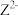 的轨道表示式为
的轨道表示式为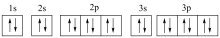
 基态
基态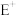 的最高能级的电子对数等于其最高能层序数
的最高能级的电子对数等于其最高能层序数A.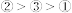 > > | B. |
C. | D.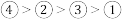 |
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语表示正确的是
A. 的分子模型示意图: 的分子模型示意图: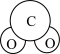 |
B.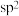 杂化轨道模型: 杂化轨道模型: |
C.H2O2的电子式: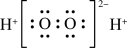 |
D.硅原子最外层电子的电子排布图: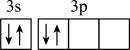 |
您最近一年使用:0次



