1 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。 、Ⅱ
、Ⅱ 元素属于
元素属于___________ 区。
②2017年5月9日我国发布了113号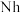 、115号
、115号 、117号
、117号 、118号
、118号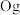 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期Ⅴ 族
族
b.117号元素 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:
(2)认识原子结构与元素周期表的关系:见表中元素 的信息,其中“
的信息,其中“ ”称为该元素原子的
”称为该元素原子的___________ ,该元素 能层上具有
能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ 。
②前四周期同族元素的某种性质 随核电荷数的变化趋势如图所示,则下列说法正确的是
随核电荷数的变化趋势如图所示,则下列说法正确的是___________ (填字母)。 、
、 、
、 表示氧族元素,则
表示氧族元素,则 表示对应氢化物的稳定性
表示对应氢化物的稳定性
B.若 、
、 、
、 表示卤族元素,则
表示卤族元素,则 表示对应简单离子的还原性
表示对应简单离子的还原性
C.若 、
、 、
、 表示第Ⅰ
表示第Ⅰ 族元素,则
族元素,则 表示对应离子的氧化性
表示对应离子的氧化性
D.若 、
、 、
、 表示第Ⅱ
表示第Ⅱ 族元素,则
族元素,则 表示最高价氧化物对应水化物的碱性
表示最高价氧化物对应水化物的碱性

 、Ⅱ
、Ⅱ 元素属于
元素属于②2017年5月9日我国发布了113号
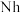 、115号
、115号 、117号
、117号 、118号
、118号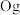 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是a.113号元素在周期表中的位置是第七周期Ⅴ
 族
族b.117号元素
 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:

(2)认识原子结构与元素周期表的关系:见表中元素
 的信息,其中“
的信息,其中“ ”称为该元素原子的
”称为该元素原子的 能层上具有
能层上具有(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:

 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是②前四周期同族元素的某种性质
 随核电荷数的变化趋势如图所示,则下列说法正确的是
随核电荷数的变化趋势如图所示,则下列说法正确的是
 、
、 、
、 表示氧族元素,则
表示氧族元素,则 表示对应氢化物的稳定性
表示对应氢化物的稳定性B.若
 、
、 、
、 表示卤族元素,则
表示卤族元素,则 表示对应简单离子的还原性
表示对应简单离子的还原性C.若
 、
、 、
、 表示第Ⅰ
表示第Ⅰ 族元素,则
族元素,则 表示对应离子的氧化性
表示对应离子的氧化性D.若
 、
、 、
、 表示第Ⅱ
表示第Ⅱ 族元素,则
族元素,则 表示最高价氧化物对应水化物的碱性
表示最高价氧化物对应水化物的碱性
您最近一年使用:0次
名校
解题方法
2 . 含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有 NO 等氮氧化物的尾气,反应方程式如下:NaClO + NO + H2O — NaCl + HNO3 (未配平)。
(1)氯在元素周期表中的位置是_______ ,其所在主族的元素中,最高价氧化物对应的水化物酸性最强的是_______ (填化学式)。其所在周期的元素中,第一电离能最大的是______ (填化学式)。
(2)配平上述反应方程式_______ 。每有 0.3mol 电子发生转移,可消耗标准状况下 NO 气体的体积约为______ L。
(3)NaClO 溶液中存在如下关系:c(OH-)_____ c(HClO)(填“>”、“=”、或“<”)。
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。
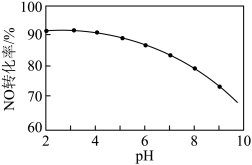
(4)NaClO 溶液的初始pH 越大,NO 的转化率越________ (填“高”或“低”),其原因是_________ 。
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
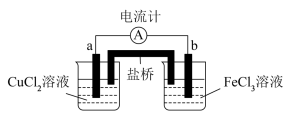
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式________ ;盐桥在原电池中所起的作用(任意写出一条)__________ 。
(1)氯在元素周期表中的位置是
(2)配平上述反应方程式
(3)NaClO 溶液中存在如下关系:c(OH-)
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。

(4)NaClO 溶液的初始pH 越大,NO 的转化率越
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
| 滴加 KI 溶液 | 再滴加 CCl4,振荡、静置 | 结论 | |
| A 试管 | 溶液变为棕黄色 | 溶液分层,下层显 | 氧化性强弱:(填“>”或“<”) KClO3 |
| B 试管 | 无现象 | 溶液分层,均无色 |
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式

您最近一年使用:0次
解题方法
3 . 硒(34Se)是人和动物体中一种必需的微量元素,存在于地球所有环境介质中,其同位素可有效示踪硒生物地球化学循环过程及其来源,下列说法不正确 的是
| A.Se位于周期表中第四周期第VIA族 |
| B.可用质谱法区分Se的两种同位素78Se和80Se |
| C.第一电离能:34Se>33As |
| D.SeO2既具有氧化性又具有还原性 |
您最近一年使用:0次
4 . 工业上电解熔融 和冰晶石(
和冰晶石( )的混合物可制得铝。下列说法
)的混合物可制得铝。下列说法不相符 的是
 和冰晶石(
和冰晶石( )的混合物可制得铝。下列说法
)的混合物可制得铝。下列说法A.半径大小: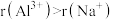 | B.还原性强弱: |
C.电离能大小: | D.碱性强弱: |
您最近一年使用:0次
2024-01-24更新
|
118次组卷
|
2卷引用:北京市顺义区2023-2024学年高二上学期期末考试化学试题
5 . X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X的原子半径小于Y的原子半径,Z基态原子核外有3个未成对电子,Y的核外电子数与Z的价层电子数相等,Q2是氧化性最强的单质,下列说法正确的是
| A.键能:Z2<W2<Q2 | B.YQ3、ZQ3 均为非极性分子 |
| C.沸点:X2W<XQ | D.同周期中第一电离能介于Y和Z之间的元素有3种 |
您最近一年使用:0次
2024-03-09更新
|
350次组卷
|
4卷引用:山东省烟台市2023-2024学年高三上学期期末考试化学试题
6 . 现有四种元素的基态原子的电子排布式如下:① ;②
;②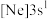 ;③
;③ ;④
;④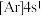 。则下列说法中正确的是
。则下列说法中正确的是
 ;②
;②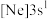 ;③
;③ ;④
;④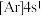 。则下列说法中正确的是
。则下列说法中正确的是| A.①和③元素均为非金属元素,并且位于同一主族 |
| B.②号元素的单质具有强氧化性 |
C.第一电离能: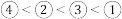 |
D.电负性: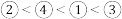 |
您最近一年使用:0次
2024-02-11更新
|
283次组卷
|
2卷引用:内蒙古呼和浩特市2023-2024学年高二上学期期末教学质量检测化学试卷
名校
7 . 短周期主族元素X、Y、Z、W的原子序数依次增大,基态Y原子有3个未成对电子,基态Z原子的价电子数等于其电子层数,这四种元素可形成离子化合物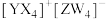 。下列叙述正确的是
。下列叙述正确的是
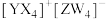 。下列叙述正确的是
。下列叙述正确的是A.氧化性: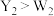 | B.电负性:Y>X>Z |
| C.Y的含氧酸一定是强酸 | D.第一电离能:Y<W |
您最近一年使用:0次
2023-12-30更新
|
479次组卷
|
2卷引用:贵州省黔西南布依族苗族自治州2023-2024学年高一上学期1月期末化学试题
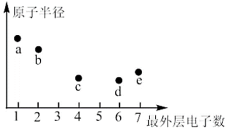
8 . a、b、c、d、e均为短周期主族元素,其中a与c的原子序数之和等于e的原子序数,上述五种元素的最外层电子数与原子半径的大小关系如图所示。请按要求回答下列问题:_______ (填元素符号),这些元素形成的酸性最强的最高价含氧酸和碱性最强的碱形成的盐是_______ (填化学式)。
(2)c、d、e三种元素可形成一种有毒气体 ,该气体分子的结构式为
,该气体分子的结构式为________ 。
(3)上述五种元素的基态原子中,未成对电子数为2的元素有________ (填元素符号)。
(4)基态b原子中有____ 种不同能量的电子;其基态 的核外电子占据的最高能级的电子云轮廓图呈
的核外电子占据的最高能级的电子云轮廓图呈_______ 形,该能级的轨道有_____ 个伸展方向。
(5)a元素的第二电离能____ (填“大于”或“小于”)b元素的第二电离能,原因是_____ 。
(2)c、d、e三种元素可形成一种有毒气体
 ,该气体分子的结构式为
,该气体分子的结构式为(3)上述五种元素的基态原子中,未成对电子数为2的元素有
(4)基态b原子中有
 的核外电子占据的最高能级的电子云轮廓图呈
的核外电子占据的最高能级的电子云轮廓图呈(5)a元素的第二电离能
您最近一年使用:0次
名校
解题方法
9 . 锂电池具有高能量密度和长寿命的特点,应用广泛。某种新型锂离子电池的电解质结构如图所示,其中短周期元素X、Y、Z、W处在同一周期,W元素形成的某种单质具有强氧化性,可用于杀菌消毒。下列说法正确的是
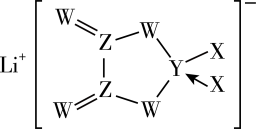
A.四种元素的原子半径: |
B.第一电离能: |
C.单质氧化性: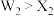 |
| D.阴离子中四种元素均满足8电子稳定结构 |
您最近一年使用:0次
2023-07-16更新
|
162次组卷
|
3卷引用:专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
(已下线)专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)福建省莆田市2022-2023学年高二下学期期末考试化学试题江西省萍乡市安源中学2022-2023学年高二下学期期中考试化学试题
名校
10 . 化合物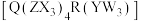 中X、Y、Z、W、Q、R的原子序数依次增大。X与Y、Z、W均能形成
中X、Y、Z、W、Q、R的原子序数依次增大。X与Y、Z、W均能形成 、
、 微粒,基态Q原子的3d轨道上有3个未成对电子,R被称为“海洋元素”,其原子序数等于W与Q的原子序数之和。下列说法错误的是
微粒,基态Q原子的3d轨道上有3个未成对电子,R被称为“海洋元素”,其原子序数等于W与Q的原子序数之和。下列说法错误的是
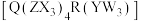 中X、Y、Z、W、Q、R的原子序数依次增大。X与Y、Z、W均能形成
中X、Y、Z、W、Q、R的原子序数依次增大。X与Y、Z、W均能形成 、
、 微粒,基态Q原子的3d轨道上有3个未成对电子,R被称为“海洋元素”,其原子序数等于W与Q的原子序数之和。下列说法错误的是
微粒,基态Q原子的3d轨道上有3个未成对电子,R被称为“海洋元素”,其原子序数等于W与Q的原子序数之和。下列说法错误的是A.化合物中Q的化合价为 |
| B.Y、Z、W中,第一电离能最大的是Z,电负性最大的是W |
| C.X、Z、W三种元素组成的化合物可能显酸性,也可能显碱性 |
| D.Y、Z、W、R分别与X形成的化合物中,沸点最高的是W对应的化合物 |
您最近一年使用:0次
2024-02-06更新
|
340次组卷
|
5卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题



