解题方法
1 . 下列各项比较中,正确的是
A.酸性: | B.电负性: |
C.沸点: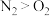 | D.中心原子孤电子对数: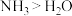 |
您最近一年使用:0次
2023-06-12更新
|
46次组卷
|
2卷引用:河北省邯郸市永年区第二中学2022-2023学年高二下学期6月月考化学试题
解题方法
2 . 镍具有良好的导磁性和可塑性,主要用于制作合金及催化剂。请回答下列问题
(1)基态镍原子的价电子排布图为____ ,同周期元素中基态原子与镍具有相同未成对电子的还有____ 种。
(2)四羰基合镍是一种无色挥发性液体,熔点-25℃,沸点43℃。则四羟基合镍中σ键和π键数目之比为___ 三种组成元素按电负性由大到小的顺序为____ 。
(3)[Ni(NH3)
4]SO4中N原子的杂化方式为____ ,写出与SO42-互为等电子体的一种分子和一种离子的化学式____ ,____ ;[Ni(
NH3)4]SO4中H-N-H键之间的夹角___ (填“>”“<”或“=”)NH3分子中H-N-H键之间的夹角。
(4)已知NiO的晶体结构(如图1),可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中,则NiO晶体中原子填充在氧原子形成的____ 体空隙中,其空隙的填充率为____ 。
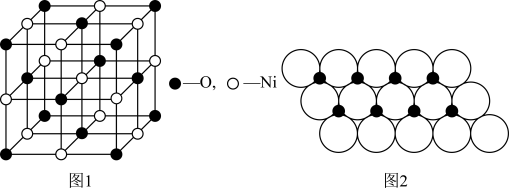
(5)一定温度下,NiO晶体可分散形成“单分子层”,O2-作单层密置排列,Ni2+填充O2-形成的正三角形空隙中(如图2),已知O2-的半径为αm,每平方米面积上分数的NiO的质量为___ g。(用a、NA表示)
(1)基态镍原子的价电子排布图为
(2)四羰基合镍是一种无色挥发性液体,熔点-25℃,沸点43℃。则四羟基合镍中σ键和π键数目之比为
(3)[Ni(NH3)
4]SO4中N原子的杂化方式为
NH3)4]SO4中H-N-H键之间的夹角
(4)已知NiO的晶体结构(如图1),可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中,则NiO晶体中原子填充在氧原子形成的

(5)一定温度下,NiO晶体可分散形成“单分子层”,O2-作单层密置排列,Ni2+填充O2-形成的正三角形空隙中(如图2),已知O2-的半径为αm,每平方米面积上分数的NiO的质量为
您最近一年使用:0次
名校
3 . 锰及其化合物用途非常广泛。回答下列问题:
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是___________ 。
(2)基态Mn原子的价电子排布式为_________ ,未成对电子数为_____ 个。
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是____________ 。
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为________ 。
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是_____ ,该分子中碳原子的杂化方式为_______ ;C、H、N的电负性从大到小的顺序为________ 。
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是_________ 。
(6)某种含锰特殊材料的晶胞结构如下图所示:
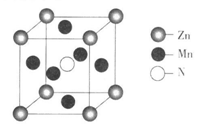
若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为____ ( 列出代数式即可)。
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是
(2)基态Mn原子的价电子排布式为
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是
(6)某种含锰特殊材料的晶胞结构如下图所示:

若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为
您最近一年使用:0次
2018-05-17更新
|
388次组卷
|
2卷引用:河北省石家庄精英中学2020-2021学年高二下学期期末考试化学试题
名校
解题方法
4 . 下列选项中的各组元素 从左到右
从左到右 同时满足下列三个条件的是 ( )
同时满足下列三个条件的是 ( )
a.原子半径依次减小;b.第一电离能逐渐升高;c.电负性逐渐增大。
 从左到右
从左到右 同时满足下列三个条件的是 ( )
同时满足下列三个条件的是 ( )a.原子半径依次减小;b.第一电离能逐渐升高;c.电负性逐渐增大。
| A.Na、Mg、Al | B.C、O、N | C. Li、Na、K | D.I、Cl、F |
您最近一年使用:0次
2020-02-11更新
|
150次组卷
|
4卷引用:河北省石家庄市第一中学2020-2021学年高二下学期学情反馈(一)化学试题
解题方法
5 . 已知X.Y元素同周期,且电负性X>Y,下列说法错误的是
| A.X与Y形成化合物时,X显负价,Y显正价 |
| B.第一电离能Y不一定大于X |
| C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性 |
| D.气态氢化物的稳定性:HmY小于HmX |
您最近一年使用:0次
名校
解题方法
6 . 一种可用作有机化工原料的化合物Q的结构如图。已知X、Y、Z、W、M为原子序数依次增大的主族元素,其中X的核电荷数等于其主族序数,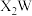 是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
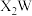 是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是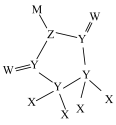
| A.原子半径:W>Z>Y | B.第一电离能:Z>W>Y |
| C.电负性:M>W>Z | D.键角: |
您最近一年使用:0次
2024-05-22更新
|
163次组卷
|
4卷引用:2024届河北省保定市十校高三下学期三模化学试题
解题方法
7 . 聚乙二醇(PEG)有良好的生物相容性,在水中可与 形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是
形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是

 形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是
形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是
A.PEG中 和 和 的杂化方式相同 的杂化方式相同 | B. 的VSEPR模型为四面体形 的VSEPR模型为四面体形 |
C.键角: | D.电负性: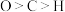 |
您最近一年使用:0次
8 . 回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是________ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)①在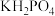 的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是________ (填离子符号)。
②原子中运动的电子有两种相反的自旋状态,若一种自旋状态用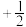 表示,与之相反的用
表示,与之相反的用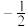 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为________ 。
(1)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为

B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)①在
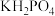 的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是②原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
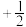 表示,与之相反的用
表示,与之相反的用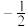 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
您最近一年使用:0次
名校
9 . 分子结构决定分子的性质,下列关于分子结构与性质的说法正确的是
| A.乙醚是非极性分子,乙醇是极性分子,因此乙醚在水中的溶解度比乙醇小 |
B.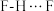 中的氢键键能小于 中的氢键键能小于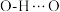 ,因此 ,因此 的沸点比 的沸点比 高 高 |
| C.从葡萄中提取的酒石酸盐具有光学活性,因此酒石酸盐中含有手性碳原子 |
D.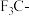 是吸电子基团, 是吸电子基团,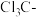 是推电子基团,因此 是推电子基团,因此 的酸性强于 的酸性强于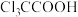 |
您最近一年使用:0次
解题方法
10 . X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y原子的电子总数是内层电子数的4倍,Y和R同主族,Y和Z最外层电子数之和与W的最外层电子数相同。25℃时,0.1mol/L X和W形成化合物的水溶液pH=1.下列说法正确的是
| A.电负性:Y>W>R>Z |
| B.Y、Z、W三种元素组成的化合物的水溶液一定显碱性 |
| C.简单离子的半径:R>W>Y>Z |
| D.因X与Y组成的分子间存在氢键,所以X与Y组成的分子比X与R组成的分子稳定 |
您最近一年使用:0次



