名校
解题方法
1 . GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]____________ ;下列状态的铝元素中,电离最外层的一个电子所需能量最小的是______________ (填标号)。
A.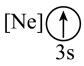 B.
B.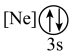 C.
C.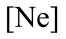 D.
D.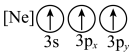
(2)8—羟基喹啉合铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与 8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为
8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为______________ ; 8—羟基喹啉合铝中所含元素电负性最大的是______________ (填元素符号,下同),第一电离能最大的是__________ (填元素符号),N原子的杂化方式为_____________ 。
(3)已知下列化合物的熔点:
①表格中卤化物的熔点产生差异的原因是_______________________________________________ 。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6分子,分子中每个原子最外层均达到8电子,二聚体Al2Cl6的结构式为______________________________ ;其中Al的配位数为_________ 。
(1)基态As原子核外电子排布式为[Ar]
A.
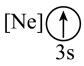 B.
B.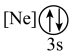 C.
C.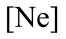 D.
D.
(2)8—羟基喹啉合铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与
 8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为
8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为(3)已知下列化合物的熔点:
| 化合物 | AlF3 | GaF3 | AlCl3 |
| 熔点/℃ | 1040 | 1000 | 194 |
①表格中卤化物的熔点产生差异的原因是
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6分子,分子中每个原子最外层均达到8电子,二聚体Al2Cl6的结构式为
您最近一年使用:0次
2019-12-18更新
|
222次组卷
|
2卷引用:福建省南安第一中学2020届高三上学期第二次月考化学试题
解题方法
2 . I.尿素[CO(NH2)2]是人工合成的第一种有机物。
(1)尿素中所含元素的电负性最大的是________ ,尿素分子间的氢键可表示为_____ 。
(2)尿素可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3。
①与铁同周期且未成对电子数与Fe3+相同的元素是________ 。
②[Fe(H2NCONH2)6](NO3)3中不存在 的化学键____________ (填序号)。
A离子键B金属键C配位键Dσ键Eπ键
③NO3-中N原子杂化后的价电子排布图为_______ ,NO3-的空间构型为________ 。
II.Mg2NiH4是一种贮氢的金属氢化物
(3)Mg2NiH4可通过氢化镁和镍单质球磨制成。在Mg2NiH4晶胞中,Ni原子占据如图的顶点和面心,Mg2+处于图八个小立方体的体心。
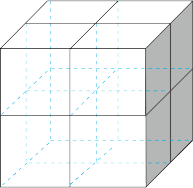
①Mg2NiH4中H的化合价为______ 。
②Mg2+位于Ni原子形成的___________ (填“八面体空隙”或“四面体空隙”)。
③若晶体的密度为dg·cm-3,Mg2NiH4的摩尔质量为Mg·mol-1,则Mg2+和Ni原子的最短距离为___________ nm(用含d、M的代数式表示)。
(1)尿素中所含元素的电负性最大的是
(2)尿素可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3。
①与铁同周期且未成对电子数与Fe3+相同的元素是
②[Fe(H2NCONH2)6](NO3)3中
A离子键B金属键C配位键Dσ键Eπ键
③NO3-中N原子杂化后的价电子排布图为
II.Mg2NiH4是一种贮氢的金属氢化物
(3)Mg2NiH4可通过氢化镁和镍单质球磨制成。在Mg2NiH4晶胞中,Ni原子占据如图的顶点和面心,Mg2+处于图八个小立方体的体心。

①Mg2NiH4中H的化合价为
②Mg2+位于Ni原子形成的
③若晶体的密度为dg·cm-3,Mg2NiH4的摩尔质量为Mg·mol-1,则Mg2+和Ni原子的最短距离为
您最近一年使用:0次
名校
解题方法
3 . 铁触媒是重要的催化剂,铁触媒在500 ℃左右时的活性最大,这也是合成氨反应一般选择在500 ℃左右进行的重要原因之一。CO易与铁触媒作用导致其失去催化活性:Fe+5CO===Fe(CO)5;在溶液中除去CO的化学方程式为[Cu(NH3)2]OOCCH3+CO+NH3 = 刹[Cu(NH3)3(CO)]OOCCH3。请回答下列问题:
(1)基态Fe原子的核外电子排布式为[Ar]___ ;C、N、O的电负性由大到小的顺序为______ 。
(2)Cu2+在水中呈现蓝色是因为形成了四水合铜(Ⅱ)离子,其化学式为______ ;配合物[Cu(NH3)2]OOCCH3中,铜显___ 价,碳原子的杂化轨道类型是______ ,NH3价电子对互斥理论模型是______ 。
(3)用[Cu(NH3)2]OOCCH3溶液除去CO的反应中,肯定有________ (填字母)形成。
A.离子键 B.配位键 C.非极性键 D.σ键
(4)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是________ 。
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为________ ,面心立方堆积与体心立方堆积的两种铁晶体的密度之比为________ (写出已化简的比例式即可)。(两种堆积中最邻近的铁原子的核间距相等)

(1)基态Fe原子的核外电子排布式为[Ar]
(2)Cu2+在水中呈现蓝色是因为形成了四水合铜(Ⅱ)离子,其化学式为
(3)用[Cu(NH3)2]OOCCH3溶液除去CO的反应中,肯定有
A.离子键 B.配位键 C.非极性键 D.σ键
(4)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为

您最近一年使用:0次
2019-05-07更新
|
428次组卷
|
2卷引用:【校级联考】福建省莆田第一中学、第四中学2019届高三下学期一模理科综合化学试题
名校
解题方法
4 . 氯磺酰氰酯(结构简式为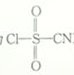 )是一种多用途的有机合成试剂,在HClO4-NaClO4介质中, K5[Co3+O4W12O36](简写为Co3+W)可催化合成氯磺酰氰酯。
)是一种多用途的有机合成试剂,在HClO4-NaClO4介质中, K5[Co3+O4W12O36](简写为Co3+W)可催化合成氯磺酰氰酯。
(2)氯磺酰氰酯分子中硫原子和碳原子的杂化轨道类型分别是
(3)ClO4-的空间构型为
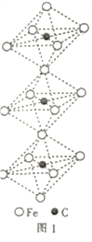
(4)一种由铁、碳形成的间隙化合物的晶体结构如图1所示,其中碳原子位于铁原子形成的八面体的中心,每个铁原子又为两个八面体共用,则该化合物的化学式为
您最近一年使用:0次
2018-05-25更新
|
267次组卷
|
3卷引用:【全国省级联考】福建省百校2018届高三下学期临考冲刺检测化学试题
5 . 下表是前20号元素中的部分元素的一些数据:
试回答下列问题:
(1)以上10种元素电负性最大的是_____ (填元素符号)。比元素B原子序数大7的元素在元素周期表中的位置:第_____ 周期,第_____ 族,其基态原子的核外电子排布式是________ 。
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)__________ 。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其分子中共形成________ 个σ键,________ 个π键。
(4)I与氢元素形成的10电子分子X的空间构型为________ ;将X溶于水后的溶液滴入到CuSO4溶液中至过量,得到的络离子的化学式为________ ,其中X与Cu2+之间以_____________ 键结合。
(5)下图是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a._________________________________ 。
b._________________________________ 。

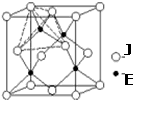
(6)如图是J和E组成的晶体结构,则每个与J周围最近J原子数目为_________ ,若晶胞边长为a cm,则晶体的密度为_______________ (用含a、NA的代数式表示)(g/mL)。
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)以上10种元素电负性最大的是
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其分子中共形成
(4)I与氢元素形成的10电子分子X的空间构型为
(5)下图是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a.
b.

(6)如图是J和E组成的晶体结构,则每个与J周围最近J原子数目为

您最近一年使用:0次
2017-12-20更新
|
310次组卷
|
3卷引用:2020届高三化学二轮选修大题必练—— 物质结构与性质大题练
6 . 科学家正在研究温室气体CH4和CO2的转化和利用。
(1)CH4和CO2所含的三种元素电负性从小到大的顺序为______ 。
(2)下列关于CH4和CO2的说法正确的是______ (填序号)。
a.固态CO2属于分子晶体
b. CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的电子排布式为____________ ,Ni该元素位于元素周期表的第___ 族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有_____ molσ键。
(4)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表.CH4与H2O形成的水合物俗称“可燃冰”。


①“可燃冰”中分子间存在的2种作用力是______ 。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想.已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________________________ 。
(1)CH4和CO2所含的三种元素电负性从小到大的顺序为
(2)下列关于CH4和CO2的说法正确的是
a.固态CO2属于分子晶体
b. CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的电子排布式为
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1mol Ni(CO)4中含有
(4)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表.CH4与H2O形成的水合物俗称“可燃冰”。


①“可燃冰”中分子间存在的2种作用力是
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想.已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
您最近一年使用:0次
2016-12-09更新
|
1727次组卷
|
3卷引用:2015年全国普通高等学校招生统一考试化学(福建卷)



