名校
1 . 过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一、
(1)锌化铜是一种金属互化物,元素铜的第二电离能___________ (填“大于”“小于”或“等于”)锌的第二电离能,理由是___________ 。
(2)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为(CH3)2SO。(CH3)2SO中C—S—O的键角___________ (填“大于”“小于”或“等于”)CH3COCH3中C—C—O的键角,理由是___________ ;元素S、Cl、O的电负性由大到小的顺序为___________ 。
(3)利用CuSO4和NaOH制备的Cu(OH)2悬浊液检验醛基时,生成砖红色的Cu2O,其晶胞结构如图所示。

该晶胞原子分数坐标A为(0,0,0),C为( ,
, ,
, ),则D原子分数坐标为
),则D原子分数坐标为___________ 。
②若Cu2O晶体密度为d g·cm-3,晶胞参数为a pm,则阿伏加德罗常数的值NA为___________ (用含d和a的式子表示)。
(1)锌化铜是一种金属互化物,元素铜的第二电离能
(2)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为(CH3)2SO。(CH3)2SO中C—S—O的键角
(3)利用CuSO4和NaOH制备的Cu(OH)2悬浊液检验醛基时,生成砖红色的Cu2O,其晶胞结构如图所示。

该晶胞原子分数坐标A为(0,0,0),C为(
 ,
, ,
, ),则D原子分数坐标为
),则D原子分数坐标为②若Cu2O晶体密度为d g·cm-3,晶胞参数为a pm,则阿伏加德罗常数的值NA为
您最近一年使用:0次
名校
解题方法
2 . 下列关于分子的结构和性质的描述错误的是
| A.碘易溶于四氯化碳溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
B.硫难溶于水,微溶于酒精,易溶于 ,说明分子极性: ,说明分子极性: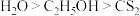 |
| C.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性 |
D.乙醇分子(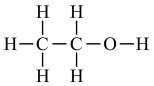 )中所有碳原子都是手性碳原子 )中所有碳原子都是手性碳原子 |
您最近一年使用:0次
名校
解题方法
3 . 下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。
(1)元素e位于周期表中______ 区,其基态原子核外有______ 种运动状态不同的电子。
(2)基态c原子中有______ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为______ 形
(3)b、c、d三种元素的第一电离能由大到小的顺序为______ (填元素符号);b、c、d三种元素中能形成氢键的是______ (填元素符号)。
(4)已知高温下化合物f2d比化合物fd更稳定,试从核外电子排布的角度解释原因______ 。

(1)元素e位于周期表中
(2)基态c原子中有
(3)b、c、d三种元素的第一电离能由大到小的顺序为
(4)已知高温下化合物f2d比化合物fd更稳定,试从核外电子排布的角度解释原因
您最近一年使用:0次
2024-01-02更新
|
83次组卷
|
2卷引用:北京市大兴区2022-2023学年大兴一中高二上学期期中考试(1+3学部)
4 . 在化学发展史上,许多科学家的研究成果对人类的进步和化学的发展做出了杰出的贡献,下列对科学家的主要成就描述不正确的是
| A | B | C | D |
 鲍林 |  泡利 |  范德华 |  门捷列夫 |
| 电负性:描述不同元素的原子对键合电子的吸引能力 | 泡利原理:一个原子轨道内最多容纳2个电子,且自旋平行 | 范德华力:分子之间存在相互作用力 | 元素周期律:元素性 质随着原子序数递增呈周期性的重复 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 下列说法中,正确的是
| A.s区元素全部是金属元素 |
| B.共价化合物中电负性大的成键元素表现为负价 |
| C.含有非极性键的分子一定是非极性分子 |
| D.非极性分子中一定含有非极性键 |
您最近一年使用:0次
名校
解题方法
6 . 前4周期主族元素X、Y、Z、W的原子序数依次增大。价层电子数满足Z=X+Y;原子半径X小于Y,Y是空气中含量最多的元素;基态Z原子的核外电子总数是其最高能级电子数的2倍;W的内层电子全排满,且第四能层的单电子只有1个。下列说法正确的是
| A.W位于元素周期表p区 | B.电负性X>Y |
C.X、Z形成的分子一定是 微粒 微粒 | D.W一定位于第IIIA族 |
您最近一年使用:0次
名校
解题方法
7 . 前四周期主族元素X、Y、Z、Q的原子序数依次增大,基态X原子核外电子占据两种形状不同的原子轨道,且两种轨道中电子总数相等,Q与X处于同一主族。Y的周期序数与族序数相等,Z的第二电离能远小于第三电离能。下列说法正确的是
A.电负性: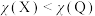 | B.最高价氧化物对应水化物的碱性: |
| C.Z的氯化物是工业漂白粉的有效成分 | D.X、Z只能形成一种离子化合物 |
您最近一年使用:0次
2023-12-30更新
|
216次组卷
|
2卷引用:江苏省射阳中学2023-2024学年高二上学期11月期中考试化学试题
名校
8 . 生成氢气:在恒温恒容的反应器中,将水蒸气通过红热的炭即产生水煤气: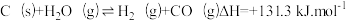 。
。
(1)以上涉及到的元素中,电负性最大的元素为_______。
(2)H2O的价层电子对空间结构为_______ (需过程)
(3)写出该反应的平衡常数表达式_______ 。
(4)下列能作为反应达到平衡的判据是_______。
(5)有利于提高H2平衡产率的条件是_______。
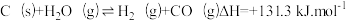 。
。(1)以上涉及到的元素中,电负性最大的元素为_______。
| A.碳 | B.氢 | C.氧 |
(3)写出该反应的平衡常数表达式
(4)下列能作为反应达到平衡的判据是_______。
| A.容器内气体的压强不变 |
| B.K值不变 |
| C.H2O和H2的物质的量之比不变 |
| D.CO和H2的物质的量之比不变 |
| A.低温低压 | B.低温高压 |
| C.高温低压 | D.高温高压 |
您最近一年使用:0次
名校
9 . 法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法正确的是


A.该分子的分子式为 |
B.该分子中相邻C原子之间均以 杂化轨道重叠形成σ键 杂化轨道重叠形成σ键 |
| C.组成该分子的所有元素中氟的电负性最大 |
| D.该分子中有2个手性碳原子 |
您最近一年使用:0次
名校
10 . 下表是某些短周期元素的电负性值:
(1)通过分析电负性值变化规律,确定 的电负性值范围:
的电负性值范围:_______ 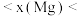
_______ 。
(2)推测 值与原子半径的关系是
值与原子半径的关系是_______ ;根据短周期元素的 值变化特点,体现了元素性质的
值变化特点,体现了元素性质的_______ 变化规律。
(3)分别指出下列两种化合物中氧元素的化合价:
_______ ,
_______ 。
(4)试推断 中化学键类型是
中化学键类型是_______ 。
(5)预测元素周期表中, 值最小的元素位于
值最小的元素位于_______ 周期_______ 族(放射性元素除外)。
| 元素符号 |  |  |  |  |  |  |  |  |  |  |  |  |
电负性值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析电负性值变化规律,确定
 的电负性值范围:
的电负性值范围: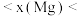
(2)推测
 值与原子半径的关系是
值与原子半径的关系是 值变化特点,体现了元素性质的
值变化特点,体现了元素性质的(3)分别指出下列两种化合物中氧元素的化合价:


(4)试推断
 中化学键类型是
中化学键类型是(5)预测元素周期表中,
 值最小的元素位于
值最小的元素位于
您最近一年使用:0次



