名校
1 . 现有六种元素A、B、C、D、E、F,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的轨道表示式为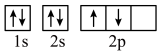 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(2)B元素的电负性___________ (填“大于”“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物的晶体类型为___________ 。
(4)E基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向。
(5)下列关于F原子的价电子轨道表示式是___________ 。
(6)基态Fe3+核外电子排布式为___________ 。过量单质F与B的最高价氧化物对应的水化物的稀溶液完全反应,生成BC气体,该反应的离子方程式为___________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素是地壳中含量最多的元素 |
| D元素原子的第一至第四电离能分别是:I1=738 kJ·mol-1;I2=1451 kJ·mol-1;I3=7733kJ·mol-1;I4=10540 kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
(1)某同学根据上述信息,推断A基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(2)B元素的电负性
(3)C与D形成的化合物的晶体类型为
(4)E基态原子中能量最高的电子,其电子云在空间有
(5)下列关于F原子的价电子轨道表示式是
(6)基态Fe3+核外电子排布式为
您最近一年使用:0次
名校
2 . 二硫代磷酸酯的分子结构如图所示。下列说法错误的是
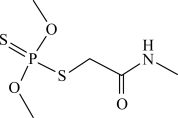
A.电负性: |
B.该分子中含有23个 键 键 |
C.该分子中碳原子的杂化方式为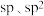 |
D.基态N原子价电子轨道表示式为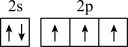 |
您最近一年使用:0次
2023-12-26更新
|
550次组卷
|
5卷引用:青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题
名校
解题方法
3 . 下列曲线表示第ⅦA族元素(F、 、I)性质随其质子数的变化趋势,错误的是
、I)性质随其质子数的变化趋势,错误的是
 、I)性质随其质子数的变化趋势,错误的是
、I)性质随其质子数的变化趋势,错误的是A.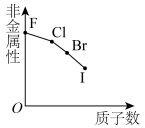 | B. |
C.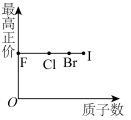 | D.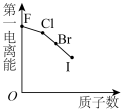 |
您最近一年使用:0次
2023-12-26更新
|
238次组卷
|
7卷引用:青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题
青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题(已下线)名校期中好题汇编-原子结构与性质(选择题)名校期中好题汇编-原子结构与性质(选择题)山东省菏泽市鄄城县第一中学2023-2024学年高二上学期1月期末化学试题江西省部分学校2023-2024学年高二上学期1月期末化学试题(已下线)1.2.2 元素周期律(基础)黑龙江省绥化市绥棱县第一中学2023-2024学年高二下学期开学化学试题
名校
解题方法
4 . 构成物质的微粒种类及相互间的作用力是影响物质性质的主要因素。
(1)已知:H与O可以形成H2O和H2O2两种化合物。
①H2O内O-H(a)、水分子间的范德华力(b)和氢键(c),从强到弱的顺序为______ 。(用a、b、c表示)。H+可与H2O形成H3O+,H3O+中H-O-H的键角比H2O中的大,原因是______ 。
②H2O2是常用的氧化剂,分子结构如图所示。
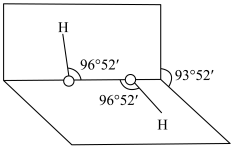
i.H2O2的电子式是______ 。
ii.下列关于H2O2的说法中正确的是______ (填序号)。。
a.分子中含有极性键和非极性键
b.氧原子的轨道发生了sp3杂化
c.分子是非极性分子
iii.H2O2易溶于水,难溶于CC14,主要原因是______ 。
(2)已知:在一定条件下,十八胺具有一定的还原性,不同的金属盐与十八胺体系反应可以得到不同的产物,产物的差异与金属离子获得电子的能力有关。
表1部分金属元素的电负性
表2单一金属盐与十八胺体系反应得到的产物
①请结合上述信息,分析不同的金属盐与十八胺体系反应得到不同类型产物的原因:Zn、Co、Ni元素电负性相对较小,获得电子的能力相对较弱,在反应中未发生元素化合价的变化,得到金属氧化物:______ 。
②Co2+和Pd2+盐混合后再与十八胺体系反应得到金属间化合物CoPd2.该化合物中Co原子与Pd原子间的作用力是______ (填“离子键”或“共价键”),依据表1信息写出判断理由______ 。
③Pt4+盐与十八胺体系的反应与上述反应类似。请推测单一Pt4+盐与十八胺体系的反应的产物是______ 。
(1)已知:H与O可以形成H2O和H2O2两种化合物。
①H2O内O-H(a)、水分子间的范德华力(b)和氢键(c),从强到弱的顺序为
②H2O2是常用的氧化剂,分子结构如图所示。

i.H2O2的电子式是
ii.下列关于H2O2的说法中正确的是
a.分子中含有极性键和非极性键
b.氧原子的轨道发生了sp3杂化
c.分子是非极性分子
iii.H2O2易溶于水,难溶于CC14,主要原因是
(2)已知:在一定条件下,十八胺具有一定的还原性,不同的金属盐与十八胺体系反应可以得到不同的产物,产物的差异与金属离子获得电子的能力有关。
表1部分金属元素的电负性
| 金属元素 | Zn | Co | Ni | Ag | Pd | Pt |
| 电负性 | 1.65 | 1.88 | 1.91 | 1.93 | 2.2 | 2.2 |
| 金属盐中的金属离子 | Zn2+ | Co2+ | Ni2+ | Ag+ | Pd2+ |
| 反应产物 | ZnO | CoO | NiO | Ag | Pd |
②Co2+和Pd2+盐混合后再与十八胺体系反应得到金属间化合物CoPd2.该化合物中Co原子与Pd原子间的作用力是
③Pt4+盐与十八胺体系的反应与上述反应类似。请推测单一Pt4+盐与十八胺体系的反应的产物是
您最近一年使用:0次
名校
解题方法
5 . 下列判断不正确的是
| A.电负性:P<S<Cl | B.沸点:Cl2<Br2<I2 |
| C.微粒半径:Li+<O2-<Na+ | D.键角:BF3>CH4>H2O |
您最近一年使用:0次
2023-12-25更新
|
180次组卷
|
2卷引用:北京市大兴区2022-2023学年大兴一中高二上学期期中考试(1+3学部)
名校
解题方法
6 .  、
、 、
、 、
、 为原子序数依次增大的同一短周期的主族元素,基态
为原子序数依次增大的同一短周期的主族元素,基态 原子
原子 轨道的电子总数与其
轨道的电子总数与其 轨道的电子总数相等,基态
轨道的电子总数相等,基态 原子
原子 层电子总数是内层电子总数的2倍,上述四种元素形成的阴离子的结构如图,下列说法正确的是
层电子总数是内层电子总数的2倍,上述四种元素形成的阴离子的结构如图,下列说法正确的是
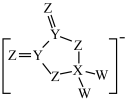
 、
、 、
、 、
、 为原子序数依次增大的同一短周期的主族元素,基态
为原子序数依次增大的同一短周期的主族元素,基态 原子
原子 轨道的电子总数与其
轨道的电子总数与其 轨道的电子总数相等,基态
轨道的电子总数相等,基态 原子
原子 层电子总数是内层电子总数的2倍,上述四种元素形成的阴离子的结构如图,下列说法正确的是
层电子总数是内层电子总数的2倍,上述四种元素形成的阴离子的结构如图,下列说法正确的是
A.第一电离能: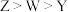 | B.最简单氢化物的沸点: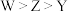 |
C. 为金属元素 为金属元素 | D.电负性: |
您最近一年使用:0次
名校
解题方法
7 . 前四周期元素 的原子序数依次增大,
的原子序数依次增大, 原子中有6个运动状态不同的电子,
原子中有6个运动状态不同的电子, 是地壳中含量最多的元素,基态
是地壳中含量最多的元素,基态 原子
原子 层上的电子总数是
层上的电子总数是 原子轨道上电子数的两倍,基态
原子轨道上电子数的两倍,基态 原子中有6个未成对电子。下列说法正确的是
原子中有6个未成对电子。下列说法正确的是
 的原子序数依次增大,
的原子序数依次增大, 原子中有6个运动状态不同的电子,
原子中有6个运动状态不同的电子, 是地壳中含量最多的元素,基态
是地壳中含量最多的元素,基态 原子
原子 层上的电子总数是
层上的电子总数是 原子轨道上电子数的两倍,基态
原子轨道上电子数的两倍,基态 原子中有6个未成对电子。下列说法正确的是
原子中有6个未成对电子。下列说法正确的是A.电负性: ;氢化物的熔、沸点: ;氢化物的熔、沸点: |
B.一定条件下, 与氢元素形成的某些化合物与 与氢元素形成的某些化合物与 的单质及氢化物均能反应 的单质及氢化物均能反应 |
C.同周期中,元素 的第一电离能最大 的第一电离能最大 |
D.同周期中,基态时,与 原子最外层电子数相同的元素有1种 原子最外层电子数相同的元素有1种 |
您最近一年使用:0次
名校
解题方法
8 . 下列关于分子的结构和性质的描述中,正确 的是
| A.对羟基苯甲醛的熔点比邻羟基苯甲醛的熔点低 |
| B.氨分子间有氢键,故气态氨分子的热稳定性比水蒸气的高 |
| C.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
| D.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性 |
您最近一年使用:0次
名校
解题方法
9 . “液态阳光”项目通过太阳能电解水制氢,再采用催化剂将二氧化碳加氢合成甲醇。高选择性催化剂的组成为 固溶体。四方体
固溶体。四方体 晶胞如图所示,回答下列问题:
晶胞如图所示,回答下列问题:
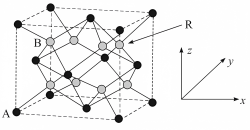
(1)图示晶胞中A代表___________ (填“ ”或“
”或“ ”)原子。
”)原子。
(2) 在元素周期表中的位置
在元素周期表中的位置___________ ,第二电离能:
___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(3)关于 分子:
分子:
① 的电子式为
的电子式为___________ , 是
是___________ 分子(填“极性”或“非极性”)。
②H、C、N、O四种元素的电负性由大到小的顺序为___________ (用元素符号表示)。
③甲醇的沸点(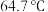 )介于水(
)介于水( )和甲硫醇(
)和甲硫醇( ,
,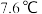 )之间,其原因是
)之间,其原因是___________ 。
(4)该晶胞中原子坐标参数 为
为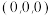 ,则
,则 的原子坐标参数为
的原子坐标参数为___________ 。
(5)晶胞参数为长 、宽
、宽 、高
、高 ,晶体密度为
,晶体密度为___________  (写出计算式即可,其中阿伏加德罗常数数值为
(写出计算式即可,其中阿伏加德罗常数数值为 )。
)。
 固溶体。四方体
固溶体。四方体 晶胞如图所示,回答下列问题:
晶胞如图所示,回答下列问题:
(1)图示晶胞中A代表
 ”或“
”或“ ”)原子。
”)原子。(2)
 在元素周期表中的位置
在元素周期表中的位置
 (填“大于”或“小于”)。
(填“大于”或“小于”)。(3)关于
 分子:
分子:①
 的电子式为
的电子式为 是
是②H、C、N、O四种元素的电负性由大到小的顺序为
③甲醇的沸点(
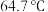 )介于水(
)介于水( )和甲硫醇(
)和甲硫醇( ,
,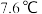 )之间,其原因是
)之间,其原因是(4)该晶胞中原子坐标参数
 为
为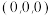 ,则
,则 的原子坐标参数为
的原子坐标参数为(5)晶胞参数为长
 、宽
、宽 、高
、高 ,晶体密度为
,晶体密度为 (写出计算式即可,其中阿伏加德罗常数数值为
(写出计算式即可,其中阿伏加德罗常数数值为 )。
)。
您最近一年使用:0次
名校
解题方法
10 . 有机化合物 和
和 发生水解时的主要反应分别是
发生水解时的主要反应分别是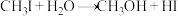 和
和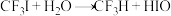 ,下列说法正确的是
,下列说法正确的是
 和
和 发生水解时的主要反应分别是
发生水解时的主要反应分别是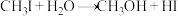 和
和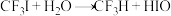 ,下列说法正确的是
,下列说法正确的是| A.电负性:F>O>C>H |
| B.可用乙醇萃取碘水中的碘 |
C.F元素的最高价氧化物对应的水化物的化学式: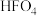 |
| D.H元素和I元素之间通过离子键形成HI |
您最近一年使用:0次



