解题方法
1 . X、Y、Z、R、Q是原子序数依次增大的短周期主族元素,其中基态X的最高能层中含有一个空轨道;同周期主族元素中只有两种元素的第一电离能大于Z;五种元素可形成某种离子液体阴离子的结构如下图所示。错误 的是

A.离子半径: | B.简单氢化物的沸点: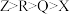 |
C.该阴离子中原子的价层孤电子对数: | D.电负性: |
您最近一年使用:0次
2 . 有机物M由原子序数依次增大的短周期主族非金属元素W、X、Y、Z组成,基态Y原子含有2个未成对电子,Z的原子序数是Y的2倍。M的质谱图如下。下列说法正确的是
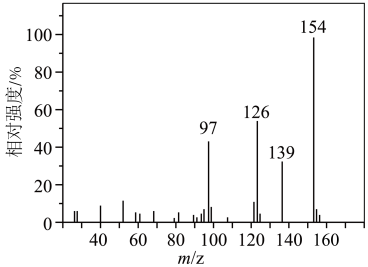
| A.原子半径:Z>Y>X>W | B.M的相对分子质量为154 |
C. : :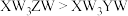 | D.X、Y、Z的最简单氢化物均为极性分子 |
您最近一年使用:0次
名校
3 . 下列说法错误的是
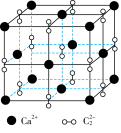
| A.CO2与SiO2的键角相等 |
| B.SiH4、CO2均是由极性键构成的非极性分子 |
| C.HCNO中元素的电负性:O>N>C>H |
| D.CaC2晶胞如图所示,Ca2+的配位数为6 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
| A.某金属元素M气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703…,当它与氯气反应时生成MCl3 |
| B.硫酸酸性强于亚硫酸的原因是硫酸分子中非羟基氧的个数多 |
C.CCl4分子中所有原子的最外层电子都满足了 稳定结构 稳定结构 |
D. 和CH4含有的共价键都是 和CH4含有的共价键都是 |
您最近一年使用:0次
名校
解题方法
5 . A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,相关信息如下表:
请用化学用语填空:
(1)A元素在元素周期表中的位置___________ ;C元素和F元素的电负性比较,较小的是___________ (填元素符号)。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为___________ ,B元素所形成的单质分子中σ键与π键数目之比为___________ 。
(3)F元素原子的价电子的轨道表示式是___________ ;G的高价阳离子的溶液与H单质反应的离子方程式为___________ ;元素X与元素E在周期表中呈对角线关系,且元素X的最高价氧化物的水化物也具有两性,试写出X元素的最高价氧化物的水化物与D元素的最高价氧化物的水化物反应的化学方程式___________ 。
| 元素 | 元素相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
(1)A元素在元素周期表中的位置
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为
(3)F元素原子的价电子的轨道表示式是
您最近一年使用:0次
解题方法
6 . 恩格列净是治疗2型糖尿病的一种原料药,其关键中间体(F)的合成路线如下:
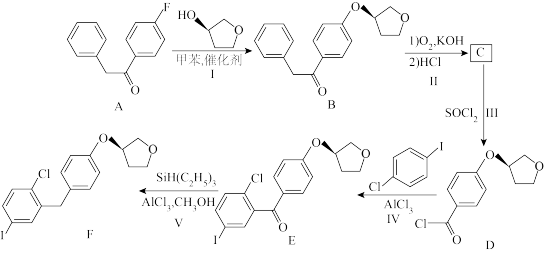
已知: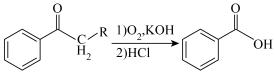 +RCOOH
+RCOOH
回答下列问题:
(1)B分子含有的官能团名称为
(2)反应Ⅰ在
(3)反应Ⅱ生成两种有机物,一种为C,另一种产物的结构简式为
(4)
 易水解:
易水解: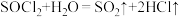 。反应Ⅲ的化学方程式为
。反应Ⅲ的化学方程式为(5)V的反应类型为
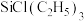 ,若反应中Si的化合价不变,则
,若反应中Si的化合价不变,则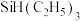 中三种元素按电负性由大到小排列为
中三种元素按电负性由大到小排列为(6)芳香族化合物G是C的同分异构体,请写出符合下列条件的G的结构简式
①能与 溶液反应产生气体
溶液反应产生气体
②核磁共振氢谱有四组峰且峰面积比为6∶3∶2∶1。
您最近一年使用:0次
名校
解题方法
7 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
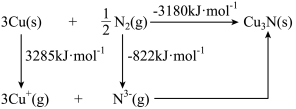
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
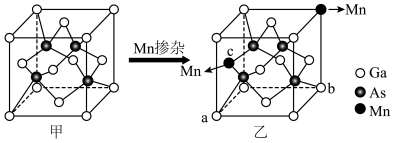
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近一年使用:0次
名校
解题方法
8 . 酞菁和酞菁钴可制得光动力学中的光敏剂,分子结构如图,其中酞菁分子中所有原子共平面,下列说法正确的是
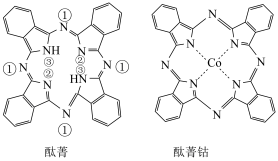
| A.酞菁钴中钴的化合价为+4 |
| B.直径为1.5×10–9 m的酞菁钴分子能透过半透膜 |
| C.酞菁钴中元素的电负性由大到小的顺序为N>C>H>Co |
| D.标注①②的N原子的杂化方式是sp2,③的N原子的杂化方式是sp3 |
您最近一年使用:0次
2024-03-13更新
|
483次组卷
|
2卷引用:福建省厦门第一中学2023-2024学年高三下学期2月第一次月考化学试卷
名校
9 . 某电池的电解液部分微观结构如图,“---”表示微粒间存在较强静电作用。M、N、W、X、Y、Z为原子序数依次增大的短周期元素。下列说法错误的是
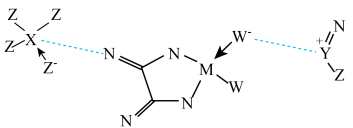
A.未成对电子数: | B.电负性: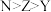 |
C.最简单氢化物的沸点: | D.熔点: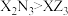 |
您最近一年使用:0次
2024-03-07更新
|
342次组卷
|
2卷引用:福建省厦门市2024届高三下学期第二次质检化学试题
名校
10 . 下列比较中,正确的是
| A.第一电离能:Na<Mg<Al | B.电负性:Cl>S>As |
| C.原子半径:O>F>Na | D.最高正化合价:F>S>N |
您最近一年使用:0次
2024-03-01更新
|
147次组卷
|
3卷引用:福建省漳州市华安县第一中学2023-2024学年高二下学期3月月考化学试题



