解题方法
1 . 中国科学家团队成功合成了五氮阴离子盐 。五氮阴离子(
。五氮阴离子(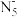 )为环状平面结构,是制备全氮类物质
)为环状平面结构,是制备全氮类物质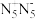 的中间体。
的中间体。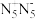 是新一代超高能含能材料下列说法正确的是
是新一代超高能含能材料下列说法正确的是
 。五氮阴离子(
。五氮阴离子(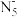 )为环状平面结构,是制备全氮类物质
)为环状平面结构,是制备全氮类物质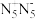 的中间体。
的中间体。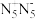 是新一代超高能含能材料下列说法正确的是
是新一代超高能含能材料下列说法正确的是
| A.阴阳离子之间作用力只存在离子键 | B.五氮阴离子盐中N、O两种元素均为sp3杂化 |
| C.电负性:N>O>H | D.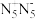 可以作炸药、推进剂 可以作炸药、推进剂 |
您最近一年使用:0次
2 . 氮氧化物会导致光化学烟雾和酸雨,在 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是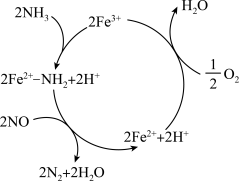
A.基态 的价层电子排布式为 的价层电子排布式为 |
| B.电负性:N>O>H>Fe |
| C.该过程中存在极性键和非极性键的断裂和形成 |
D.图中的总反应可表示为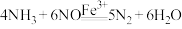 |
您最近一年使用:0次
2024-02-25更新
|
267次组卷
|
5卷引用:福建省福州第三中学2023-2024学年高三上学期第五次质量检测化学试题
名校
解题方法
3 . 一种由W、X、Y、Z、Q五种短周期主族元素组成的离子结构如图所示,其中X、Q同主族,Y的基态原子s轨道电子数是p轨道的2倍,且W、X、Z原子序数之和为15.下列说法正确的是
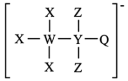
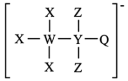
A.电负性: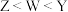 |
B.最高价氧化物对应水化物的酸性: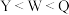 |
C.阴离子还原性: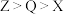 |
| D.X与Z形成的化合物沸点一定高于Y与Z形成的化合物沸点 |
您最近一年使用:0次
解题方法
4 . 四种短周期主族元素在元素周期表中的相对位置如图所示,且X、Y、Z和Q四种元素的p轨道电子总数为24。化学家鲍林以Y的电负性作为参照标准,得出了各元素的电负性。下列叙述错误的是
| X | Y | |||
| Z | Q |
| A.最简单氢化物的稳定性:Y>Q>Z |
B. 分子中每个原子最外层都达到8电子稳定结构 分子中每个原子最外层都达到8电子稳定结构 |
| C.最高价氧化物对应水化物的酸性: Z<Q |
D.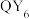 分子呈正八面体形 分子呈正八面体形 |
您最近一年使用:0次
2023-10-28更新
|
337次组卷
|
2卷引用:福建省宁德市部分达标学校2023-2024学年高三上学期期中考试化学试题
名校
解题方法
5 . 咔唑(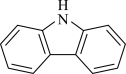 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是
 )是一种新型有机液体储氢介质。下列说法错误的是
)是一种新型有机液体储氢介质。下列说法错误的是| A.电负性:N>C>H |
| B.同周期元素中第一电离能小于N的有4种 |
C.咔唑的沸点比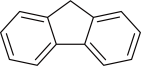 的沸点高 的沸点高 |
D.基态氮原子的外围电子轨道表示式不能写为 ,因为违背了洪特规则原理 ,因为违背了洪特规则原理 |
您最近一年使用:0次
2023-09-22更新
|
121次组卷
|
3卷引用:福建省泉州市部分中学2022-2023学年高二下学期期末联考化学试题
名校
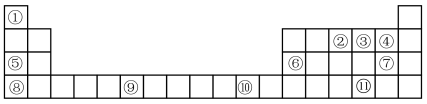
6 . 表格为门捷列夫元素周期表的一部分,其中的编号代表对应的元素。用元素符号回答下列问题:
(1)基态F原子有___________ 种运动状态的电子。
(2)元素③⑪电负性较大的是___________ ;Se的原子结构示意图为___________ 。
(3)元素铬的基态原子的价电子排布图为:___________ 。
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为___________ 。
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为________ 。
(6)②③的简单气态氢化物中较稳定的是___________ (填化学式),元素⑥⑦的最高价氧化物的水化物相互反应的离子方程式为___________ 。
(1)基态F原子有
(2)元素③⑪电负性较大的是
(3)元素铬的基态原子的价电子排布图为:
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为
(6)②③的简单气态氢化物中较稳定的是
您最近一年使用:0次
2023-09-16更新
|
254次组卷
|
2卷引用:福建省龙岩市连城县第一中学2022-2023学年高二下学期3月月考化学试题
7 . 现有四种元素基态原子的电子排布式如下。则下列有关比较中不正确的是
①1s22s22p5②1s22s22p3③1s22s22p63s23p4④1s22s22p63s23p3
①1s22s22p5②1s22s22p3③1s22s22p63s23p4④1s22s22p63s23p3
| A.电负性:①>②>③>④ |
| B.第一电离能:①>②>③>④ |
| C.原子半径:④>③>②>① |
| D.②、③的简单氢化物,中心原子均为sp3杂化,且均为极性分子 |
您最近一年使用:0次
解题方法
8 . 钛及其化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)Ti(BH4)3是一种储氢材料。BH 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为___ ;Ti、B、H元素的电负性由大到小排列顺序为_____ 。
(2)已知Ti3+易形成多种配合物,[TiCl(H2O)5]Cl2·H2O是其中的一种。
①1mol该配合物中含有_______ molσ键。
②Ti3+具有较强还原性的原因是___________ 。
(3)研究表明,TiO2通过氮掺杂反应可生成TiO2-xNy,能使TiO2对可见光具有活性,反应如图所示。
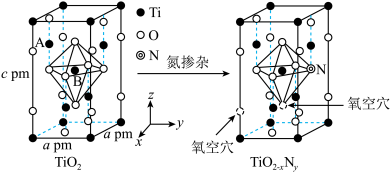
①上图TiO2晶胞中钛原子占据___________ 个氧原子围成的八面体空隙。
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为( ,
, ,
, ),则A点原子的分数坐标为(
),则A点原子的分数坐标为( ,0,
,0,___________ )。
③TiO2-xNy晶体中x=___________ 。
(1)Ti(BH4)3是一种储氢材料。BH
 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为(2)已知Ti3+易形成多种配合物,[TiCl(H2O)5]Cl2·H2O是其中的一种。
①1mol该配合物中含有
②Ti3+具有较强还原性的原因是
(3)研究表明,TiO2通过氮掺杂反应可生成TiO2-xNy,能使TiO2对可见光具有活性,反应如图所示。

①上图TiO2晶胞中钛原子占据
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为(
 ,
, ,
, ),则A点原子的分数坐标为(
),则A点原子的分数坐标为( ,0,
,0,③TiO2-xNy晶体中x=
您最近一年使用:0次
名校
解题方法
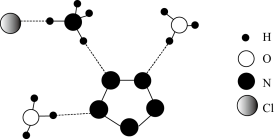
9 . 阴离子 和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
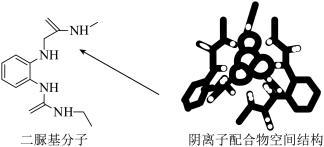
 和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
A.所含元素电负性最大的是 |
| B.二脲基分子中所有碳原子不可能共平面 |
C. 离子与 离子与 离子的空间结构不同 离子的空间结构不同 |
D.二脲基分子中 的 的 和 和 离子的 离子的 形成氢键 形成氢键 |
您最近一年使用:0次
10 . 实验室用邻二氮菲(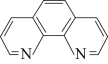 )与
)与 形成的红色配合离子(图1)测定
形成的红色配合离子(图1)测定 的浓度。回答下列问题:
的浓度。回答下列问题:

(1)Fe元素在周期表中的位置为__________ ,该配合物中心离子的配位数为__________ 。
(2)该配合离子所含元素的电负性最大的是__________ ,C原子的杂化方式为__________ 。
(3)该配合离子存在的化学键类型有__________ 。
a.离子键 b.配位键 c.极性键 d.非极性键 e.金属键 f.氢键
(4)从结构角度分析, 易被氧化成
易被氧化成 的原因是
的原因是__________ 。
(5)合成氨反应中铁催化剂表面吸附氮原子,图2为氮原子在铁的晶面上的单层附着局部示意图,图中铁原子与氮原子的个数比为__________ 。
(6)铁晶体中的原子堆积方式如图3所示, 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为 ,若晶胞密度为
,若晶胞密度为 ,则
,则
__________ (列出表达式)。
 )与
)与 形成的红色配合离子(图1)测定
形成的红色配合离子(图1)测定 的浓度。回答下列问题:
的浓度。回答下列问题:
(1)Fe元素在周期表中的位置为
(2)该配合离子所含元素的电负性最大的是
(3)该配合离子存在的化学键类型有
a.离子键 b.配位键 c.极性键 d.非极性键 e.金属键 f.氢键
(4)从结构角度分析,
 易被氧化成
易被氧化成 的原因是
的原因是(5)合成氨反应中铁催化剂表面吸附氮原子,图2为氮原子在铁的晶面上的单层附着局部示意图,图中铁原子与氮原子的个数比为
(6)铁晶体中的原子堆积方式如图3所示,
 表示阿伏加德罗常数的值,晶胞参数为
表示阿伏加德罗常数的值,晶胞参数为 ,若晶胞密度为
,若晶胞密度为 ,则
,则
您最近一年使用:0次



