名校
解题方法
1 .  是重要的还原剂,合成方法:
是重要的还原剂,合成方法: 。下列说法正确的是
。下列说法正确的是
 是重要的还原剂,合成方法:
是重要的还原剂,合成方法: 。下列说法正确的是
。下列说法正确的是A.半径大小: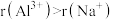 | B.电负性大小: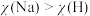 |
C.第一电离能: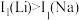 | D.碱性强弱: |
您最近一年使用:0次
2023-01-19更新
|
371次组卷
|
3卷引用:福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题
福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题江苏省南通市海安市2022-2023学年高三上学期1月期末考试化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题1-5)
名校
解题方法
2 . 法匹拉韦是治疗新冠肺炎的一种药物,其结构如图所示。下列说法错误的是


| A.该分子中所含元素中电负性最小的是H |
| B.该分子中C﹣F键的键能大于C﹣N键的键能 |
| C.该分子中所有C原子都为sp2杂化 |
| D.该分子中σ键与π键数目之比为7:2 |
您最近一年使用:0次
2023-01-13更新
|
588次组卷
|
5卷引用:福建省福州市连江第一中学2022-2023学年高二下学期4月期中化学试题
名校
解题方法
3 . 某锂电池材料的结构如图,M、W、X、Y、Z是原子序数依次增大的同周期主族元素,Y元素原子的价电子数是W的两倍。下列说法正确的是
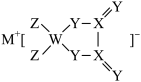
| A.简单氢化物沸点:X>Y |
| B.第一电离能:M>Z |
| C.元素X与Y原子轨道中含有的未成对电子数相同 |
| D.五种元素电负性最大的是X |
您最近一年使用:0次
2022-12-23更新
|
553次组卷
|
4卷引用:福建省厦门外国语学校2022-2023学年高二下学期期中考试化学试题
4 . “律动世界”国际化学元素周期表主题年活动报告中,提到了一种具有净水作用的物质,它由Q、W、X、Y、Z五种原子序数依次增大的元素组成。该五种元素的性质或结构信息如下表:
下列说法正确的是
| 元素 | 信息 |
| Q | 基态原子只有一种形状的轨道填有电子,并容易形成共价键 |
| W | 基态原子有5个原子轨道填充有电子,有2个未成对电子 |
| X | 最高价氧化物对应的水化物与Y、Z最高价氧化物对应的水化物都能反应 |
| Y | 在元素周期表中位于第3周期、第ⅥA族 |
| Z | 焰色反应为紫色 |
| A.电负性:Q<W<Y | B.第一电离能:W<X<Z |
| C.简单离子半径:X<W<Z<Y | D.这种物质只含离子键 |
您最近一年使用:0次
2022-11-02更新
|
1057次组卷
|
6卷引用:福建省福州高级中学2022-2023学年高二下学期4月期中考试化学试题
名校
解题方法
5 . 科学研究发现铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,因此受到研究人员的广泛关注。γ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去_______ 轨道电子。
(2)NH3中H−N−H的键角比NH 中H−N−H的键角
中H−N−H的键角_______ (填“大”或“小”)。
(3)羰基铁粉[Fe(CO)5]中配位原子为_______ 。
(4)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为_______ 。
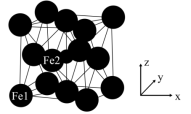
(5)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为_______ 。已知该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为_______ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)NH3中H−N−H的键角比NH
 中H−N−H的键角
中H−N−H的键角(3)羰基铁粉[Fe(CO)5]中配位原子为
(4)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(5)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
您最近一年使用:0次
2022-08-29更新
|
88次组卷
|
2卷引用:福建省福清虞阳中学2023-2024学年高三上学期第一次综合训练化学试题
名校
解题方法
6 . 某种锂盐的结构如图所示,其阴离子由W、X、Y、Z四种同周期主族元素构成,X原子的最外层电子数是W原子的次外层电子数的3倍,化合物中除Li+外其它原子均满足8电子稳定结构。下列说法正确的是
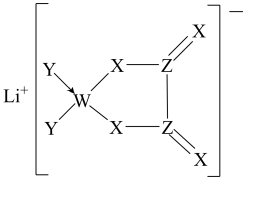

| A.W位于第2周期IVA族 | B.原子半径:Z>X>Y |
| C.元素电负性:Y>Z>X | D.最高化合价:Y>Z>W |
您最近一年使用:0次
2022-05-07更新
|
432次组卷
|
6卷引用:福建省厦门市湖滨中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
7 . 据《科学》报道,中国科学家首次实现超导体(Bi2Te3/NBSe2)中分段费米面。回答下列问题:
(1)Bi与P位于同主族,基态P原子的价层电子排布式为___________ 。基态Se原子核外电子云轮廓图呈哑铃形的能级上共有___________ 个电子。
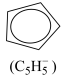
(2)二氯二茂铌的组成为(C5H5)2NbCl2.环戊二烯阴离子( )的平面结构简式如图所示:
)的平面结构简式如图所示:
①C、H、Cl的电负性由大到小的顺序为___________ 。
② 中C原子的杂化类型是
中C原子的杂化类型是___________ 。
③已知分子中的大π键可以用 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为___________ 。
(3) 的空间构型为
的空间构型为___________ 。
(4)四氟化铌(NbF4)的熔点为72℃,它的晶体类型为___________ 。
(1)Bi与P位于同主族,基态P原子的价层电子排布式为
(2)二氯二茂铌的组成为(C5H5)2NbCl2.环戊二烯阴离子(
 )的平面结构简式如图所示:
)的平面结构简式如图所示:
①C、H、Cl的电负性由大到小的顺序为
②
 中C原子的杂化类型是
中C原子的杂化类型是③已知分子中的大π键可以用
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为(3)
 的空间构型为
的空间构型为(4)四氟化铌(NbF4)的熔点为72℃,它的晶体类型为
您最近一年使用:0次
2022-03-25更新
|
233次组卷
|
2卷引用:福建省漳州市第三中学2022-2023学年高二下学期3月质量检测化学试题
名校
8 . 短周期元素X、Y、Z、W、R的原子序数依次增大,Y与W同主族,Z与R同主族,它们形成的甲、乙两种物质(如图)是有机合成中常用的还原剂。下列说法正确的是
甲: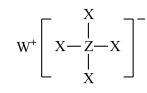 ,乙:
,乙: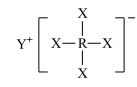
甲:
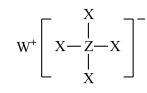 ,乙:
,乙: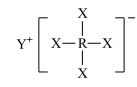
| A.电负性:X>Z>R |
| B.第一电离能:Y<Z<R |
| C.元素Z和R最高价氧化物对应的水化物都具有两性 |
| D.单质Y和W在空气中燃烧的产物所含化学键类型完全相同 |
您最近一年使用:0次
2022-03-03更新
|
723次组卷
|
6卷引用:福建省福清虞阳中学2023-2024学年高三上学期第一次综合训练化学试题
福建省福清虞阳中学2023-2024学年高三上学期第一次综合训练化学试题福建省福安市第一中学2023届高三上学期第一次检测化学试题山东省淄博市2022届高三下学期第一次模拟考试化学试题广东省佛山市第四中学2021-2022学年高二下学期3月段考化学试题(已下线)专项08 物质结构 元素周期律-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)云南省富源县第一中学2021-2022学年高三下学期4月月考化学试题
名校
解题方法
9 . 氮元素可以形成多种化合物。回答以下问题:
(1)基态氮原子的电子轨道排布式是_______ 。
(2)C、N、O三种元素第一电离能从小到大的顺序是_______ 。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①N2H4分子中氮原子轨道的杂化类型是_______ 。
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ΔH=-1038.7 kJ·mol-1;若该反应中有2 mol N-H键断裂,则形成的π键有_______ mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内存在_______ (填标号)。
a.离子键 b.共价键 c.范德华力 d.配位键
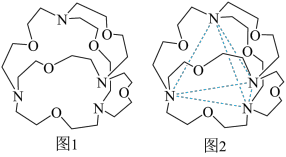
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是_______ (填标号)。
a.CF4 b.NH c.H2O d.CH4
c.H2O d.CH4
(5)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),该分子中所有原子电负性由大到小顺序是_______ 。
(1)基态氮原子的电子轨道排布式是
(2)C、N、O三种元素第一电离能从小到大的顺序是
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①N2H4分子中氮原子轨道的杂化类型是
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ΔH=-1038.7 kJ·mol-1;若该反应中有2 mol N-H键断裂,则形成的π键有
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内存在
a.离子键 b.共价键 c.范德华力 d.配位键
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是

a.CF4 b.NH
 c.H2O d.CH4
c.H2O d.CH4(5)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),该分子中所有原子电负性由大到小顺序是
您最近一年使用:0次
2021-05-14更新
|
126次组卷
|
2卷引用:福建省宁德第一中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
10 . 下列有关化学用语表述或性质比较正确的是
A.基态氧原子核外价电子排布轨道表示式 |
| B.磷化铜(Cu3P2)用于制造磷青铜,电负性:Cu<P |
C.用原子轨道描述氢分子中化学键的形成: |
D.在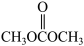 分子中, C 原子和O 原子均为 sp3杂化 分子中, C 原子和O 原子均为 sp3杂化 |
您最近一年使用:0次
2021-04-05更新
|
793次组卷
|
7卷引用:福建省南平市高级中学2022-2023学年高二下学期期中考试化学试题



