名校
解题方法
1 . 翡翠是玉石中的一种,其主要成分为NaAlSi2O6,常含微量Cr、Ni、Mn、Fe、Mg等元素,其中Cr3+的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一。
(1)基态硅原子的核外电子排布式为___________________ 。
(2)NaAlSi2O6所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物是___________ (写电子式)。
(3)硅与碳类似,能与氢元素形成SiH4、Si2H4、Si3H8,此三种分子中硅原子为sp3杂化的有_______ ;Si2H4分子的空间构型是___________ 。
(4)已知氧化钠、氧化铝的熔点分别为1132℃、2054℃,从结构的角度解释导致这种差异的主要原因:_________
(5)已知某FeSO4·xH2O的结构如图所示。
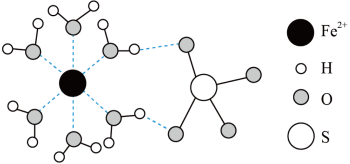
粒子内部的键角SO
_______ H2O(填“>”“<”或“=”),从杂化类型及斥力大小角度说明判断的理由:_______________ 。
(6)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式。
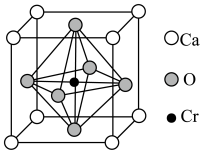
①该晶体的化学式为_______ 。
②已知钙离子、氧离子半径分别为100pm、140pm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为___________ pm。
(1)基态硅原子的核外电子排布式为
(2)NaAlSi2O6所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物是
(3)硅与碳类似,能与氢元素形成SiH4、Si2H4、Si3H8,此三种分子中硅原子为sp3杂化的有
(4)已知氧化钠、氧化铝的熔点分别为1132℃、2054℃,从结构的角度解释导致这种差异的主要原因:
(5)已知某FeSO4·xH2O的结构如图所示。

粒子内部的键角SO

(6)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式。

①该晶体的化学式为
②已知钙离子、氧离子半径分别为100pm、140pm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
名校
解题方法
2 . 中国科学家首次在月球上发现新矿物,将其命名为“嫦娥石”,“嫦娥石”中包含了Fe、Cu、Ti、Cr、Ni、Mo、N、O等多种元素。
(1)鉴定月球土壤的元素组成,可采用的方法是___________ 。
A.光谱分析 B.X-射线衍射分析
(2)在第二周期中,第一电离能比N高的主族元素是___________ 。氮原子的电子排布图表示的状态中,能量由低到高的顺序是___________ (填序号)。
A.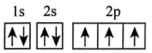 B.
B.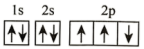
C.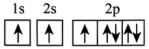 D.
D.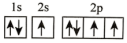
(3)已知有关氮、磷的单键和三键的键能( )如下表:
)如下表:
从能量角度看,氮以 、而白磷以
、而白磷以 (结构式可表示为
(结构式可表示为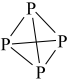 )形式存在的原因是
)形式存在的原因是___________ 。
(4)已知 分子的键角约为107°,而同主族磷的氢化物
分子的键角约为107°,而同主族磷的氢化物 分子的键角约为94°,试用价层电子对互斥模型解释
分子的键角约为94°,试用价层电子对互斥模型解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:___________
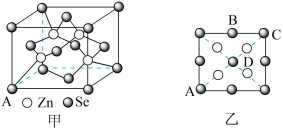
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,乙图为甲图的俯视图,若原子坐标A为(0,0,0),B为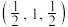 ,则D原子坐标为
,则D原子坐标为___________ ;若该晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_________________ 。
(1)鉴定月球土壤的元素组成,可采用的方法是
A.光谱分析 B.X-射线衍射分析
(2)在第二周期中,第一电离能比N高的主族元素是
A.
 B.
B.
C.
 D.
D.
(3)已知有关氮、磷的单键和三键的键能(
 )如下表:
)如下表:| N-N |  | P-P |  |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以
 、而白磷以
、而白磷以 (结构式可表示为
(结构式可表示为 )形式存在的原因是
)形式存在的原因是(4)已知
 分子的键角约为107°,而同主族磷的氢化物
分子的键角约为107°,而同主族磷的氢化物 分子的键角约为94°,试用价层电子对互斥模型解释
分子的键角约为94°,试用价层电子对互斥模型解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,乙图为甲图的俯视图,若原子坐标A为(0,0,0),B为
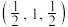 ,则D原子坐标为
,则D原子坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
3 . 我国科学家在寻找“点击反应”的砌块过程中,发现一种新的化合物,结构如下图所示,其中X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与W是同一主族元素。下列说法正确的是
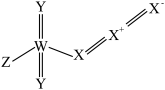

| A.元素电负性:Z>Y>W | B.简单氢化物沸点:X>Y>W |
| C.简单离子半径:Z>Y>X | D.X、W氧化物的水化物均为强酸 |
您最近一年使用:0次
4 . 回答下列问题:
(1)下列现象与原子核外电子跃迁有关的是___________ (填序号)。
a.焰火 b.LED灯光 c.金属导电
(2)在周期表中,与Li的化学性质最相似的邻族元素是___________ 。
(3)硼、钛等元素的化合物具有广泛的应用价值。
①B原子中存在未成对电子的能级电子云在空间有___________ 种伸展方向。
② (硼氢化钛)可由
(硼氢化钛)可由 和
和 反应制得。基态钛原子的价层电子轨道表示式为
反应制得。基态钛原子的价层电子轨道表示式为___________ 。电负性大小顺序为H___________ B(填“>”或“<”)。
(4)氮单质及其化合物在研究和生产中有着广泛的应用。
①亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到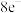 结构,则其电子式为
结构,则其电子式为___________ ,其水解会生成两种酸,写出水解的化学方程式___________ 。
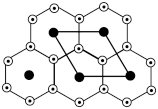
②氮化锂晶体中存在锂、氮原子共同组成的锂、氮层,锂原子以石墨晶体中的碳原子方式排布,N原子处在六元环的中心,同层中锂、氮的原子个数比为___________ ;
(1)下列现象与原子核外电子跃迁有关的是
a.焰火 b.LED灯光 c.金属导电
(2)在周期表中,与Li的化学性质最相似的邻族元素是
(3)硼、钛等元素的化合物具有广泛的应用价值。
①B原子中存在未成对电子的能级电子云在空间有
②
 (硼氢化钛)可由
(硼氢化钛)可由 和
和 反应制得。基态钛原子的价层电子轨道表示式为
反应制得。基态钛原子的价层电子轨道表示式为(4)氮单质及其化合物在研究和生产中有着广泛的应用。
①亚硝酰氯(NOCl)是一种红褐色液体,每个原子最外层都达到
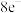 结构,则其电子式为
结构,则其电子式为②氮化锂晶体中存在锂、氮原子共同组成的锂、氮层,锂原子以石墨晶体中的碳原子方式排布,N原子处在六元环的中心,同层中锂、氮的原子个数比为

您最近一年使用:0次
解题方法
5 . 由短周期元素组成的一种药物的分子结构式如图所示。其中X原子的核外电子只有一种运动状态;元素Y、Z、W、E原子序数依次增大,基态W与E的价电子排布均为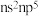 。下列说法不正确的是
。下列说法不正确的是
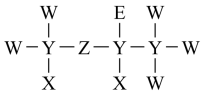
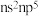 。下列说法不正确的是
。下列说法不正确的是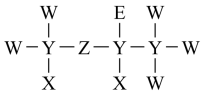
| A.沸点高低:XW>XE | B.元素电负性大小:X<Y<W |
| C.简单氢化物的稳定性:Y<Z<W | D.该结构式中所有原子均达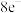 稳定结构 稳定结构 |
您最近一年使用:0次
名校
解题方法
6 . 立方氮化硼硬度高,耐磨性好,在机械加工行业有广泛应用。制备立方氮化硼的一种方法为 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A. 的分子构型为三角锥型 的分子构型为三角锥型 |
B.元素电负性大小为 |
| C.反应混合物中所有化学键均为共价键 |
D.形成 时B原子先激发后杂化,其激发态价电子轨道表示式为: 时B原子先激发后杂化,其激发态价电子轨道表示式为: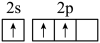 |
您最近一年使用:0次
名校
解题方法
7 . 下列有关化学用语的表示错误的是
A.四氯化碳分子的球棍模型: |
B.次氯酸的电子式: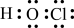 |
C.质子数、中子数分别为11、12的核素: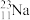 |
| D.从电负性的角度分析,CF3I水解反应的方程式为:CF3I+H2O→CF3OH+HI |
您最近一年使用:0次
名校
解题方法
8 . 下列有关合成药物胃复安的说法不正确的是
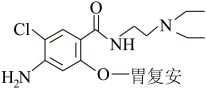
| A.分子中碳原子有2种杂化类型 |
| B.该分子组成元素的电负性由大到小的顺序为:O>N>C>H |
| C.该分子组成元素第一电离能最大的是O |
| D.分子中所有氮原子上都有一对孤电子对 |
您最近一年使用:0次
2023-03-16更新
|
251次组卷
|
2卷引用:福建省龙岩第一中学2022-2023学年高二下学期第一次月考化学试题
解题方法
9 . W、R、X、Y、Z为原子序数依次增大的短周期元素.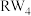 、
、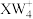 和
和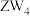 三种微粒的空间构型相同,Y原子的电子层数等于最外层电子数。以下说法错误的是
三种微粒的空间构型相同,Y原子的电子层数等于最外层电子数。以下说法错误的是
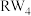 、
、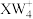 和
和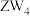 三种微粒的空间构型相同,Y原子的电子层数等于最外层电子数。以下说法错误的是
三种微粒的空间构型相同,Y原子的电子层数等于最外层电子数。以下说法错误的是A.氢化物稳定性: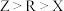 | B.最高价氧化物对应水化物酸性: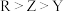 |
C.电负性: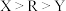 | D.原子晶体 中Z的配位数为4 中Z的配位数为4 |
您最近一年使用:0次
名校
解题方法
10 . 硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为pnm,乙图为晶胞的俯视图,下列说法正确的是
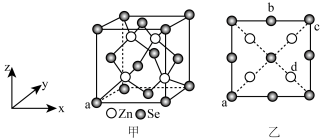
| A.晶胞中硒原子的配位数为12 |
B.晶胞中d点原子分数坐标为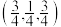 |
C.相邻两个Zn原子的最短距离为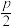 nm nm |
| D.电负性:Zn>Se |
您最近一年使用:0次
2023-03-03更新
|
1972次组卷
|
12卷引用:福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题
福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题山东省济宁市2023届高三一模考试(3月)化学试题山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)专题十 晶胞示意图(练)河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题(已下线)热点08 金属晶体和离子晶体山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题山东省临沂市第二十四中学2023-2024学年高二下学期3月学科素养水平监测化学试题(已下线)选择题11-12



