名校
解题方法
1 . 表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是

下列说法正确的是
| A.电负性:x>y |
| B.ca3分子的空间构型为平面三角形 |
| C.c形成的单质中σ键与π键个数之比为1 :2 |
| D.b、c、d形成的气态氢化物互为等电子体 |
您最近一年使用:0次
名校
2 . 火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断下列有关说法正确的是( )
| A.羰基硫属于非极性分子 | B.羰基硫的电子式为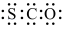 |
| C.羰基硫的沸点比CO2低 | D.羰基硫分子中三个原子处于同一直线上 |
您最近一年使用:0次
2020-07-17更新
|
59次组卷
|
3卷引用:安徽省六安中学2019-2020学年高二下学期期末考试化学试题
解题方法
3 . 下列各分子中,属于含极性键的非极性分子的是
| A.P4 | B.CO2 | C.H2S | D.NH3 |
您最近一年使用:0次
名校
解题方法
4 . 按照要求回答下列问题:
(1)基态 Cr 原子的价电子排布式为_______ ,占据最高能层的电子的电子云轮廓图形状为__ 。
(2)在BF3分子中,硼原子的杂化轨道类型为________ ,BF3和过量NaF作用可生成NaBF4,BF 的立体构型为
的立体构型为________ ,写出BF 的一种等电子体
的一种等电子体_______ 。
(3)Fe3+比 Fe2+更稳定的原因是_______________________________ 。
(4)金刚石晶胞中面心和顶点碳原子替换成硅原子即为金刚砂晶胞,其晶胞如图所示:
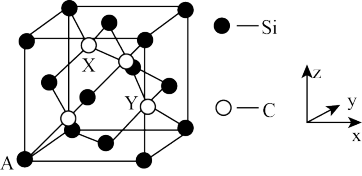
①金刚砂的化学式为_________ 。
②原子坐标参数表示晶胞内部各原子的相对位置。图中 A 原子坐标(0,0,0),则金刚砂晶胞中碳原子 X 的原子坐标为____________ 。
(1)基态 Cr 原子的价电子排布式为
(2)在BF3分子中,硼原子的杂化轨道类型为
 的立体构型为
的立体构型为 的一种等电子体
的一种等电子体(3)Fe3+比 Fe2+更稳定的原因是
(4)金刚石晶胞中面心和顶点碳原子替换成硅原子即为金刚砂晶胞,其晶胞如图所示:

①金刚砂的化学式为
②原子坐标参数表示晶胞内部各原子的相对位置。图中 A 原子坐标(0,0,0),则金刚砂晶胞中碳原子 X 的原子坐标为
您最近一年使用:0次
名校
解题方法
5 . I. 现有一组物质的熔点(℃)数据,据此回答下列问题:
(1)HF熔点反常是由于______________ 。这组物质中共价键的键能最大的是_____ 。
II.按要求回答下列问题。
(2)CS2气化时克服的粒子间作用是__________ ,1mol CS2中含有___ mol σ键,含有___ mol π键。
(3)HCHO分子中C原子轨道的杂化类型为______ 。
| HF:-83 | HCl:-115 | HBr:-89 | HI:-51 |
(1)HF熔点反常是由于
II.按要求回答下列问题。
(2)CS2气化时克服的粒子间作用是
(3)HCHO分子中C原子轨道的杂化类型为
您最近一年使用:0次
名校
解题方法
6 . 下列说法中正确的是( )
| A.H2O是一种非常稳定的化合物,这是由于氢键所致 |
| B.杂化轨道全部参加形成化学键 |
| C.气体单质中,一定有σ键,可能有π键 |
| D.两个原子之间形成共价键时,最多有一个σ键 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法错误的是
| A.原子间通过共用电子对所形成的化学键叫共价键 |
| B.两个成键原子间的核间距离叫键长,键长越短,化学键越牢固 |
| C.极性分子中一定含有极性键 |
| D.离子化合物中不可能含有非极性键 |
您最近一年使用:0次
2020-06-21更新
|
387次组卷
|
2卷引用:陕西省榆林市绥德县绥德中学2019-2020学年高二上学期第二次阶段检测化学试题
10-11高二下·河北衡水·阶段练习
名校
解题方法
8 . 下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | SO2溶于水形成的溶液能导电 | SO2是电解质 |
| B | 白磷为正四面体结构的分子 | 白磷分子中P—P键间的键角是109.5° |
| C | 1体积水可以溶解约700体积氨气 | 氨是极性分子且存在氢键的影响 |
| D | HF的沸点高于HCl | H—F的键长比H—Cl的键长短 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-06-16更新
|
180次组卷
|
18卷引用:2011-2012学年陕西省师大附中高二下学期期中考试化学试卷
(已下线)2011-2012学年陕西省师大附中高二下学期期中考试化学试卷(已下线)2010-2011学年河北省冀州中学高二下学期第三次月考化学卷2014-2015学年辽宁实验分校高二下6月阶段测试化学试卷2016届安徽省六安一中高三上第四次月考化学试卷2015-2016学年四川省南充高中高二下期末化学试卷吉林省长春汽车经济开发区第三中学2018-2019学年高二下学期4月月考化学试题山西省孝义市2019-2020学年高二下学期3月阶段性考试化学试题天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题福建省莆田第一中学2019-2020学年高二下学期期中考试化学试题四川省乐山十校2020-2021学年高二上学期半期联考化学试题湖北省孝感市高级中学2020—2021学年高二下学期2月调研考试化学试题(已下线)模块同步卷05 分子的立体构型及分子的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)福建省福清西山学校高中部2020-2021学年高二下学期期中考试化学试题吉林省通化县综合高级中学2020-2021学年高二下学期期末考试化学试题宁夏贺兰县景博中学2021-2022学年高二下学期第一次月考化学试题四川省乐山市沫若中学2022-2023学年高二上学期第一次月考化学试题四川省盐亭中学2022-2023学年高二上学期期中教学质量监测(理科)化学试题河南省焦作市2022-2023学年第四中学高二下学期期中考试 化学试卷
名校
解题方法
9 . 一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式为________________ 。
②NO 的空间构型
的空间构型__________ (用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①CO分子的等电子体有______ 。(至少写两个)
②HCHO分子中C原子轨道的杂化类型为______ 。
③1 mol CO2中含有的σ键与π键数目之比为_____ 。
④CO还能以配体形式与金属形成配合物,如Fe(CO)5,1mol Fe(CO)5中π键数目为__________ 。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式为
②NO
 的空间构型
的空间构型(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①CO分子的等电子体有
②HCHO分子中C原子轨道的杂化类型为
③1 mol CO2中含有的σ键与π键数目之比为
④CO还能以配体形式与金属形成配合物,如Fe(CO)5,1mol Fe(CO)5中π键数目为
您最近一年使用:0次
名校
解题方法
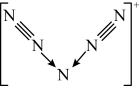
10 . 最近,科学家合成了含有N 的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )
的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )
 的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )
的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )
A.每个N 中含有35个质子和36个电子 中含有35个质子和36个电子 |
| B.该离子中有非极性键和配位键 |
| C.该离子中含有2个π键 |
D.与PCl 互为等电子体 互为等电子体 |
您最近一年使用:0次



