解题方法
1 . 完成下列问题。
(1)甲醇( )空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为:
)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为: 2
2

①HCHO分子内σ键与π键个数之比为_______ ,HCHO的空间结构为_______ 。
② 和HCHO分子中碳原子的杂化轨道类型分别为
和HCHO分子中碳原子的杂化轨道类型分别为_______ 和_______ 。
③甲醇氧化生成HCHO时,会产生CO、 、
、 等副产物。相同条件下,
等副产物。相同条件下, 的沸点比
的沸点比 的高,主要原因为
的高,主要原因为_______ 。
(2)金属镍是电池制造过程中重要的原材料,未来十年新能源汽车领域镍需求增长将达8~16倍。一种制备金属镍的方法为 。回答下列问题:
。回答下列问题:
①已知 熔融状态时能导电,上述制备反应化学方程式中的6种物质所属的晶体类型有
熔融状态时能导电,上述制备反应化学方程式中的6种物质所属的晶体类型有____ 种。
②丁二酮肟( )是检验
)是检验 的灵敏试剂,可与
的灵敏试剂,可与 生成丁二酮肟镍亮红色沉淀。丁二酮肟镍分子(结构如图1所示)内不存在的作用力有
生成丁二酮肟镍亮红色沉淀。丁二酮肟镍分子(结构如图1所示)内不存在的作用力有_______ (填标号)。

A.金属键 B.氢键 C.π键 D.配位键 E.离子键
③镧镍合金是稀土系储氢合金的典型代表,其晶胞参数分别为apm、bpm、cpm,阿伏加德罗常数的值为 ,该合金储氢后的晶胞如图2所示。1mol镧形成的该合金能储存
,该合金储氢后的晶胞如图2所示。1mol镧形成的该合金能储存_______ mol氢气。储氢前,该合金的密度为_______  (列出含a、b、c和
(列出含a、b、c和 的计算式即可)。
的计算式即可)。

(1)甲醇(
 )空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为:
)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为: 2
2

①HCHO分子内σ键与π键个数之比为
②
 和HCHO分子中碳原子的杂化轨道类型分别为
和HCHO分子中碳原子的杂化轨道类型分别为③甲醇氧化生成HCHO时,会产生CO、
 、
、 等副产物。相同条件下,
等副产物。相同条件下, 的沸点比
的沸点比 的高,主要原因为
的高,主要原因为(2)金属镍是电池制造过程中重要的原材料,未来十年新能源汽车领域镍需求增长将达8~16倍。一种制备金属镍的方法为
 。回答下列问题:
。回答下列问题:①已知
 熔融状态时能导电,上述制备反应化学方程式中的6种物质所属的晶体类型有
熔融状态时能导电,上述制备反应化学方程式中的6种物质所属的晶体类型有②丁二酮肟(
 )是检验
)是检验 的灵敏试剂,可与
的灵敏试剂,可与 生成丁二酮肟镍亮红色沉淀。丁二酮肟镍分子(结构如图1所示)内不存在的作用力有
生成丁二酮肟镍亮红色沉淀。丁二酮肟镍分子(结构如图1所示)内不存在的作用力有
A.金属键 B.氢键 C.π键 D.配位键 E.离子键
③镧镍合金是稀土系储氢合金的典型代表,其晶胞参数分别为apm、bpm、cpm,阿伏加德罗常数的值为
 ,该合金储氢后的晶胞如图2所示。1mol镧形成的该合金能储存
,该合金储氢后的晶胞如图2所示。1mol镧形成的该合金能储存 (列出含a、b、c和
(列出含a、b、c和 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
名校
解题方法
2 . 明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载。锌及其化合物在生产、生活中有着重要的用途。锌是生命体必需的微量元素,被称为“生命之花”。
(1)基态Zn原子核外电子共有____ 种空间运动状态。
(2)锌与铜在周期表中的位置相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10失去1个电子需要的能量由大到小排序是____ (填字母)。
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。其中CO 的空间构型为
的空间构型为____ (用文字描述)。与CO 互为等电子体的分子是
互为等电子体的分子是____ (写一种即可)。
(4)葡萄糖酸锌为有机锌补剂,对胃黏膜刺激小,在人体中吸收率高。如图是葡萄糖酸锌的结构简式。

①葡萄糖酸锌组成元素中电负性最大的元素为____ ,其中C原子的杂化方式为____ 。
②1mol葡萄糖酸分子中含有____ molσ键。葡萄糖酸的熔点小于葡萄糖酸锌的熔点原因是____ 。
(5)ZnS是一种性能优异的荧光材料,在自然界中有立方ZnS和六方ZnS两种晶型,其晶胞结构如图所示:

①立方ZnS中,Zn2+填充在S2—形成的____ 空隙中;
②六方ZnS的晶体密度为____ g·cm-3(设NA为阿伏加德罗常数的值)。
(1)基态Zn原子核外电子共有
(2)锌与铜在周期表中的位置相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10失去1个电子需要的能量由大到小排序是
| A.④②①③ | B.④②③① | C.①②④③ | D.①④③② |
 的空间构型为
的空间构型为 互为等电子体的分子是
互为等电子体的分子是(4)葡萄糖酸锌为有机锌补剂,对胃黏膜刺激小,在人体中吸收率高。如图是葡萄糖酸锌的结构简式。

①葡萄糖酸锌组成元素中电负性最大的元素为
②1mol葡萄糖酸分子中含有
(5)ZnS是一种性能优异的荧光材料,在自然界中有立方ZnS和六方ZnS两种晶型,其晶胞结构如图所示:

①立方ZnS中,Zn2+填充在S2—形成的
②六方ZnS的晶体密度为
您最近一年使用:0次
2022-05-24更新
|
546次组卷
|
2卷引用:广西壮族自治区南宁市第三中学2022届高三一模理综化学试题
名校
解题方法
3 . 全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有_______ 种,若其电子排布式表示为[ Ne]3s2 违背了
违背了_______ 。
(2)高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3_______ SiCl4(填“>”或“<”),与SiCl4互为等电子体的离子为_______ (任写1种即可)。已知电负性:H>Si,则SiHCl3充分水解的化学方程式为_______ 。
(3)复兴号高铁车体材质用到Mn、Co等元素。
①Mn的一种配合物化学式为[ Mn(CO)5( CH3CN)],下列说法正确的是_______ (填字母标号)。
A. CH3CN与Mn原子配位时,提供孤电子对的是C原子
B. Mn原子的配位数为6
C. CH3CN中C原子的杂化类型为sp2、sp3
D. CH3CN中σ键与π键数目之比为5:2
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测MnCO3比CoCO3的分解温度_______ (填“高”或“低”),解释原因_______ 。
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,其中阴离子( N3- )采用面心立方最密堆积方式,则r(Ti3+)为_______ D,该氮化钛的密度_______ g· cm-3(列出计算式即可)。

(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有
 违背了
违背了(2)高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3
(3)复兴号高铁车体材质用到Mn、Co等元素。
①Mn的一种配合物化学式为[ Mn(CO)5( CH3CN)],下列说法正确的是
A. CH3CN与Mn原子配位时,提供孤电子对的是C原子
B. Mn原子的配位数为6
C. CH3CN中C原子的杂化类型为sp2、sp3
D. CH3CN中σ键与π键数目之比为5:2
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测MnCO3比CoCO3的分解温度
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,其中阴离子( N3- )采用面心立方最密堆积方式,则r(Ti3+)为

您最近一年使用:0次
2022-04-14更新
|
1935次组卷
|
11卷引用:广西南宁市第二中学2021-2022学年高三下学期收网题理综化学试题
广西南宁市第二中学2021-2022学年高三下学期收网题理综化学试题山西省临汾市2022届高考考前适应性训练考试(二)理科综合化学试题(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考押题预测卷01(全国甲卷)广东省茂名市普通高中毕业班2022届高三下学期模拟考试化学试题北京市第二中学2022届高三下学期五月模拟考试化学试题广东省广州市第六中学2022届高三第三次模拟考试化学试题(已下线)第21练 新高考模式综合练(广东卷)-2022年【暑假分层作业】高二化学(2023届一轮复习通用)新疆乌鲁木齐市第四中学2021-2022学年高二下学期期末考试化学试题陕西师范大学附属中学、渭北中学等2022-2023学年高三上学期期初检测化学联考试题陕西师范大学附属中学、渭北中学等2023届高三上学期期初检测联考化学试题
名校
4 . 下列说法正确的是
A. 键和 键和 键都属于共价键,均有方向性 键都属于共价键,均有方向性 |
| B.气体单质中,一定有σ键,可能有π键 |
C.苯分子中每个碳原子的 杂化轨道中的其中一个形成大 杂化轨道中的其中一个形成大 键 键 |
| D.等物质的量的[Cu(H2O)4]2+与[Ag(NH3)2]+中所含的σ键数之比为3:2 |
您最近一年使用:0次
2021-01-29更新
|
1530次组卷
|
6卷引用:广西南宁市宾阳县宾阳中学2021-2022学年高二下学期3月月考化学试题
广西南宁市宾阳县宾阳中学2021-2022学年高二下学期3月月考化学试题山东省烟台市2020-2021学年高二上学期期末考试化学试题(已下线)2.2 分子的空间结构(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)山东省烟台市莱州第一中学2021-2022学年高二12月月考化学试题专题4 分子空间结构与物质性质 本专题达标检测(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测
解题方法
5 . 点击化学的代表反应为铜催化的叠氮-炔基Husigen环加成反应,NaN3、SO2F2、FSO2N2等均是点击化学中常用无机试剂。回答下列问题:
(1)基态Cu原子价电子排布式为___________ ;基态N原子未成对电子有___________ 个。
(2)F、O、N的电负性从小到大的顺序是___________ 。
(3)SO2F2中硫原子价层电子对数目为___________ ;SO2F2的沸点比FSO2N3的低,其主要原因是___________ 。
(4)NaN3是HN3的钠盐,下列有关HN3说法正确的是___________ (填字母)。
a.HN3分子呈直线型 b.HN3分子间存在氢键
c.HN3中氮原子杂化方式只有sp d.HN3与HOCN互为等电子体
(5)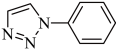 是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有
是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有___________ 个σ键。
(6)CuBr是点击化学常用的催化剂,其晶胞结构如图所示,晶胞参数为a pm。
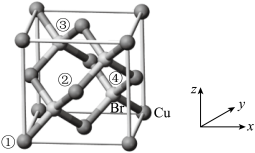
已知①、②号铜原子坐标依次为(0,0,0)、( ,0,
,0, ),则③号溴原子的坐标为
),则③号溴原子的坐标为___________ ;设NA为阿伏加德罗常数的值,CuBr的密度为___________ g·cm-3(列出计算式)。
(1)基态Cu原子价电子排布式为
(2)F、O、N的电负性从小到大的顺序是
(3)SO2F2中硫原子价层电子对数目为
(4)NaN3是HN3的钠盐,下列有关HN3说法正确的是
a.HN3分子呈直线型 b.HN3分子间存在氢键
c.HN3中氮原子杂化方式只有sp d.HN3与HOCN互为等电子体
(5)
 是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有
是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有(6)CuBr是点击化学常用的催化剂,其晶胞结构如图所示,晶胞参数为a pm。

已知①、②号铜原子坐标依次为(0,0,0)、(
 ,0,
,0, ),则③号溴原子的坐标为
),则③号溴原子的坐标为
您最近一年使用:0次
解题方法
6 . 碳及其化合物广泛存在于自然界中,回答下列问题:
(1)在基态C原子中,核外存在_______ 对自旋方向相反的电子。
(2)丙酮( )分子中,中间碳原子的杂化方式为
)分子中,中间碳原子的杂化方式为______ ; 中
中 键和π键的数目之比为
键和π键的数目之比为__________________ .
(3)写出两个与CO2具有相同空间构型的分子或离子:_____________
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体;Fe3+的核外电子排布式为__________________ 。
(5)已知第IIA族元素的碳酸盐MCO3热分解的主要过程为M2+结合碳酸根离子中的O2-,释放出CO2。则CaCO3的分解温度低于BaCO3的原因是_______________ 。分子中的大π键用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则CO32-中的大π键应表示为
),则CO32-中的大π键应表示为____________ 。
(6)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,一个六元环上的C原子数为__________________ 。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接_____ 个六元环,六元环中最多有_______ 个C原子在同一平面。
(1)在基态C原子中,核外存在
(2)丙酮(
 )分子中,中间碳原子的杂化方式为
)分子中,中间碳原子的杂化方式为 中
中 键和π键的数目之比为
键和π键的数目之比为(3)写出两个与CO2具有相同空间构型的分子或离子:
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
(5)已知第IIA族元素的碳酸盐MCO3热分解的主要过程为M2+结合碳酸根离子中的O2-,释放出CO2。则CaCO3的分解温度低于BaCO3的原因是
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则CO32-中的大π键应表示为
),则CO32-中的大π键应表示为(6)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,一个六元环上的C原子数为
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次



