1 . Si、S、Se在自然界中形成多种多样的物质结构。回答下列问题:
(1)Se与O同族,电负性较大的是_____ ;基态Se原子的价电子运动状态有_____ 种。
(2)已知液态的二氧化硫可以发生类似水的自电离: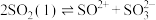 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为__ , 的空间结构为
的空间结构为_______ 。
(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为_______ ,二者中更易与 形成配位键的是
形成配位键的是_______ 。 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是_______ 。
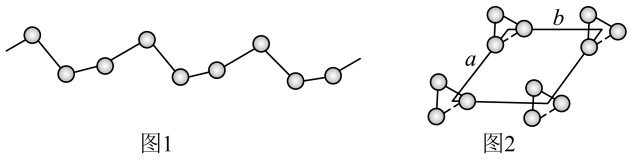
(5) -硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。
-硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。 -硒六方晶胞参数为
-硒六方晶胞参数为 、
、 、
、 (其中
(其中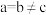 ),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为
),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为 。
。_______ 。晶胞中含有Se原子的数目为_______ ;则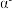 -硒晶胞的摩尔体积为
-硒晶胞的摩尔体积为______  (列出算式)。
(列出算式)。
(1)Se与O同族,电负性较大的是
(2)已知液态的二氧化硫可以发生类似水的自电离:
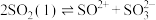 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为 的空间结构为
的空间结构为(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物
 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为 形成配位键的是
形成配位键的是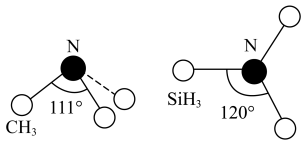
 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是(5)
 -硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。
-硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。 -硒六方晶胞参数为
-硒六方晶胞参数为 、
、 、
、 (其中
(其中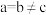 ),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为
),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为 。
。
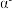 -硒晶胞的摩尔体积为
-硒晶胞的摩尔体积为 (列出算式)。
(列出算式)。
您最近一年使用:0次
解题方法
2 . 2020年12月17日,我国的嫦娥五号返回器携带月球样品,在内蒙古预定区域安全着陆。经科学家分析,发现月球土壤中富含有He、O、Si、 Fe、 Mg、Ca、Mn、Ti、Al、Au、Ag、 Pb、 Zn、 Cu等元素。
(1)使用3He的热核反应堆没有中子产生,故使用3He作为能源时,不会产生辐射。写出He的电子排布图_______ 。
(2)溶液中Fe3+比Fe2+更稳定的原因是_______ 。
(3)金属Ca和Mn属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点沸点等都比金属Mn低,其原因是_______ 。
(4)向Cu(OH)2悬浊液中通入NH3,蓝色沉淀溶解,溶液变为深蓝色,发生了如下反应:Cu(OH)2 + 4NH3 = [Cu(NH3)4]2+ + 2OH—,NH3分子中N的杂化类型为_______ , 比较NH3和[Cu(NH3)4]2+中H—N—H 键角的大小: NH3_______ [Cu(NH3)4]2+ (填“>”或“<”),1mol [Cu(NH3)4]2+中σ键的数目为_______ NA。
(5)CaTiO3的晶胞如图所示,Ti4+的配位数是_______ ,若Ca2+位于晶胞顶点,则O2-位于_______ 位置,若晶胞参数为anm,则晶体密度为_______ g·cm-3 (列出计算式,阿伏加德罗常数用NA表示)。

(1)使用3He的热核反应堆没有中子产生,故使用3He作为能源时,不会产生辐射。写出He的电子排布图
(2)溶液中Fe3+比Fe2+更稳定的原因是
(3)金属Ca和Mn属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点沸点等都比金属Mn低,其原因是
(4)向Cu(OH)2悬浊液中通入NH3,蓝色沉淀溶解,溶液变为深蓝色,发生了如下反应:Cu(OH)2 + 4NH3 = [Cu(NH3)4]2+ + 2OH—,NH3分子中N的杂化类型为
(5)CaTiO3的晶胞如图所示,Ti4+的配位数是

您最近一年使用:0次
名校
解题方法
3 . 明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载。锌及其化合物在生产、生活中有着重要的用途。锌是生命体必需的微量元素,被称为“生命之花”。
(1)基态Zn原子核外电子共有____ 种空间运动状态。
(2)锌与铜在周期表中的位置相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10失去1个电子需要的能量由大到小排序是____ (填字母)。
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。其中CO 的空间构型为
的空间构型为____ (用文字描述)。与CO 互为等电子体的分子是
互为等电子体的分子是____ (写一种即可)。
(4)葡萄糖酸锌为有机锌补剂,对胃黏膜刺激小,在人体中吸收率高。如图是葡萄糖酸锌的结构简式。

①葡萄糖酸锌组成元素中电负性最大的元素为____ ,其中C原子的杂化方式为____ 。
②1mol葡萄糖酸分子中含有____ molσ键。葡萄糖酸的熔点小于葡萄糖酸锌的熔点原因是____ 。
(5)ZnS是一种性能优异的荧光材料,在自然界中有立方ZnS和六方ZnS两种晶型,其晶胞结构如图所示:

①立方ZnS中,Zn2+填充在S2—形成的____ 空隙中;
②六方ZnS的晶体密度为____ g·cm-3(设NA为阿伏加德罗常数的值)。
(1)基态Zn原子核外电子共有
(2)锌与铜在周期表中的位置相邻。现有4种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10失去1个电子需要的能量由大到小排序是
| A.④②①③ | B.④②③① | C.①②④③ | D.①④③② |
 的空间构型为
的空间构型为 互为等电子体的分子是
互为等电子体的分子是(4)葡萄糖酸锌为有机锌补剂,对胃黏膜刺激小,在人体中吸收率高。如图是葡萄糖酸锌的结构简式。

①葡萄糖酸锌组成元素中电负性最大的元素为
②1mol葡萄糖酸分子中含有
(5)ZnS是一种性能优异的荧光材料,在自然界中有立方ZnS和六方ZnS两种晶型,其晶胞结构如图所示:

①立方ZnS中,Zn2+填充在S2—形成的
②六方ZnS的晶体密度为
您最近一年使用:0次
2022-05-24更新
|
546次组卷
|
2卷引用:四川省宜宾市叙州区第一中学校2024届高三上学期一诊模拟考试理综化学试题
名校
4 . 中科院大连物化所成功利用具有尖晶石结构的Co3O4电催化剂电解水。
(1)Co在周期表中的位置是____ ,基态Co的电子占据的最高能层符号为____ 。
(2)钴盐引发动物中毒时,通常可以用EDTA(结构如图)解毒。其中,N的杂化方式均为____ ,N的I1(第一电离能)大于O的I1,其原因是____ ;自由基是指含单电子的基团,1mol—COOH(羧基自由基)中存在____ molσ键和____ molπ键。

(3)EDTA可以由乙二胺与甲醛、氰化钠间接得到。离子化合物氰化钠的晶体类型为____ ,甲醛分子的空间构型为____ 。
(4)Co3O4晶体中O作面心立方最密堆积(如图),Co随机填充在晶胞中O构成的8个四面体空隙和4个八面体空隙中,则Co的配位数分别为____ ,Co总的空隙填充率为____ ,如果晶胞边长为anm,Co3O4的摩尔质量为Mg/mol,NA为阿伏加德罗常数的值,则Co3O4的晶体密度为____ g/cm3(列出计算式)。

(1)Co在周期表中的位置是
(2)钴盐引发动物中毒时,通常可以用EDTA(结构如图)解毒。其中,N的杂化方式均为

(3)EDTA可以由乙二胺与甲醛、氰化钠间接得到。离子化合物氰化钠的晶体类型为
(4)Co3O4晶体中O作面心立方最密堆积(如图),Co随机填充在晶胞中O构成的8个四面体空隙和4个八面体空隙中,则Co的配位数分别为

您最近一年使用:0次
2022-03-26更新
|
383次组卷
|
3卷引用:四川省遂宁市2022届高三第二次诊断性考试(二模)理综化学试题
解题方法
5 . 贝壳、珍珠、方解石等主要成分均含有CaCO3,回答下列问题:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧碳酸钙时的焰色为_______ (填标号)。
A 黄色 B 红色 C 紫色 D 绿色
(2)CaCO3中三种元素第一电离能由小到大的顺序是__________ 。CaCO3中的化学键除了σ键外,还存在_________________ 。
(3)关于CO2和CO32-的下列说法正确的是__________ 。
a 两种微粒价层电子对数相同 b 两种微粒的中心原子均无孤电子对
c 键角:CO2>CO32- d 两种微粒的中心原子杂化方式相同
(4)难溶碳酸盐易分解,CaCO3、BaCO3热分解温度更高的是_____ ,原因是______ 。
(5)方解石的菱面体结构如图1,沿三次轴的俯视图为正六边形。方解石的六方晶胞结构如图2,晶胞底面为平行四边形,其较小夹角为60°,边长为a nm,晶胞高为c nm。

A点在俯视图中为a,则B点在俯视图中的位置为_________ (填字母)。方解石的六方晶胞中,Ca2+和CO32-个数比为___________ ;若阿伏加 德罗常数为NA,则该方解石的密度为________ g/cm3(列出计算式)。
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧碳酸钙时的焰色为
A 黄色 B 红色 C 紫色 D 绿色
(2)CaCO3中三种元素第一电离能由小到大的顺序是
(3)关于CO2和CO32-的下列说法正确的是
a 两种微粒价层电子对数相同 b 两种微粒的中心原子均无孤电子对
c 键角:CO2>CO32- d 两种微粒的中心原子杂化方式相同
(4)难溶碳酸盐易分解,CaCO3、BaCO3热分解温度更高的是
(5)方解石的菱面体结构如图1,沿三次轴的俯视图为正六边形。方解石的六方晶胞结构如图2,晶胞底面为平行四边形,其较小夹角为60°,边长为a nm,晶胞高为c nm。

A点在俯视图中为a,则B点在俯视图中的位置为
您最近一年使用:0次
名校
解题方法
6 . Ni元素在生产、生活中有着广泛的应用。 回答下列问题:
(1)基态Ni原子价层电子的排布式为____ 。
(2)科学家在研究金属矿物质组分的过程中,发现了Cu-Ni-Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体最可靠的科学方法是对固体进行_____ 。
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中,第一电离能最大的元素是____ ;(SCN)2分子中,硫原子的杂化方式是____ ,σ键和π键数目之比为_____ 。
(4)[Ni(NH3)6](NO3)2中,不存在的化学键为____ (填标号)。
a.离子键 b.金属键 c.配位键 d.氢键
(5)镍合金储氢的研究已取得很大进展。
①图甲是一种镍基合金储氢后的晶胞结构示意图。 该合金储氢后,含1molLa的合金可吸附H2的数目为_____ 。
②Mg2NiH4是一种贮氢的金属氢化物。在Mg2NiH4晶胞中,Ni原子占据如图乙的顶点和面心,Mg2+处于乙图八个小立方体的体心。Mg2+位于Ni原子形成的___ (填“八面体空隙”或“四面体空隙”)。 若晶体的密度为dg/cm3,Mg2NiH4的摩尔质量为Mg/mol,则Mg2+和Ni原子的最短距离为 ___ nm(用含d、M、NA的代数式表示)。

(1)基态Ni原子价层电子的排布式为
(2)科学家在研究金属矿物质组分的过程中,发现了Cu-Ni-Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体最可靠的科学方法是对固体进行
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中,第一电离能最大的元素是
(4)[Ni(NH3)6](NO3)2中,不存在的化学键为
a.离子键 b.金属键 c.配位键 d.氢键
(5)镍合金储氢的研究已取得很大进展。
①图甲是一种镍基合金储氢后的晶胞结构示意图。 该合金储氢后,含1molLa的合金可吸附H2的数目为
②Mg2NiH4是一种贮氢的金属氢化物。在Mg2NiH4晶胞中,Ni原子占据如图乙的顶点和面心,Mg2+处于乙图八个小立方体的体心。Mg2+位于Ni原子形成的

您最近一年使用:0次
2020-04-14更新
|
360次组卷
|
3卷引用:四川省德阳市2020届高三“二诊”考试(全国III)理综化学试题
名校
解题方法
7 . 铁、钴、镍及化合物在机械制造、磁性材料、新型电池或高效催化剂等许多领域都有着广泛的应用。请回答下列问题:
 基态Ni原子的价电子排布式为
基态Ni原子的价电子排布式为_______ 。镍与CO生成的配合物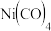 ,
, 中含有的
中含有的 键数目为
键数目为_________ ;写出与CO互为等电子体的阴离子的化学式_________ 。
 研究发现,在
研究发现,在 低压合成甲醇反应
低压合成甲醇反应 中,Co氧化物负载的纳米粒子催化剂具有高活性,显示出良好的应用前景。
中,Co氧化物负载的纳米粒子催化剂具有高活性,显示出良好的应用前景。
 元素Co与O中,第一电离能较大的是
元素Co与O中,第一电离能较大的是_______ 。
 生成物
生成物 与
与 中,沸点较高的是
中,沸点较高的是________ ,原因是___________ 。
 用KCN处理含
用KCN处理含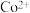 的盐溶液,有红色的
的盐溶液,有红色的 析出,将它溶于过量的KCN溶液后,可生成紫色的
析出,将它溶于过量的KCN溶液后,可生成紫色的 。
。 具有强还原性,在加热时能与水反应生成淡黄色的
具有强还原性,在加热时能与水反应生成淡黄色的 ,写出该反应的离子方程式
,写出该反应的离子方程式____________ 。
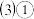 铁有
铁有 、
、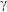 、
、 三种同素异形体
三种同素异形体 如图
如图 ,
, 、
、 两种晶胞中铁原子的配位数之比为
两种晶胞中铁原子的配位数之比为_____ 。

 若Fe原子半径为rpm,
若Fe原子半径为rpm, 表示阿伏加 德罗常数的值,则
表示阿伏加 德罗常数的值,则 单质的密度为
单质的密度为_______ 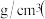 列出算式即可
列出算式即可 。
。
 在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为
在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为 1,
1,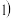 晶面。如图,则
晶面。如图,则 晶胞体中
晶胞体中 1,
1,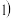 晶面共有
晶面共有_____ 个。

 基态Ni原子的价电子排布式为
基态Ni原子的价电子排布式为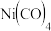 ,
, 中含有的
中含有的 键数目为
键数目为 研究发现,在
研究发现,在 低压合成甲醇反应
低压合成甲醇反应 中,Co氧化物负载的纳米粒子催化剂具有高活性,显示出良好的应用前景。
中,Co氧化物负载的纳米粒子催化剂具有高活性,显示出良好的应用前景。 元素Co与O中,第一电离能较大的是
元素Co与O中,第一电离能较大的是 生成物
生成物 与
与 中,沸点较高的是
中,沸点较高的是 用KCN处理含
用KCN处理含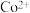 的盐溶液,有红色的
的盐溶液,有红色的 析出,将它溶于过量的KCN溶液后,可生成紫色的
析出,将它溶于过量的KCN溶液后,可生成紫色的 。
。 具有强还原性,在加热时能与水反应生成淡黄色的
具有强还原性,在加热时能与水反应生成淡黄色的 ,写出该反应的离子方程式
,写出该反应的离子方程式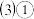 铁有
铁有 、
、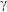 、
、 三种同素异形体
三种同素异形体 如图
如图 ,
, 、
、 两种晶胞中铁原子的配位数之比为
两种晶胞中铁原子的配位数之比为
 若Fe原子半径为rpm,
若Fe原子半径为rpm, 表示阿伏加 德罗常数的值,则
表示阿伏加 德罗常数的值,则 单质的密度为
单质的密度为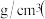 列出算式即可
列出算式即可 。
。 在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为
在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为 1,
1, 晶面。如图,则
晶面。如图,则 晶胞体中
晶胞体中 1,
1, 晶面共有
晶面共有
您最近一年使用:0次
2020-01-27更新
|
547次组卷
|
3卷引用:四川省成都市第七中学2020届高三第一次诊断考试理科综合化学试题
8 . 乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______ ; lmol  中含有的π键数目为
中含有的π键数目为_______ 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为_______ 。
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是_______ ;分子中处于同一直线上的原子数目最多为_______ 。
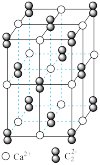
(4)CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),则该晶胞中的碳原子个数为_______ 。 CaC2晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的
的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的 数目为
数目为_______ 。
(1)CaC2中
 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的π键数目为
中含有的π键数目为(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
(4)CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),则该晶胞中的碳原子个数为
 的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的
的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的 数目为
数目为
您最近一年使用:0次
2018-06-03更新
|
486次组卷
|
2卷引用:【全国百强校】四川省双流中学2018届高三考前第二次模拟考试理综-化学试题



