名校
解题方法
1 . 我国力争在2030年前实现“碳达峰”。2060年前实现“碳中和”的目标,因此二氧化碳的固定及转化成了重要的研究课题。
Ⅰ.在 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;
Ⅱ.新型 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。
请回答下列问题:
(1)基态Cu原子的外围电子排布式为___________ ,基态O原子核外有___________ 种不同运动状态的电子。
(2)Ⅰ中涉及的 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是___________ (填化学式)。
(3) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子中含有的 键和
键和 键数目之比为
键数目之比为___________ 。
(4) 反应中,
反应中, 的立体构型为
的立体构型为___________ , 的沸点高于
的沸点高于 的原因是
的原因是___________ 。
(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为___________ 。
②设晶胞边长为anm, 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  。
。
Ⅰ.在
 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;Ⅱ.新型
 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。请回答下列问题:
(1)基态Cu原子的外围电子排布式为
(2)Ⅰ中涉及的
 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是(3)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为 键和
键和 键数目之比为
键数目之比为(4)
 反应中,
反应中, 的立体构型为
的立体构型为 的沸点高于
的沸点高于 的原因是
的原因是(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。
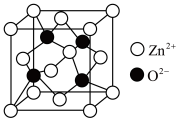
 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为②设晶胞边长为anm,
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 。
。
您最近一年使用:0次
2023-07-30更新
|
973次组卷
|
5卷引用:内蒙古名校联盟2022-2023学年高二下学期期末考试化学试题
内蒙古名校联盟2022-2023学年高二下学期期末考试化学试题江西省吉安市宁冈中学2023-2024学年高三上学期开学考试化学试题黑龙江省牡丹江市第三高级中学2023-2024学年高三上学期第三次月考化学试卷河南省商丘市宁陵县东关高中2023-2024学年高二下学期第一次月考 化学试题(已下线)专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
名校
2 . 教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有_______ 种不同运动状态的电子。
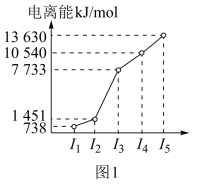
(2)如图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ 。

(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于_______ 晶体。
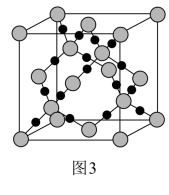
(4)第一电离能介于Al、P之间的第三周期元素有_______ 种。 GaCl3原子的杂化方式为_______ 。写出与GaCl3结构相同的一种等电子体(写离子)_______ 。
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有_______ 个紧邻分子。D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是_______ (填字母标号)。
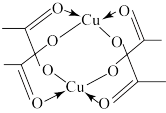
a.极性键 b.非极性键 c.配位键 d.金属键
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有

(2)如图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于

(4)第一电离能介于Al、P之间的第三周期元素有
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有

a.极性键 b.非极性键 c.配位键 d.金属键
您最近一年使用:0次
解题方法
3 . 已知Al、Mg、Na为第三周期元素,其原子的第一至第四电离能如下表:
(1)则Al、Mg、Na的电负性从大到小的顺序为_____________ 。
(2) C、N、O、H是周期表中前10号元素,它们的原子半径依次减小,H能分别与C、N、O形成电子总数相等的分子CH4、NH3、H2O。
①在CH4、NH3、H2O分子中,C、N、O三原子都采取_______ 杂化;
②CH4是含有_____ 键(填“极性”或“非极性”)的____ 分子(填“极性”或“非极性”);
③NH3是一种易液化的气体,请简述其易液化的原因_______ 。
④H2O分子的VSEPR模型的空间构型为_____ ;H2O分子的空间构型为______ 。
(3) K、Cr、 Cu三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1。
①K元素组成的单质的晶体堆积模型为______ (填代号);
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
②Cr元素在其化合物中最高化合价为_____ ;
③Cu2+离子的核外电子排布式为______ ;
| 电离能/kJ‧mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
(1)则Al、Mg、Na的电负性从大到小的顺序为
(2) C、N、O、H是周期表中前10号元素,它们的原子半径依次减小,H能分别与C、N、O形成电子总数相等的分子CH4、NH3、H2O。
①在CH4、NH3、H2O分子中,C、N、O三原子都采取
②CH4是含有
③NH3是一种易液化的气体,请简述其易液化的原因
④H2O分子的VSEPR模型的空间构型为
(3) K、Cr、 Cu三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1。
①K元素组成的单质的晶体堆积模型为
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
②Cr元素在其化合物中最高化合价为
③Cu2+离子的核外电子排布式为
您最近一年使用:0次
4 . A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是______ (填元素符号),其中C原子的核外电子排布式为__________ 。
(2)单质A有两种同素异形体,其中沸点高的是_____ (填分子式),原因是_______ ;A和B的氢化物所属的晶体类型分别为______ 和______ 。
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为______ ,中心原子的杂化轨道类型为______ 。
(4)化合物D2A的立体构型为___ ,中心原子的价层电子对数为______ ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_________ 。
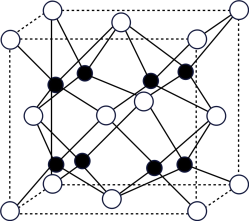
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为______ :晶胞中A原子的配位数为_________ ;列式计算晶体F的密度(g.cm-3)_____ 。
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,F的化学式为

您最近一年使用:0次
2019-01-30更新
|
7103次组卷
|
32卷引用:内蒙古通辽市/科左中旗民族职专·实验高中2023-2024学年高三上学期第二次月考化学试卷
内蒙古通辽市/科左中旗民族职专·实验高中2023-2024学年高三上学期第二次月考化学试卷2015年全国普通高等学校招生统一考试化学(新课标II卷)2016届广东省仲元中学高三11月月考理科综合化学试卷2016届重庆市第一中学高三上12月月考理综化学试卷2016届宁夏六盘山中学高三上第一次模拟理综化学试卷2017届江西省九江市十校高三第二次联考理科综合化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题宁夏六盘山高级中学2017届高三第五次模拟考试理科综合化学试题宁夏石嘴山市第三中学2018届高三9月月考化学试题河北省正定中学2017届高三上学期第三次月考化学试题四川省南充高级中学2018届高三上学期第四次检测理综化学试题山西省临猗县临晋中学2017-2018学年高二下学期期末考试化学试题西藏自治区日喀则市南木林高级中学2019届高三第一次月考理综化学试题河北省唐山市第十一中学2018-2019学年高二下学期期中考试化学试题鲁科版高中化学选修3模块综合测评卷山西省应县第一中学校2018-2019学年高二下学期期中考试化学试题云南省玉溪一中2020届高三上学期期中考试理综化学试题云南省西畴县第二中学2019-2020学年高三上学期期末考试化学试题四川省成都市双流棠湖中学2019-2020学年高二下学期第二次月考化学试题2020届浙江省杭州学军中学高三教学质量监测卷化学试题湖南省长沙市礼雅中学2020届高三下学期三月份网络教学质量监测理科综合化学试题吉林省长春市东北师大附中2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分广东省广州市华南师范大学附属中学2020届高三教学质量监测卷理科综合化学试题广东省深圳外国语学校2021届高三上学期11月月考化学试题四川省成都市北大成都附属实验学校2021届高三上学期12月月考理科综合化学试题广东省2021届高三“六校联盟”第三次联考化学试题四川省成都龙泉中学2021届高三下学期4月月考理科综合化学试题吉林省松原市实验高级中学2021届高三5月月考化学试题(已下线)2020年海南卷化学高考真题变式题15-19山东省德州市2021-2022学年高二下学期物质结构与性质模块综合测评化学试题吉林省汪清县汪清四中2020-2021学年高二下学期期末考试化学试题河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题
名校
5 . 根据物质结构有关性质和特点,回答以下问题:
(1)过渡元素Co 基态原子价电子轨道表达式为_______________________________ 。第四电离能I4 (Co) < I4 (Fe) ,其原因是__________________________________________ 。
(2)磷的氯化物有两种:PCl3和PCl5 ,PCl3中磷原子的杂化类型为__________ ,PCl3的立体构型为__________ ,其中PCl3的沸点________ (填“大于”或“小于”)PCl5,原因是__________ 。
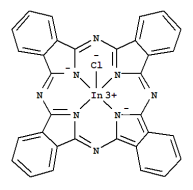
(3)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如下图所示,该分子中存在的化学键为___________ (填选项字母)
a.σ键 b.π键 c.离子键 d.配位键
(4)氯有多种含氧酸,其电离平衡常数如下:
从物质结构的角度解释以上含氧酸 Ka 依次减小的原因________________________ 。
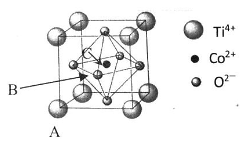
(5)钴的一种化合物的晶胞结构如下图所示:
①已知A点的原子坐标参数为(0,0,0),C 点为(1/2,1/2,1/2),则B点的原子坐标参数为___________ 。
②已知晶胞参数 a = 0.5485 nm,则该晶体的密度为_______________ g/cm3。(列出计算表达式即可)
(1)过渡元素Co 基态原子价电子轨道表达式为
(2)磷的氯化物有两种:PCl3和PCl5 ,PCl3中磷原子的杂化类型为
(3)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如下图所示,该分子中存在的化学键为

a.σ键 b.π键 c.离子键 d.配位键
(4)氯有多种含氧酸,其电离平衡常数如下:
| 化学式 | HClO4 | HClO3 | HClO2 | HClO |
| Ka | 1×1010 | 1×10 | 1×10‾2 | 4×10‾8 |
从物质结构的角度解释以上含氧酸 Ka 依次减小的原因
(5)钴的一种化合物的晶胞结构如下图所示:


①已知A点的原子坐标参数为(0,0,0),C 点为(1/2,1/2,1/2),则B点的原子坐标参数为
②已知晶胞参数 a = 0.5485 nm,则该晶体的密度为
您最近一年使用:0次
2018-11-01更新
|
519次组卷
|
2卷引用:内蒙古巴彦淖尔一中2019届高三上学期第二次月考理综化学试题
名校
6 . 有原子序数依次增大的A、B、C、D、E、F、G七种元素,A元素的原子是周期表中半径最小的原子,B原子最外层电子数是次外层电子数的1.5倍,元素C在自然界中形成物质种类最多,E、F、G三种元素原子的质子数之和为62,E元素原子2p轨道上有两个未成对电子,G元素原子4p轨道上有1个未成对电子,且它的阴离子具有跟氪相同的电子层结构,E、F、G能够形成多种常见的盐。请回答下列问题:
(1)E元素原子的价层电子的电子排布图为________ ;F元素原子基态时的电子排布式:______ ,E、F形成的化合物之一能够与水反应放出气体,写出该化合物与水反应的离子方程式:______ 。
(2)B、D、F均可与G形成化合物
①用电子式表示F、G形成的化合物的过程:__________ 。
②BG3和DG3中心原子的杂化方式分别为__________ 和____________ 。电负性大小关系为B____ D;第一电离能介于B和D之间的第二周期元素有________ 种。
(3)C、E能形成两种常见的化合物,根据等电子原理,写出CE分子的结构式____ 。
(4)由A、C、E形成的气态化合物X,其分子的空间构型是___ ;1 molX分子中σ键的数目为____ ;X可被催化氧化,该反应的催化剂含有Cu、Zn、Ag、Fe等元素。基态Fe原子的电子排布了____________ 个能级,有_________ 个运动状态,在周期表中在_______ 区。向黄色FeCl3溶液中加入无色KSCN溶液,溶液变成红色。该反应在有的教材中用方程式FeCl3+3KSCN==Fe(SCN)3+3KCl表示。生成物中KCl既不是难溶物、难电离的物质,也不是易挥发物质,该反应之所以能进行的原因是___________ 。经研究表明Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合。
①所得Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显红色。该配合物离子的化学式是__________________ 。
②若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为___________ 。
(1)E元素原子的价层电子的电子排布图为
(2)B、D、F均可与G形成化合物
①用电子式表示F、G形成的化合物的过程:
②BG3和DG3中心原子的杂化方式分别为
(3)C、E能形成两种常见的化合物,根据等电子原理,写出CE分子的结构式
(4)由A、C、E形成的气态化合物X,其分子的空间构型是
①所得Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显红色。该配合物离子的化学式是
②若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为
您最近一年使用:0次
2018-01-30更新
|
220次组卷
|
2卷引用:内蒙古赤峰二中2017-2018学年高二上学期期末考试化学试题



