解题方法
1 . 下列关于 、
、 、
、 三种微粒的说法不正确
三种微粒的说法不正确
 、
、 、
、 三种微粒的说法不正确
三种微粒的说法不正确| A.三种微粒所含有的电子数相等 | B.三种微粒中氮原子的杂化方式相同 |
| C.三种微粒的VSEPR模型相同 | D.键角大小关系: |
您最近一年使用:0次
解题方法
2 . 下列各组粒子的中心原子杂化类型相同,其键角不相等的是
A. | B. |
C. 、环己烷 、环己烷 | D. (苯)、 (苯)、 |
您最近一年使用:0次
3 . 下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是
① ②
② ③
③ ④
④ ⑤
⑤
①
 ②
② ③
③ ④
④ ⑤
⑤
| A.①③④⑤ | B.①②③⑤ | C.①③⑤ | D.①②③④⑤ |
您最近一年使用:0次
名校
4 . 下列说法正确的有个
①价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
②所有σ键强度都大于π键
③杂化轨道只用于形成共价键
④只要分子的空间结构为平面三角形,中心原子均为sp2杂化
⑤NH3与H3O+的VSEPR构型均为四面体形,二者空间结构一致
⑥p能级能量一定比s能级的能量高
①价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
②所有σ键强度都大于π键
③杂化轨道只用于形成共价键
④只要分子的空间结构为平面三角形,中心原子均为sp2杂化
⑤NH3与H3O+的VSEPR构型均为四面体形,二者空间结构一致
⑥p能级能量一定比s能级的能量高
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法中不正确的是
| A.X射线衍射实验可以区分晶体和非晶体,也可以获得晶体的键长和键角的数值 |
| B.价层电子对互斥模型一般不用于预测以过渡金属为中心原子的分子空间结构 |
| C.杂化轨道用于形成σ键或用来容纳未参与成键的孤电子对,未参与杂化的p轨道可用于形成π键 |
D.链一元有机酸 (R-是直链烷基)中,烷基是推电子基团,烷基越长羧酸的酸性越强 (R-是直链烷基)中,烷基是推电子基团,烷基越长羧酸的酸性越强 |
您最近一年使用:0次
2023-02-17更新
|
694次组卷
|
4卷引用:内蒙古赤峰新城红旗中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
6 . 下列有关 、
、 、
、 、
、 的说法正确的是
的说法正确的是
 、
、 、
、 、
、 的说法正确的是
的说法正确的是A. 和 和 中的键角 中的键角 前者大 前者大 |
B. 和 和 的空间构型相同 的空间构型相同 |
C. 和 和 中N原子的杂化方式相同 中N原子的杂化方式相同 |
D. 与 与 形成的 形成的 中,提供孤电子对形成配位键的是 中,提供孤电子对形成配位键的是 |
您最近一年使用:0次
2022-05-05更新
|
743次组卷
|
4卷引用:内蒙古通辽市重点学校2022-2023学年高二下学期3月质量检测化学试题
内蒙古通辽市重点学校2022-2023学年高二下学期3月质量检测化学试题山东省聊城市2022届高三二模化学试题辽宁省实验中学2022届高三考前模拟训练化学试题(已下线)微专题50 分子的立体结构的判断-备战2023年高考化学一轮复习考点微专题
解题方法
7 . O、S、Cl、Cr、Cu五种元素的单质及其化合物在工农业生产和生活中有着广泛的应用。请回答下列问题:
(1)Cr元素有_______ 种不同运动状态的电子,基态Cr原子价层电子的排布式为_______ 。
(2)O、S、C的电负性由大到小的顺序是_______ (填元素符号)。
(3)O、S的最简单氢化物中键角较大的是_______ (填化学式),原因是_______ 。
(4) 的立体构型为
的立体构型为_______ 。
(5)O、Cu组成的一种化合物的晶胞结构示意图如下。
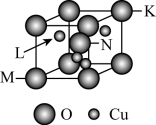
①该化合物的化学式为_______ 。
②晶胞边长:描述晶胞的大小和形状。若晶胞边长为a nm,设 为阿伏加德罗常数的值,该化合物的密度为
为阿伏加德罗常数的值,该化合物的密度为_______ (用含a、 的代数式表示)
的代数式表示) 。
。
(1)Cr元素有
(2)O、S、C的电负性由大到小的顺序是
(3)O、S的最简单氢化物中键角较大的是
(4)
 的立体构型为
的立体构型为(5)O、Cu组成的一种化合物的晶胞结构示意图如下。

①该化合物的化学式为
②晶胞边长:描述晶胞的大小和形状。若晶胞边长为a nm,设
 为阿伏加德罗常数的值,该化合物的密度为
为阿伏加德罗常数的值,该化合物的密度为 的代数式表示)
的代数式表示) 。
。
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、W、R是元素周期表前四周期元素中的五种常见元素,其原子序数依次增大。X的基态原子的最外层电子排布式为nsnnpn+1。Y、Z同主族且ZY2是导致酸雨的主要物质之一。R位于ds区且原子最外层只有一个电子。W原子次外层电子数为最外层电子数的7倍。回答下列问题:
(1)W在元素周期表中的位置是____ ,其基态原子的价电子排布图为____ 。
(2)Y的气态氢化物稳定性比Z的气态氢化物的稳定性____ (填“强”或“弱”)。Y的第一电离能比X的____ (填“大”或“小”)。
(3)X的最常见的气体氢化物分子的VSEPR模型为____ ,分子的空间构型是____ 。
(4)原子总数相同、价电子总数相同的分子或离子称为等电子体。分别写出一种与XO 互为等电子体的单质和化合物的化学式
互为等电子体的单质和化合物的化学式____ 、____ 。
(1)W在元素周期表中的位置是
(2)Y的气态氢化物稳定性比Z的气态氢化物的稳定性
(3)X的最常见的气体氢化物分子的VSEPR模型为
(4)原子总数相同、价电子总数相同的分子或离子称为等电子体。分别写出一种与XO
 互为等电子体的单质和化合物的化学式
互为等电子体的单质和化合物的化学式
您最近一年使用:0次
2022-04-08更新
|
144次组卷
|
2卷引用:内蒙古赤峰市元宝山区第一中学2021-2022学年高二下学期4月月考化学试题
名校
9 . 有下列微粒:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ,填下列空白(填序号):
,填下列空白(填序号):
(1)呈正四面体的是_______ 。
(2)中心原子轨道为sp杂化的是_______ ,为 杂化的是
杂化的是_______ 。
(3)只含有极性键的非极性分子为_______ 。
(4)VSEPR模型为平面三角形的有_______ 。
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ,填下列空白(填序号):
,填下列空白(填序号):(1)呈正四面体的是
(2)中心原子轨道为sp杂化的是
 杂化的是
杂化的是(3)只含有极性键的非极性分子为
(4)VSEPR模型为平面三角形的有
您最近一年使用:0次
解题方法
10 . 氮化硼(BN)是-种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
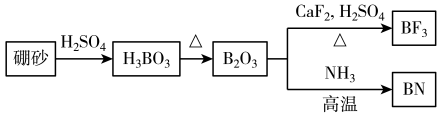
请回答下列问题:
(1) 在BF3分子中,F-B-F的键角是_____ ,B原子的杂化轨道类型为_____ ,BF3和过量NaF作用可生成NaBF4, 的立体结构为
的立体结构为______ 。
(2)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为_____ (填“极性键”或“非极性键”),层间作用力为_____ 。

请回答下列问题:
(1) 在BF3分子中,F-B-F的键角是
 的立体结构为
的立体结构为(2)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
您最近一年使用:0次



