名校
解题方法
1 . 我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排式为___________ ;单晶硅的晶体类型为___________ 。SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为___________ 。
(2)SiCl4可发生水解反应,机理如下:
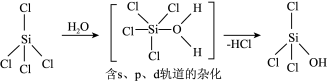
含s、p、d轨道的杂化类型有:①dsp2②sp3d③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为___________ (填标号)。
(3)CS2分子中存在___________ 个σ键和___________ 个π键。
(4)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___________ 。
(5)FeCO3的阴离子的空间构型为___________ ,写出一种与该阴离子互为等电子体的分子的化学式___________ 。
(6)工业上常用羰基镍[Ni(CO)4]制备高纯镍,其熔点-19°C,沸点43℃,试分析晶体中σ键与π键数目的比值为___________ ,羰基镍属于___________ 晶体。已知钛和铝的相对原子半径分别是1.45和1.43,钛的硬度比铝大的原因是___________ 。
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排式为
(2)SiCl4可发生水解反应,机理如下:

含s、p、d轨道的杂化类型有:①dsp2②sp3d③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(3)CS2分子中存在
(4)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(5)FeCO3的阴离子的空间构型为
(6)工业上常用羰基镍[Ni(CO)4]制备高纯镍,其熔点-19°C,沸点43℃,试分析晶体中σ键与π键数目的比值为
您最近一年使用:0次
2 . 人们长期以来一直认为氟的含氧酸不存在。但是1971年斯图尔杰和阿佩曼成功地合成次氟酸后,这种论点被剧烈地动摇了。他们是在0℃以下将氟化物从细冰末的上面通过,得到毫克量的次氟酸。
(1)以下两种结构式,能正确地表示次氟酸的结构的是___________ ;
A. B.
B.
(2)次氟酸中氧元素的化合价是_____ ,次氟酸的电子式为_____ ,次氟酸的分子中共价键的键角____ (填“>”“<”或“=”)180°。
(1)以下两种结构式,能正确地表示次氟酸的结构的是
A.
 B.
B.
(2)次氟酸中氧元素的化合价是
您最近一年使用:0次
3 . 碳族元素包括:C、Si、 Ge、 Sn、Pb。
(1)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过____ 杂化与周围碳原子成键,多层碳纳米管的层与层之间靠____ 结合在一起。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为____ 。
(3)用价层电子对互斥理论推断SnBr2分子中Sn—Br的键角___ 120°(填“>”“<”或“=”)。
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为_______ ,每个Ba2+与____ 个O2-配位。
(1)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(3)用价层电子对互斥理论推断SnBr2分子中Sn—Br的键角
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为
您最近一年使用:0次
2019-01-30更新
|
937次组卷
|
7卷引用:2015-2016学年四川省雅安天全中学高二上学期11月月考化学试卷
名校
4 . 在HF、H2O、NH3、CS2、CH4、N2、BF3分子中:
(1)以非极性键结合的非极性分子是________ ;
(2)以极性键结合的具有直线形结构的非极性分子是________ ;
(3)以极性键结合的具有正四面体形结构的非极性分子是________ ;
(4)以极性键结合的具有三角锥形结构的极性分子是________ ;
(5)以极性键结合的具有sp3杂化轨道结构的分子是________ ;
(6)以极性键结合的具有sp2杂化轨道结构的分子是________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键结合的具有直线形结构的非极性分子是
(3)以极性键结合的具有正四面体形结构的非极性分子是
(4)以极性键结合的具有三角锥形结构的极性分子是
(5)以极性键结合的具有sp3杂化轨道结构的分子是
(6)以极性键结合的具有sp2杂化轨道结构的分子是
您最近一年使用:0次
2018-04-24更新
|
520次组卷
|
6卷引用:四川省南充高级中学2020-2021学年高二上学期第二次月考化学试题
四川省南充高级中学2020-2021学年高二上学期第二次月考化学试题宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 学科素养提升鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第2章学科素养提升(已下线)2.3.1 共价键的极性 范德华力-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)第二章 分子结构与性质(A卷)
名校
5 . (1)NH3、N2H4在工业生产和国防建设中都有广泛应用。
①N2H4(g) N2(g)+2H2(g) △H1=akJ·mol-1
N2(g)+2H2(g) △H1=akJ·mol-1
②N2(g)+3H2(g) 2NH3(g) △H2=bkJ·mol-1
2NH3(g) △H2=bkJ·mol-1
③7N2H4(g) 8NH3(g)+3N2(g)+2H2(g) △H3
8NH3(g)+3N2(g)+2H2(g) △H3
则△H3=_________ (用含a和b的代数式表示)
(2)N2中存在_________ 键(填“极性”或“非极性”),NH3的VSEPR模型是______________ 。用短线表示共价键,小黑点表示孤对电子的结构式叫路易斯结构式,NH4的路易斯结构式为______________ 。
①N2H4(g)
 N2(g)+2H2(g) △H1=akJ·mol-1
N2(g)+2H2(g) △H1=akJ·mol-1②N2(g)+3H2(g)
 2NH3(g) △H2=bkJ·mol-1
2NH3(g) △H2=bkJ·mol-1③7N2H4(g)
 8NH3(g)+3N2(g)+2H2(g) △H3
8NH3(g)+3N2(g)+2H2(g) △H3则△H3=
(2)N2中存在
您最近一年使用:0次
6 . 下表中实线是元素周期表的部分边界,其中上边界并未用实线画出。
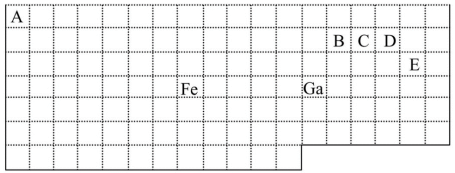
根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为_________________ 。
(2)铁元素位于元素周期表的________ 区;Fe和CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为__________ 。
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO互为等电子体的分子和离子分别为_______ 和______ (填化学式)。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有__________ 。
(5)根据VSEPR模型预测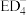 的空间构型为
的空间构型为__________ 。

根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为
(2)铁元素位于元素周期表的
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO互为等电子体的分子和离子分别为
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有
(5)根据VSEPR模型预测
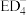 的空间构型为
的空间构型为
您最近一年使用:0次
2017-07-08更新
|
161次组卷
|
2卷引用:四川省巴中市平昌县博雅学校2021-2022学年高二上学期第二次月考化学试题
填空题
|
适中(0.65)
|
7 . 硒化锌是一种透明黄色半导体,也可作红外光学材料,熔点1520℃。
(1)基态锌原子的价电子排布式是
(2)根据元素周期律,电负性Se
(3)H2Se的分子构型是
(4)H2O的沸点
(5)晶体Zn为六方最密堆积,其配位数是
(6)在硒化锌ZnSe晶胞中,Se2—离子作面心立方最密堆积,且Se2—与Se2—之间的最短距离为a nm,则晶胞边长为
(7)假设阿伏伽德罗常数值为NA,则144g 硒化锌ZnSe晶体中的晶胞数是
您最近一年使用:0次
解题方法
8 . 比较下列各项中的前者和后者,用“>”、“<”、或“=”填空
(1)沸点: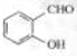

(2)在水中的溶解度:CH3CH2OHCH3(CH3)2CH2OH
(3)酸性:HClO3HClO4
(4)键长:H-OH-S
(5)未成对电子数:OCr
(1)沸点:


(2)在水中的溶解度:CH3CH2OHCH3(CH3)2CH2OH
(3)酸性:HClO3HClO4
(4)键长:H-OH-S
(5)未成对电子数:OCr
您最近一年使用:0次




