名校
解题方法
1 . 硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液,回答下列问题:
(1)基态Ni2+的电子排布式为_______ 。
(2)①在1mol[Ni(NH3)6]2+中含有σ键的数目为_______ 。
②Ni、N、O三种元素的第一电离能由小到大的顺序是为_____ 。
③液氨中存在电离平衡2NH3⇌NH + NH
+ NH ,根据价层电子对互斥理论,可推知NH2—的空间构型为
,根据价层电子对互斥理论,可推知NH2—的空间构型为_______ ,液氨体系内,氮原子的杂化轨道类型为_____ 。NH3比PH3更容易液化的原因为_____ 。
(3)氧化镍晶胞如图所示,镍离子的配位数为_______ 。
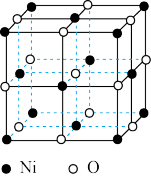
已知晶胞参数为a cm,NA为阿伏加德罗常数的值,则氧化镍晶体密度为______ g/cm3。
(1)基态Ni2+的电子排布式为
(2)①在1mol[Ni(NH3)6]2+中含有σ键的数目为
②Ni、N、O三种元素的第一电离能由小到大的顺序是为
③液氨中存在电离平衡2NH3⇌NH
 + NH
+ NH ,根据价层电子对互斥理论,可推知NH2—的空间构型为
,根据价层电子对互斥理论,可推知NH2—的空间构型为(3)氧化镍晶胞如图所示,镍离子的配位数为

已知晶胞参数为a cm,NA为阿伏加德罗常数的值,则氧化镍晶体密度为
您最近一年使用:0次
解题方法
2 . 钛被称为“国防金属”。目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:2FeTiO3+7Cl2+6C 2TiCl4+2FeCl3+6CO;TiO2+2Cl2+2C
2TiCl4+2FeCl3+6CO;TiO2+2Cl2+2C TiCl4+2CO。将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:TiCl4+2Mg
TiCl4+2CO。将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:TiCl4+2Mg Ti+2MgCl2。
Ti+2MgCl2。
(1)基态钛原子的电子排布式为____ 。
(2)与CO互为等电子体的阴离子为___ (填化学式)。
(3)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于____ (填“原子”“分子”或“离子”)晶体。
(4)TiO2+与H2O2在稀HNO3中反应生成橘红色的[TiO(H2O2)]2+离子,可用于钛的定性检验。
① 空间构型为
空间构型为_____________ 。
②H2O2中O原子轨道杂化类型为______________ 。
(5)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为____ 。

 2TiCl4+2FeCl3+6CO;TiO2+2Cl2+2C
2TiCl4+2FeCl3+6CO;TiO2+2Cl2+2C TiCl4+2CO。将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:TiCl4+2Mg
TiCl4+2CO。将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:TiCl4+2Mg Ti+2MgCl2。
Ti+2MgCl2。(1)基态钛原子的电子排布式为
(2)与CO互为等电子体的阴离子为
(3)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于
(4)TiO2+与H2O2在稀HNO3中反应生成橘红色的[TiO(H2O2)]2+离子,可用于钛的定性检验。
①
 空间构型为
空间构型为②H2O2中O原子轨道杂化类型为
(5)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为

您最近一年使用:0次
解题方法
3 . 东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电子排布式为________ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____________ 。
②1 mol [Ni(NH3)6]2+含有σ键为___ mol。
③氨的沸点高于膦(PH3),原因是________ 。
(3)某镍白铜合金的立方晶胞结构如图所示,该合金的化学式为________ 。

(1)镍元素基态原子的价电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②1 mol [Ni(NH3)6]2+含有σ键为
③氨的沸点高于膦(PH3),原因是
(3)某镍白铜合金的立方晶胞结构如图所示,该合金的化学式为

您最近一年使用:0次
名校
解题方法
4 . 中国海军航母建设正在有计划、有步骤向前推进,第一艘国产航母目前正在进行海试。 建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外亮要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,Ni2+基态原子的核外电子排布为____________ ,铬元素在周期表中______________ 区。
(2)航母甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中C原子的杂化方式为______ 杂化。

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
根据价层电子对互斥理论,预测ClO 的空间构型为
的空间构型为___________ 形,写出一个ClO 的等电子体的化学符号
的等电子体的化学符号____________ 。
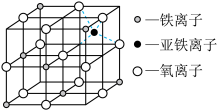
(4)海底金属软泥是在洋海底覆盖着的层红棕色沉积物, 蕴藏着大量的资源,含有硅、铁、锰、锌等。如图是从铁氧体离子形成的晶胞,写该晶体的化学式______ 。
(1)镍铬钢抗腐蚀性能强,Ni2+基态原子的核外电子排布为
(2)航母甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中C原子的杂化方式为

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
根据价层电子对互斥理论,预测ClO
 的空间构型为
的空间构型为 的等电子体的化学符号
的等电子体的化学符号
(4)海底金属软泥是在洋海底覆盖着的层红棕色沉积物, 蕴藏着大量的资源,含有硅、铁、锰、锌等。如图是从铁氧体离子形成的晶胞,写该晶体的化学式
您最近一年使用:0次
5 . (1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得一种铜锰氧化物。
①Cu基态原子的电子排布式可表示为_____ ;
② 的空间构型是
的空间构型是_____ (用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O。
①根据等电子体原理,CO分子的结构式为_____ ;
②HCHO分子中C原子轨道的杂化类型为_____ ;
③1molCO2中含有的σ键数目为_____ 。
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为_____ 。
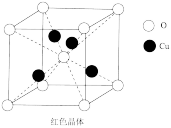
(4)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图。则该化合物的化学式是_____ 。
①Cu基态原子的电子排布式可表示为
②
 的空间构型是
的空间构型是(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O。
①根据等电子体原理,CO分子的结构式为
②HCHO分子中C原子轨道的杂化类型为
③1molCO2中含有的σ键数目为
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
(4)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图。则该化合物的化学式是

您最近一年使用:0次
名校
解题方法
6 . 氮及其化合物在生产生活中应用广泛。回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式___ ;基态铬、氮原子的核外未成对电子数之比为___ 。
(2)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为___ ,过硫酸铵的阳离子的空间构型为___ 。
(3) 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为__ ,CP的中心Co3+的配位数为___ 。
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式
(2)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为
(3)
 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为
您最近一年使用:0次
名校
解题方法
7 . 原子序数小于36的X、Y、Z、W、R五种元素,原子序数依次增大。五种元素中,仅R为金属元素,其原子序数为27。X价电子排布式为nsnnpn,元素Z基态原子s电子总数与p电子总数相等,W与其它四种元素能层数不同,且未成对电子数目为1个。根据判断出的元素回答下列问题:
(1)R2+离子核外电子排布式为________ ,X、Y、Z三种原子第一电离能由小到大的顺序为________ (用具体元素符号表示)。
(2)1 mol配合物[R(XY)6]4-中含有σ键的数目为________ 。
(3)XZW2是一种高毒类物质,结构与甲醛(HCHO)相似,其沸点高于甲醛的主要原因是________ 。
(4)YW3为黄色、油状、具有刺激性气味的液体,该分子的立体构型为________ (用文字描述)。
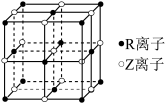
(5)某晶体的晶胞结构如图所示,则该化合物的化学式为________ (R、Z用具体元素符号表示)。
(1)R2+离子核外电子排布式为
(2)1 mol配合物[R(XY)6]4-中含有σ键的数目为
(3)XZW2是一种高毒类物质,结构与甲醛(HCHO)相似,其沸点高于甲醛的主要原因是
(4)YW3为黄色、油状、具有刺激性气味的液体,该分子的立体构型为
(5)某晶体的晶胞结构如图所示,则该化合物的化学式为

您最近一年使用:0次
解题方法
8 . 硝酸工业尾气中含有NO,可以利用强氧化剂过硫酸钠(Na2S2O8)氧化脱除NO,可以消除污染。
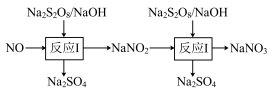
(1)NO3-空间构型为__________ 。
(2)O、N、S三种元素的第一电离能由小到大的顺序为____________ 。
(3)在反应2中,NO2-的初始浓度为0.1 mol·L-1,反应为NO2-+S2O82-+2OH- NO3-+2SO42-+H2O。不同温度下,达到平衡时NO2-的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图1所示。
NO3-+2SO42-+H2O。不同温度下,达到平衡时NO2-的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图1所示。

图中点a、点b和点c的平衡常数K的大小关系____ 。
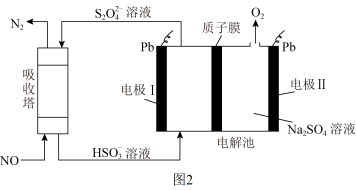
(4)间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图2所示,质子膜允许H+和H2O通过。电极 Ⅰ 的电极反应式为____ ,每处理1 mol NO,可同时得到____ g O2。

(1)NO3-空间构型为
(2)O、N、S三种元素的第一电离能由小到大的顺序为
(3)在反应2中,NO2-的初始浓度为0.1 mol·L-1,反应为NO2-+S2O82-+2OH-
 NO3-+2SO42-+H2O。不同温度下,达到平衡时NO2-的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图1所示。
NO3-+2SO42-+H2O。不同温度下,达到平衡时NO2-的脱除率与过硫酸钠(Na2S2O8)初始浓度的关系如图1所示。

图中点a、点b和点c的平衡常数K的大小关系
(4)间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图2所示,质子膜允许H+和H2O通过。电极 Ⅰ 的电极反应式为
您最近一年使用:0次
9 . 高温炼铜的反应之一为2CuFeS2+O2 Cu2S+2FeS+SO2。
Cu2S+2FeS+SO2。
(1) Cu+基态核外电子排布式为________________ 。
(2) Cu、Zn的第二电离能:I2(Cu)________ (填“>”“<”或“=”)I2(Zn)。
(3) SO2分子中S原子的轨道杂化类型为________ ,分子的空间构型为________ ,与SO2互为等电子体的分子有________ (写一种)。
(4) [Cu(CH3CN)4]+是非常稳定的络合离子,配体中σ键和π键个数之比为________ 。
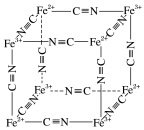
(5) Fe2+、Fe3+能与CN-络合,其结构如图所示。该离子可形成铁蓝钾盐,该钾盐的化学式为________ 。
 Cu2S+2FeS+SO2。
Cu2S+2FeS+SO2。(1) Cu+基态核外电子排布式为

(2) Cu、Zn的第二电离能:I2(Cu)
(3) SO2分子中S原子的轨道杂化类型为
(4) [Cu(CH3CN)4]+是非常稳定的络合离子,配体中σ键和π键个数之比为
(5) Fe2+、Fe3+能与CN-络合,其结构如图所示。该离子可形成铁蓝钾盐,该钾盐的化学式为
您最近一年使用:0次
名校
解题方法
10 . 锰、砷、镓及其相关化合物用途非常广泛。
(1)Mn2+基态核外电子排布式为__________ 。
(2)砷与镓、硒是同周期的主族元素,其第一电离能从小到大的顺序是__________ 。
(3)BrCH2CN可用于制备砷叶立德,BrCH2CN 分子中碳原子杂化轨道类型是__________ 。
(4)在AlCl3存在下,将C2H2通入AsCl3可得到(ClCH=CH)2AsCl等物质,AsCl3分子的几何构型为__________ ,1mol(ClCH=CH)2AsCl分子中含σ键的数目为__________ 。
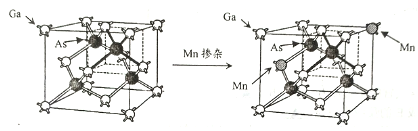
(5)GaAs是一种重要的半导体材料,按图示掺杂锰后可得稀磁性半导体材料(晶体结构不变),则该材料晶体中n(Ga) ∶n(Mn) ∶n(As)=__________ 。
(1)Mn2+基态核外电子排布式为
(2)砷与镓、硒是同周期的主族元素,其第一电离能从小到大的顺序是
(3)BrCH2CN可用于制备砷叶立德,BrCH2CN 分子中碳原子杂化轨道类型是
(4)在AlCl3存在下,将C2H2通入AsCl3可得到(ClCH=CH)2AsCl等物质,AsCl3分子的几何构型为
(5)GaAs是一种重要的半导体材料,按图示掺杂锰后可得稀磁性半导体材料(晶体结构不变),则该材料晶体中n(Ga) ∶n(Mn) ∶n(As)=

您最近一年使用:0次
2018-05-17更新
|
302次组卷
|
2卷引用:【全国市级联考】江苏省盐城市2018届高三第三次模拟考试化学试题



