解题方法
1 . 已知X、Y、Z、W、R是元素周期表前四周期中原子序数依次增大的常见元素,相关信息如下表:
(1)X基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(2) 是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为
是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为___________ 。
(3)Z的基态原子的电子排布式为___________ 。
(4)H2Y的中心原子采取___________ 杂化,VSEPR模型为___________ ,分子构型为___________ 。
| 元素 | 相关信息 |
| X | 元素原子的核外p电子数比s电子数少1 |
| Y | 地壳中含量最多的元素 |
| Z | 第一电离能至第四电离能分别是: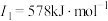 , , , ,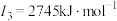 , ,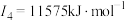 |
| W | 前四周期中电负性最小的元素 |
| R | 在周期表的第十一列 |
(2)
 是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为
是动物和人体所必需的微量元素之一,也是重要的工业原料,与Y同族。Se的原子结构示意图为(3)Z的基态原子的电子排布式为
(4)H2Y的中心原子采取
您最近一年使用:0次
名校
2 . 下列化学用语表达错误的是
A. 分子中σ键的电子云轮廓图: 分子中σ键的电子云轮廓图: |
B. 分子的VSEPR模型:四面体形 分子的VSEPR模型:四面体形 |
C. 的空间填充模型: 的空间填充模型: |
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂: |
您最近一年使用:0次
名校
3 . 请回答下列问题:
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
(2)第四周期主族元素中,第一电离能介于Ga、As之间的元素有___________ 种。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是___________ 。
(4)氧是地壳中含量最多的元素。H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因为___________ 。
(5)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是___________ 。
②若该晶胞的晶胞边长为d nm,则该合金的密度为___________  。(不用化简)
。(不用化简)
③若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下H2的体积约为__________ 。
(1)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
| A.1s22s22p43s1 | B.1s22s22p43d2 | C.1s22s22p5 | D.1s22s22p6 |
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
| 电离能/kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(4)氧是地壳中含量最多的元素。H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因为
(5)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是
②若该晶胞的晶胞边长为d nm,则该合金的密度为
 。(不用化简)
。(不用化简)③若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下H2的体积约为
您最近一年使用:0次
名校
解题方法
4 . 下表为周期表的一部分,其中的编号代表对应的元素。请回答下列问题:
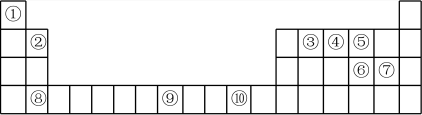
(1)表中属于d区的元素是_____ (填序号)。
(2)写出元素⑨的基态原子的核外电子排布式_____ ,元素⑩的价电子轨道表示式_____ 。
(3)表中所给元素中,原子半径最大的是_____ (填元素符号),元素⑥、⑦形成的简单离子半径更小的是_____ (填离子符号)。
(4)下列关于元素③、④分别与①形成的简单化合物的叙述正确的是_____(填序号)。
(5)元素④、⑤的第一电离更大的是_____ (填元素符号)。
(6)元素②与元素⑦形成的分子的空间结构为_____ 。

(1)表中属于d区的元素是
(2)写出元素⑨的基态原子的核外电子排布式
(3)表中所给元素中,原子半径最大的是
(4)下列关于元素③、④分别与①形成的简单化合物的叙述正确的是_____(填序号)。
| A.中心原子的价层电子对数相同 |
| B.中心原子的杂化方式不同 |
| C.分子的VSEPR模型相同,空间结构也相同 |
| D.④与①形成的分子的键角比③与①形成的分子的键角更大 |
(5)元素④、⑤的第一电离更大的是
(6)元素②与元素⑦形成的分子的空间结构为
您最近一年使用:0次
2023-12-12更新
|
583次组卷
|
2卷引用:黑龙江省大庆市肇州县第二中学2023-2024学年高二上学期12月月考化学试题
名校
5 . 反应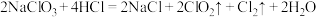 可制含氯消毒剂。下列说法正确的是
可制含氯消毒剂。下列说法正确的是
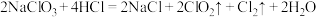 可制含氯消毒剂。下列说法正确的是
可制含氯消毒剂。下列说法正确的是| A.HCl和NaCl所含化学键类型相同 |
B. 是由极性键构成的非极性分子 是由极性键构成的非极性分子 |
C. 的空间结构为三角锥形 的空间结构为三角锥形 |
D.中子数为18的Cl原子: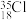 |
您最近一年使用:0次
2023-11-20更新
|
559次组卷
|
5卷引用:黑龙江省大庆市肇州县第二中学2023-2024学年高二上学期12月月考化学试题
黑龙江省大庆市肇州县第二中学2023-2024学年高二上学期12月月考化学试题江苏省南通市海安市2023-2024学年高三上学期11月期中化学试题(已下线)江苏省南通市海安高级中学2023-2024学年高三上学期期中考试化学试题江苏省南京市金陵中学2023-2024学年高三上学期期中学业质量监测 化学试卷辽宁省昌图县第一高级中学2023-2024学年高二上学期12月月考化学试卷
名校
解题方法
6 . 元素A、B、C、D、E、F、G在元素周期表中的位置如图所示,回答下列问题:

(1) 的基态原子核外电子排布式为
的基态原子核外电子排布式为___________ 。原子的第一电离能:D___________ E(填“>”或“<”)。
(2)根据价层电子对互斥理论,价层电子对之间的斥力大小有如下顺序: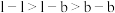 (l为孤电子对,
(l为孤电子对, 为键合电子对),则关于
为键合电子对),则关于 中的
中的 键角可得出的结论是___________。
键角可得出的结论是___________。
(3)化合物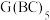 中存在的化学键类型有
中存在的化学键类型有___________ ,它在空气中燃烧生成红棕色氧化物,反应的化学方程式为___________ 。
(4)化合物 的立体构型为
的立体构型为___________ ,其中B原子的杂化轨道类型是___________ ,写出两个与 具有相同立体构型的含氧酸根离子
具有相同立体构型的含氧酸根离子___________ 。

(1)
 的基态原子核外电子排布式为
的基态原子核外电子排布式为(2)根据价层电子对互斥理论,价层电子对之间的斥力大小有如下顺序:
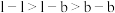 (l为孤电子对,
(l为孤电子对, 为键合电子对),则关于
为键合电子对),则关于 中的
中的 键角可得出的结论是___________。
键角可得出的结论是___________。A. | B.接近 ,但小于 ,但小于 |
C.接近 ,但大于 ,但大于 | D.接近 ,但小于 ,但小于 |
(3)化合物
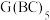 中存在的化学键类型有
中存在的化学键类型有(4)化合物
 的立体构型为
的立体构型为 具有相同立体构型的含氧酸根离子
具有相同立体构型的含氧酸根离子
您最近一年使用:0次
解题方法
7 . 下列化学用语错误的是
A.HClO的电离方程式: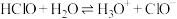 |
B.基态Se原子的价层电子排布式: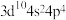 |
C. 的VSEPR模型: 的VSEPR模型: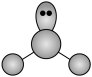 |
| D.基态Na原子核外电子占据的最高能级的电子云轮廓图的形状:球形 |
您最近一年使用:0次
2023-07-24更新
|
250次组卷
|
3卷引用:黑龙江省大庆市2023-2024学年高三上学期第一次教学质量检测化学试题
名校
8 . X、Y、Z、W为原子序数依次增大的前四周期主族元素,X的价电子构型为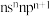 ;Z第一电离能最大;W与X位于同一主族,其某种氧化物有剧毒。下列说法不正确的是
;Z第一电离能最大;W与X位于同一主族,其某种氧化物有剧毒。下列说法不正确的是
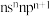 ;Z第一电离能最大;W与X位于同一主族,其某种氧化物有剧毒。下列说法不正确的是
;Z第一电离能最大;W与X位于同一主族,其某种氧化物有剧毒。下列说法不正确的是A.X、Y、Z简单氢化物的沸点: |
B. 分子的空间结构为三角锥形 分子的空间结构为三角锥形 |
| C.X、W简单氢化物的键角W<X |
D. 离子的空间结构为正八面体 离子的空间结构为正八面体 |
您最近一年使用:0次
9 . 科学家发现对LiTFSI(一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。LiTFSI的结构如图,X、Y、Z、M为同一短周期元素,Z与W位于同一主族。下列叙述正确的是
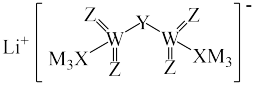

A.元素电负性: |
B.第一电离能: |
C. 、 、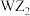 的VSEPR模型均为直线形 的VSEPR模型均为直线形 |
| D.M的简单氢化物的沸点一定高于X的氢化物 |
您最近一年使用:0次
名校
解题方法
10 .  (砒霜)是两性氧化物,分子结构如图所示,与盐酸反应能生成
(砒霜)是两性氧化物,分子结构如图所示,与盐酸反应能生成 ,
, 和
和 反应的产物之一为
反应的产物之一为 。下列说法错误的是
。下列说法错误的是
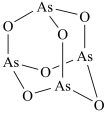
 (砒霜)是两性氧化物,分子结构如图所示,与盐酸反应能生成
(砒霜)是两性氧化物,分子结构如图所示,与盐酸反应能生成 ,
, 和
和 反应的产物之一为
反应的产物之一为 。下列说法错误的是
。下列说法错误的是
A. 分子中As原子的杂化方式为 分子中As原子的杂化方式为 |
B. 的分子空间构型为平面正三角形 的分子空间构型为平面正三角形 |
C. 的价层电子对互斥模型是四面体形 的价层电子对互斥模型是四面体形 |
D. 分子的键角小于 分子的键角小于 |
您最近一年使用:0次
2023-07-06更新
|
505次组卷
|
4卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题



