名校
解题方法
1 . 氮(N)形成的单质及它形成的化合物有重要的研究和应用价值,回答下列问题:
(1)已知NO 与CO2互为等电子体,NO
与CO2互为等电子体,NO 的结构式为
的结构式为_______ ,中心原子N的杂化方式为_______ 。
(2)NH4BF4(四氟硼酸铵)可用作铝或铜的焊接助熔剂,能腐蚀玻璃,有重要的化工用途。下列说法正确的是________ 。
(3)向硫酸铜溶液中通入过量氨气,得到深蓝色溶液,生成配合物[Cu(NH3)4]SO4,其中1mol阳离子[Cu(NH3)4]2+中含有σ键数目为________ 。向该深蓝色溶液中加入乙醇,得到深蓝色晶体,该深蓝色晶体为________ (填化学式)。
(4)请从结构角度解释HNO3的酸性比HNO2强的原因________ 。
(1)已知NO
 与CO2互为等电子体,NO
与CO2互为等电子体,NO 的结构式为
的结构式为(2)NH4BF4(四氟硼酸铵)可用作铝或铜的焊接助熔剂,能腐蚀玻璃,有重要的化工用途。下列说法正确的是
| A.核素15N的中子数为7 | B.F元素位于元素周期表p区 |
C.BF 的空间构型为正四面体形 的空间构型为正四面体形 | D.NH4BF4中存在离子键、共价键、氢键和范德华力 |
(4)请从结构角度解释HNO3的酸性比HNO2强的原因
您最近一年使用:0次
解题方法
2 . 硫及其化合物用途很广,图(a)为 的结构,图(b)为固体
的结构,图(b)为固体 中存在的三聚分子。下列说法不正确的是
中存在的三聚分子。下列说法不正确的是
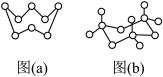
 的结构,图(b)为固体
的结构,图(b)为固体 中存在的三聚分子。下列说法不正确的是
中存在的三聚分子。下列说法不正确的是
A. 的熔、沸点比 的熔、沸点比 的熔、沸点高很多 的熔、沸点高很多 |
B. 分子的空间构型为平面三角形 分子的空间构型为平面三角形 |
C.图(a)和图(b)分子中S原子的杂化轨道类型均为 |
| D.图(a)和图(b)均存在大π键 |
您最近一年使用:0次
名校
解题方法
3 . 三卤化氮( )如
)如 、
、 等有广泛的用途。
等有广泛的用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌。回答下面问题:
可用于面粉的漂白和杀菌。回答下面问题:
(1)锑是制造液晶显示器的一种原材料,基态锑的价层电子排布式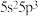 ,可知锑在元素周期表的位置是
,可知锑在元素周期表的位置是___________ 。基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(2)元素F、O、N位于同一周期,其第一电离能由大到小的顺序是___________ ,原子半径由大到小的顺序是___________ 。
(3)液晶显示器材料因含微量杂质元素铬(Cr)而呈浅红色。基态铬原子的价层电子排布式为___________ 。液晶在放电过程中会产生 和
和 离子,其中N原子的杂化类型分别是
离子,其中N原子的杂化类型分别是___________ ,键角:
___________  (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。
(4)已知热稳定性 高于
高于 ,解释其原因是
,解释其原因是___________ 。常温常压下 为无色气体,
为无色气体, 为黄色油状液体,
为黄色油状液体, 和
和 价层电子对互斥模型均为
价层电子对互斥模型均为___________ , 和
和 的分子空间构型均为
的分子空间构型均为___________ 。
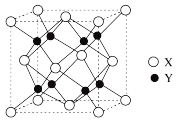
(5) 的晶胞结构如图所示,X代表的离子是
的晶胞结构如图所示,X代表的离子是___________ ;若该立方晶胞参数为apm, 的摩尔质量用
的摩尔质量用 ,阿伏加德罗常数用
,阿伏加德罗常数用 来表示,则
来表示,则 晶体的密度=
晶体的密度=___________  (写出表达式)。
(写出表达式)。
 )如
)如 、
、 等有广泛的用途。
等有广泛的用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌。回答下面问题:
可用于面粉的漂白和杀菌。回答下面问题:(1)锑是制造液晶显示器的一种原材料,基态锑的价层电子排布式
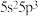 ,可知锑在元素周期表的位置是
,可知锑在元素周期表的位置是(2)元素F、O、N位于同一周期,其第一电离能由大到小的顺序是
(3)液晶显示器材料因含微量杂质元素铬(Cr)而呈浅红色。基态铬原子的价层电子排布式为
 和
和 离子,其中N原子的杂化类型分别是
离子,其中N原子的杂化类型分别是
 (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。(4)已知热稳定性
 高于
高于 ,解释其原因是
,解释其原因是 为无色气体,
为无色气体, 为黄色油状液体,
为黄色油状液体, 和
和 价层电子对互斥模型均为
价层电子对互斥模型均为 和
和 的分子空间构型均为
的分子空间构型均为(5)
 的晶胞结构如图所示,X代表的离子是
的晶胞结构如图所示,X代表的离子是 的摩尔质量用
的摩尔质量用 ,阿伏加德罗常数用
,阿伏加德罗常数用 来表示,则
来表示,则 晶体的密度=
晶体的密度= (写出表达式)。
(写出表达式)。
您最近一年使用:0次
2023-05-14更新
|
93次组卷
|
3卷引用:河北省尚义县第一中学2022-2023学年高二下学期第三次阶段测试化学试题
名校
解题方法
4 . 许多元素及它们的化合物在科学研究和工业生产中具有多种用途。请回答下列有关问题:
(1)某同学画出的基态碳原子的核外电子排布图为 ,该电子排布图违背了
,该电子排布图违背了___________ 。 都是重要的有机反应中间体。
都是重要的有机反应中间体。 的空间构型分别为
的空间构型分别为___________ 、___________ 。
(2)类卤素 对应的酸有两种,理论上硫氰酸
对应的酸有两种,理论上硫氰酸 的沸点低于异硫氰酸
的沸点低于异硫氰酸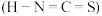 的沸点,其原因是
的沸点,其原因是___________ 。
(3) 中孤电子对与
中孤电子对与 键比值为
键比值为___________ ,碳原子的杂化方式为___________ 。
(4)白铜(铜镍合金)的立方晶胞结构如图1所示,其中原子A的坐标参数为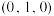
①原子B的坐标参数为___________ 。
②若该晶体密度为 ,则铜镍原子间最短距离为
,则铜镍原子间最短距离为___________ cm。

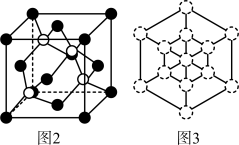
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶胞如图2所示(其中实心球为磷原子),磷化硼晶胞沿着体对角线方向的投影(图3中 表示P原子的投影),用
表示P原子的投影),用 画出B原子的投影位置
画出B原子的投影位置___________ 。
(1)某同学画出的基态碳原子的核外电子排布图为
 ,该电子排布图违背了
,该电子排布图违背了 都是重要的有机反应中间体。
都是重要的有机反应中间体。 的空间构型分别为
的空间构型分别为(2)类卤素
 对应的酸有两种,理论上硫氰酸
对应的酸有两种,理论上硫氰酸 的沸点低于异硫氰酸
的沸点低于异硫氰酸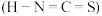 的沸点,其原因是
的沸点,其原因是(3)
 中孤电子对与
中孤电子对与 键比值为
键比值为(4)白铜(铜镍合金)的立方晶胞结构如图1所示,其中原子A的坐标参数为
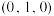
①原子B的坐标参数为
②若该晶体密度为
 ,则铜镍原子间最短距离为
,则铜镍原子间最短距离为
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶胞如图2所示(其中实心球为磷原子),磷化硼晶胞沿着体对角线方向的投影(图3中
 表示P原子的投影),用
表示P原子的投影),用 画出B原子的投影位置
画出B原子的投影位置
您最近一年使用:0次
5 . 金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:
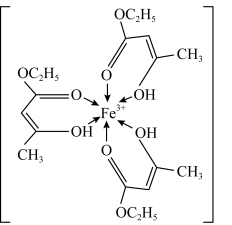
①基态铁离子的核外电子填充在___________ 个原子轨道中;
②此配离子中碳原子的杂化轨道类型为___________ ;
③此配离子中含有的化学键类型为___________ 。
A.离子键 B.金属键 C.共价键 D.配位键 E.σ键 F.π键
(2) 与钴盐形成的配离子
与钴盐形成的配离子 可用于检验
可用于检验 的存在。
的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为___________ 。
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物 和
和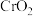 ,其中适合作录音带磁粉原料的是
,其中适合作录音带磁粉原料的是___________ 。
(4)锰的一种配合物的化学式为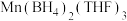 。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与
。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与 互为等电子体的微粒
互为等电子体的微粒___________ (请写出一个分子和一个离子)。
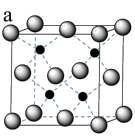
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为___________ ,已知晶胞密度为ρg/cm ,用
,用 表示阿伏加德罗常数的值,则晶胞的边长为
表示阿伏加德罗常数的值,则晶胞的边长为___________ cm(列计算式)。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①基态铁离子的核外电子填充在
②此配离子中碳原子的杂化轨道类型为
③此配离子中含有的化学键类型为
A.离子键 B.金属键 C.共价键 D.配位键 E.σ键 F.π键
(2)
 与钴盐形成的配离子
与钴盐形成的配离子 可用于检验
可用于检验 的存在。
的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物
 和
和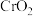 ,其中适合作录音带磁粉原料的是
,其中适合作录音带磁粉原料的是(4)锰的一种配合物的化学式为
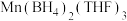 。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与
。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与 互为等电子体的微粒
互为等电子体的微粒(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为
 ,用
,用 表示阿伏加德罗常数的值,则晶胞的边长为
表示阿伏加德罗常数的值,则晶胞的边长为
您最近一年使用:0次



