解题方法
1 . 碳(C)、氮(N)、氧(O)、硫(S)等是常见的非金属元素,钴(Co)是一种重要的金属元素,回答下列问题:
(1)一种由含钴的配合物形成的新型高能材料的结构如图所示。

①阴离子 是该材料的组成部分,则1mol该阴离子中含σ键的数目为
是该材料的组成部分,则1mol该阴离子中含σ键的数目为_______ (NA为阿伏加德罗常数的值),已知该离子是平面结构,则图中标记*的N和O原子之间的σ键是由N原子的_______ 杂化轨道与O原子的_______ 轨道重叠形成。
②写出一种与 互为等电子体的分子:
互为等电子体的分子:_______ (填化学式)。
③实验证明NH3的极性比NCl3大,其原因是_______ 。
(2)一种新型环烯类储氢材料分子式为C16S8,分子中的原子都处于同平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子。

①有关键长数据如下:
从表中数据可以推测C16S8中碳硫键的性质为_______ (填字母)。
A.类似于C-S单键的性质
B.类似于C=S双键的性质
C.兼有C-S单键和C=S双键的性质
②储氢时,C16S8与H2间的作用力是_______ 。
(3) 和NH3是配合物
和NH3是配合物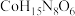 的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为
的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为_______ 。
(4)CoO2是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。

①原子坐标参数:A为(0,0,0);B为(0.31,0.31,0),则C原子的坐标参数为_______ 。
②若阿伏加德罗常数的值为NA,则该晶体密度为_______  (列出计算表达式)。
(列出计算表达式)。
(1)一种由含钴的配合物形成的新型高能材料的结构如图所示。

①阴离子
 是该材料的组成部分,则1mol该阴离子中含σ键的数目为
是该材料的组成部分,则1mol该阴离子中含σ键的数目为②写出一种与
 互为等电子体的分子:
互为等电子体的分子:③实验证明NH3的极性比NCl3大,其原因是
(2)一种新型环烯类储氢材料分子式为C16S8,分子中的原子都处于同平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子。

①有关键长数据如下:
| 化学键 | C-S | C=S | C16S8 |
| 键长/pm | 181 | 155 | 176 |
从表中数据可以推测C16S8中碳硫键的性质为
A.类似于C-S单键的性质
B.类似于C=S双键的性质
C.兼有C-S单键和C=S双键的性质
②储氢时,C16S8与H2间的作用力是
(3)
 和NH3是配合物
和NH3是配合物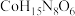 的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为
的配体,若该配合物的中心离子的价电子层有4个未成对电子,则其配位数为6的正二价配离子化学式为(4)CoO2是一种磁性材料,其晶胞结构如图甲所示,俯视图如图乙所示。

①原子坐标参数:A为(0,0,0);B为(0.31,0.31,0),则C原子的坐标参数为
②若阿伏加德罗常数的值为NA,则该晶体密度为
 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
2 . 如表为四种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是___ 。
(2)Z、Q、R相比,其原子半径由大到小的顺序是___ 。
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为___ ,其中R在周期表中的位置是__ ,R的基态原子电子排布式为___ 。
(4)与O3分子互为等电子体的一种分子为___ ,阴离子为__ 。
(5)Y与R相比,非金属性较强的是___ ,能证明这一结论的事实是___ 。(用化学方程式表示)
| 元素 | 元素的相关信息 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
(1)Y元素的最简单氢化物的空间构型是
(2)Z、Q、R相比,其原子半径由大到小的顺序是
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为
(4)与O3分子互为等电子体的一种分子为
(5)Y与R相比,非金属性较强的是
您最近一年使用:0次
名校
解题方法
3 . 通过有机分子a可组装高度有序的聚电解质薄膜b,该薄膜具有精确可调谐的层间距和高效的离子传输。下列说法错误的是

| A.有机分子a中参与sp3杂化和sp2杂化的C原子数目之比为4:1 |
| B.有机分子a中存在离子键和共价键 |
| C.聚电解质薄膜b中相邻的有机分子a之间存在氢键 |
| D.离子在聚电解质薄膜b中依靠正、负电荷间的静电作用传输 |
您最近一年使用:0次
4 . 某有机物脱羧反应机理如图所示。下列说法错误的是
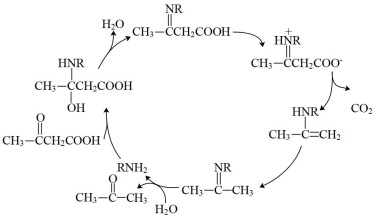
A. 可以被银氨溶液氧化 可以被银氨溶液氧化 |
| B.RNH2是脱羧反应的催化剂 |
| C.该反应过程中涉及加成反应和消去反应 |
| D.反应过程中的氮原子的杂化类型既有sp2杂化,也有sp3杂化 |
您最近一年使用:0次
名校
5 . 请回答下列问题:
(1)非金属氟化物在生产、生活和科研中应用广泛。OF2分子的空间结构为___________ ;OF2的熔、沸点___________ (填“高于”或“低于”)Cl2O,原因是___________ 。
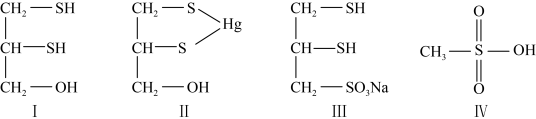
(2)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物II。___________ 。
②化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有___________ 。
A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C—C—C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
(3)硅和卤素单质反应可以得到SiX4.SiX4的熔、沸点如下表:
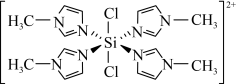
①0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是___________ (填化学式),气态SiX4分子的空间结构是___________ 。___________ ,H、C、N的电负性由大到小的顺序为___________ ,1个M2+中含有___________ 个σ键。
(1)非金属氟化物在生产、生活和科研中应用广泛。OF2分子的空间结构为
(2)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物II。
②化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有
A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C—C—C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
(3)硅和卤素单质反应可以得到SiX4.SiX4的熔、沸点如下表:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
②SiCl4与N甲基咪唑(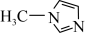 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
您最近一年使用:0次
名校
解题方法
6 . 科学家通过光催化分解水,可将太阳能转换为高热值的 ,一系列光催化剂被开发出来,其中钴配合物由于成本低、性能稳定和应用前景广泛而成为众多科学家的研究对象,一种钴配合物的结构简式如图所示,下列说法错误的是
,一系列光催化剂被开发出来,其中钴配合物由于成本低、性能稳定和应用前景广泛而成为众多科学家的研究对象,一种钴配合物的结构简式如图所示,下列说法错误的是
 ,一系列光催化剂被开发出来,其中钴配合物由于成本低、性能稳定和应用前景广泛而成为众多科学家的研究对象,一种钴配合物的结构简式如图所示,下列说法错误的是
,一系列光催化剂被开发出来,其中钴配合物由于成本低、性能稳定和应用前景广泛而成为众多科学家的研究对象,一种钴配合物的结构简式如图所示,下列说法错误的是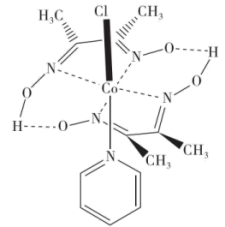
A.该配合物中C、N、O的杂化类型均为 |
| B.中心离子钴离子的配位数为6 |
| C.第一电离能大小:N>O>C>Co |
| D.Co元素为过渡金属元素,其离子对多种配体有很强的结合力 |
您最近一年使用:0次
2024-04-13更新
|
229次组卷
|
2卷引用:河北省石家庄市河北正定中学2023-2024学年高三下学期第一次月考化学试题
解题方法
7 . 下列关于有机物中碳原子的成键特点的说法错误的是
| A.CH4分子中的碳原子轨道的杂化方式为sp3 |
| B.苯分子的分子空间结构为平面形 |
C.乙炔分子中含有 键和 键和 键,其分子的空间结构为直线形 键,其分子的空间结构为直线形 |
D.乙烯分子中形成 键的电子云重叠程度小于形成 键的电子云重叠程度小于形成 键的电子云重叠程度 键的电子云重叠程度 |
您最近一年使用:0次
名校
8 . 多杂原子—氢键桥接电子传递途径赋予了超分子催化体系很高的光催化性能,有机物 和
和 配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是
配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是

 和
和 配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是
配合物形成的超分子催化体系的局部结构如图所示。下列说法错误的是
A.与 同周期且未成对电子数相同的元素还有3种 同周期且未成对电子数相同的元素还有3种 |
B.每个配体与 形成2个配位键 形成2个配位键 |
| C.①和②处氮原子杂化方式相同 |
D.①处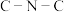 键夹角小于③处 键夹角小于③处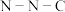 键夹角 键夹角 |
您最近一年使用:0次
2024-02-13更新
|
250次组卷
|
2卷引用:河北省沧州市泊头市部分学校2023-2024学年高三上学期12月月考化学试题
名校
9 . 下列说法错误的是
A.甲基碳正离子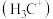 的空间结构为三角锥形 的空间结构为三角锥形 |
| B.单层石墨烯的片层中只存在共价键,不存在范德华力 |
| C.乙二醇分子间可形成氢键 |
D.1个 (乙酰胆碱)分子中有8个 (乙酰胆碱)分子中有8个 杂化的原子 杂化的原子 |
您最近一年使用:0次
2024-01-15更新
|
175次组卷
|
2卷引用:河北省沧州市部分学校2023-2024学年高三上学期12月联考化学试题
名校
10 . 质子离子液体具有高质子电导率以及优异的电化学和热稳定性,某质子离子液体的结构如图所示,下列说法错误的是
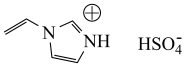

| A.上述离子液体固态时,含有极性共价键、配位键和离子键 |
B.阴离子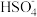 中S原子为sp3杂化 中S原子为sp3杂化 |
| C.第一电离能:S<O<N |
| D.C、N、O形成的简单氢化物的沸点均为所在主族最高的 |
您最近一年使用:0次



