2019·甘肃兰州·一模
1 . 根据下列信息,结合有关物质结构的知识回答:
(1)已知M是短周期金属元素,M的部分电离能如下表所示:

则M基态原子的电子排布式为___________ ,该金属晶体的堆积方式为六方最密堆积,配位数为___________ 。
(2)已知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似,且三种离子晶体的晶格能数据如下表所示:

则KC1、CaO、TiN三种离子晶体熔点由高到低的顺序为___________ ,原因是___________ 。
(3)根据下图回答:
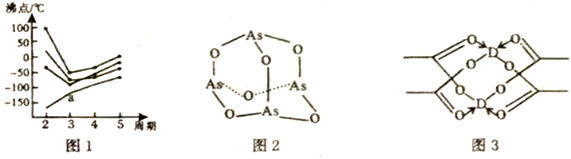
①如图1所示,每条折线表示周期表ⅣA~ⅦA中的某一主族元素的简单氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的物质是___________ (填化学式)。判断依据是___________ 。
②As4O6的分子结构如图2所示,则该化合物中As的杂化方式是___________ ,与AsO43-互为等电子体的微粒是___________ (写出一种即可)。
③D的醋酸盐晶体局部结构如图3所示,该晶体中含有的化学键类型有___________ (填字母标号)
A.极性键 B.非极性键 C.配位键 D.金属键
(4)Fe的一种晶体结构如图甲、乙所示,若按甲虚线方向切割乙,得到的截面图A~D中正确的是___________ (填字母标号)。

假设铁原子的半径是rcm,铁的相对原子质量为M,则该晶体的密度为___________ (设阿伏伽德罗常数的值为NA)
(1)已知M是短周期金属元素,M的部分电离能如下表所示:

则M基态原子的电子排布式为
(2)已知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似,且三种离子晶体的晶格能数据如下表所示:

则KC1、CaO、TiN三种离子晶体熔点由高到低的顺序为
(3)根据下图回答:

①如图1所示,每条折线表示周期表ⅣA~ⅦA中的某一主族元素的简单氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的物质是
②As4O6的分子结构如图2所示,则该化合物中As的杂化方式是
③D的醋酸盐晶体局部结构如图3所示,该晶体中含有的化学键类型有
A.极性键 B.非极性键 C.配位键 D.金属键
(4)Fe的一种晶体结构如图甲、乙所示,若按甲虚线方向切割乙,得到的截面图A~D中正确的是

假设铁原子的半径是rcm,铁的相对原子质量为M,则该晶体的密度为
您最近一年使用:0次
名校
2 . 硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式___________ 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝的晶体类型是___________ ;
②写出Al2Cl6分子的结构式___________ ;
③单分子A1Cl3的立体构型是___________ ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是___________ 。
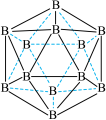
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),若其中有两个原子为10B,其余为11B,则该结构单元有___________ 种不同的结构类型。
(4)金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm−3,计算确定其晶胞的类型(简单、体心或面心立方)___________ ;晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)=___________ pm。
(1)写出基态镓原子的电子排布式
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝的晶体类型是
②写出Al2Cl6分子的结构式
③单分子A1Cl3的立体构型是
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),若其中有两个原子为10B,其余为11B,则该结构单元有

(4)金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm−3,计算确定其晶胞的类型(简单、体心或面心立方)
您最近一年使用:0次
2016-12-09更新
|
450次组卷
|
6卷引用:【全国百强校】甘肃省白银市会宁县第一中学2019届高三上学期第三次月考理科综合化学试题



