名校
1 . [化学——选修3:物质结构与性质]
周期表前四周期的元素a、b、c、d、e,原子序数依次增大,a是组成物质种类最多的元素,c是地壳中含量最多的元素,d与a同族,e2+离子3d轨道中有9个电子。回答下列问题:
(1)e原子的价层电子排布图为____________
(2)晶体d、晶体da晶体ac2的熔点由高到低的顺序为____________ (用化学用语表示,下同),a、b、c三种元素的第一电离能由大到小的顺序为________________________ 。
(3)元素b、c形成两种常见阴离子bc2-和bc3-,其中bc2-离子的中心原子杂化轨道类型为____________ ,bc3-离子的空间构型为____________ 。
(4)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。请写出得到深蓝色透明溶液的离子方程式________________________ ,析出深蓝色晶体时加入乙醇的作用是________________________ 。
(5)e单质的晶胞结构如图所示,e原子半径为rpm,e晶体密度的计算式为____________ g·cm3。(用含NA、r的表达式表示)

周期表前四周期的元素a、b、c、d、e,原子序数依次增大,a是组成物质种类最多的元素,c是地壳中含量最多的元素,d与a同族,e2+离子3d轨道中有9个电子。回答下列问题:
(1)e原子的价层电子排布图为
(2)晶体d、晶体da晶体ac2的熔点由高到低的顺序为
(3)元素b、c形成两种常见阴离子bc2-和bc3-,其中bc2-离子的中心原子杂化轨道类型为
(4)向e2+硫酸盐的水溶液中加入过量的氨水,可得到深蓝色透明溶液,加入乙醇可析出深蓝色晶体。请写出得到深蓝色透明溶液的离子方程式
(5)e单质的晶胞结构如图所示,e原子半径为rpm,e晶体密度的计算式为

您最近一年使用:0次
2020-09-09更新
|
426次组卷
|
3卷引用:新疆昌吉市第九中学2021届高三上学期开学考试化学试题
2 . 铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液,电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为___________ 。
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______ 。
(3)SO42-的立体构型是________ ,其中S原子的杂化轨道类型是_______ 。
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是
(3)SO42-的立体构型是
您最近一年使用:0次
3 . (1)BF3与一定量的水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
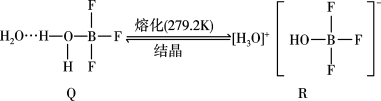
①晶体Q中各种微粒间的作用力不涉及____________ (填序号)。
a.离子键 b.共价键 c.配位键 d.金属键e.氢键 f.范德华力
②R中阳离子的空间构型为________ ,阴离子的中心原子轨道采用________ 杂化。
(2)已知苯酚( )具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成的离子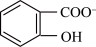 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________ Ka(苯酚)(填“>”或“<”),其原因是________________ 。

①晶体Q中各种微粒间的作用力不涉及
a.离子键 b.共价键 c.配位键 d.金属键e.氢键 f.范德华力
②R中阳离子的空间构型为
(2)已知苯酚(
 )具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
您最近一年使用:0次
4 . 卤族元素包括F、Cl、Br等元素。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是______ 。

(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为______ ,该功能陶瓷的化学式为______ 。

(3)BCl3和NCl3中心原子的杂化方式分别为__________ 和________ 。第一电离能介于B、N之间的第二周期元素有______ 种。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是

(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为

(3)BCl3和NCl3中心原子的杂化方式分别为
您最近一年使用:0次
2015-07-31更新
|
210次组卷
|
2卷引用:新疆巴州种畜场学校2019届高三下学期第二次模拟考试理科综合化学试题
真题
5 . 金属镍在电池、合金、催化剂等方面应用广泛.
(1)下列关于金属及金属键的说法正确的是_____ .
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是____ .
(3)过滤金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=___ .CO与N2结构相似,CO分子内σ键与π键个数之比为______ .
(4)甲醛(H2C═O)在Ni催化作用下加氢可得甲醇(CH3OH).甲醇分子内C原子的杂化方式为_____ ,甲醇分子内的O﹣C﹣H键角____ (填“大于”“等于”或“小于”)甲醛分子内的O﹣C﹣H键角.
(1)下列关于金属及金属键的说法正确的是
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是
(3)过滤金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
(4)甲醛(H2C═O)在Ni催化作用下加氢可得甲醇(CH3OH).甲醇分子内C原子的杂化方式为
您最近一年使用:0次
2014-06-05更新
|
1800次组卷
|
3卷引用:新疆第一汽车厂学校2019届高三第三次模拟考试理科综合化学试题



