名校
解题方法
1 . 近日,比亚迪宣布推出基于磷酸铁锂技术的“刀片电池”,刀片电池能量密度大,安全性高。电池的正极活性材料是 。
。
(1)铁元素位于周期表___________ ;基态 的电子排布式为
的电子排布式为___________ 。
(2)正极材料 的阴离子
的阴离子 的空间构型为
的空间构型为___________ ,磷原子采取的杂化方式为___________ 。
(3)Fe原子或离子外围有较多能量相近的空轨道,能与 、
、 、
、 等形成配合物。
等形成配合物。 的结构简式如下图所示,其结构中
的结构简式如下图所示,其结构中 键和
键和 键的个数比为
键的个数比为___________ , 中含有的化学键类型是
中含有的化学键类型是___________ 。(填字母)。

a.极性共价键 b.离子键 c.配位键 d.金属键
(4)硼酸 是一种片层状结构的白色晶体,层内的
是一种片层状结构的白色晶体,层内的 分子间通过氢键相连(如图)。
分子间通过氢键相连(如图)。

①硼酸分子中B最外层有___________ 个电子,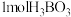 的晶体中有
的晶体中有___________ mol氢键。
②硼酸溶于水生成弱电解质一水合硼酸 ,它电离生成少量
,它电离生成少量 和
和 ,则硼酸为
,则硼酸为___________ 元酸, 含有的化学键类型为
含有的化学键类型为___________ 。
(5) 的
的 、
、 、
、 分别为
分别为 、
、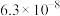 、
、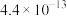 ,硝酸完全电离,而亚硝酸
,硝酸完全电离,而亚硝酸 ,请根据结构与性质的关系解释:
,请根据结构与性质的关系解释:
① 的
的 远大于
远大于 的原因
的原因___________ ;
②硝酸比亚硝酸酸性强的原因___________ 。
 。
。(1)铁元素位于周期表
 的电子排布式为
的电子排布式为(2)正极材料
 的阴离子
的阴离子 的空间构型为
的空间构型为(3)Fe原子或离子外围有较多能量相近的空轨道,能与
 、
、 、
、 等形成配合物。
等形成配合物。 的结构简式如下图所示,其结构中
的结构简式如下图所示,其结构中 键和
键和 键的个数比为
键的个数比为 中含有的化学键类型是
中含有的化学键类型是
a.极性共价键 b.离子键 c.配位键 d.金属键
(4)硼酸
 是一种片层状结构的白色晶体,层内的
是一种片层状结构的白色晶体,层内的 分子间通过氢键相连(如图)。
分子间通过氢键相连(如图)。
①硼酸分子中B最外层有
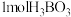 的晶体中有
的晶体中有②硼酸溶于水生成弱电解质一水合硼酸
 ,它电离生成少量
,它电离生成少量 和
和 ,则硼酸为
,则硼酸为 含有的化学键类型为
含有的化学键类型为(5)
 的
的 、
、 、
、 分别为
分别为 、
、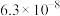 、
、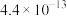 ,硝酸完全电离,而亚硝酸
,硝酸完全电离,而亚硝酸 ,请根据结构与性质的关系解释:
,请根据结构与性质的关系解释:①
 的
的 远大于
远大于 的原因
的原因②硝酸比亚硝酸酸性强的原因
您最近一年使用:0次
2023-04-20更新
|
148次组卷
|
2卷引用:河南省焦作市博爱县第一中学2023-2024学年高三上学期8月月考化学试题
名校
解题方法
2 . 2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(1)基态As原子的价电子排布图为________ ,基态Ga原子核外有____ 个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为____ 和+3。
(3)1918年美国人通过反应:HC≡CH+AsCl3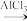 CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为
CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为________ ;AsCl3分子的空间构型为___________ 。
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中碳原子的杂化方式为_______
(1)基态As原子的价电子排布图为
(2)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为
(3)1918年美国人通过反应:HC≡CH+AsCl3
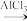 CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为
CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中碳原子的杂化方式为
您最近一年使用:0次
2020-11-16更新
|
393次组卷
|
4卷引用:河南省焦作市博爱英才学校2021届高三开学考试化学试题
河南省焦作市博爱英才学校2021届高三开学考试化学试题(已下线)易错27 分子的立体结构-备战2021年高考化学一轮复习易错题辽宁省南台、岫二、牛庄、海城三中、腾鳌、析木等高级中学2020-2021学年高二上学期期末考试化学试题辽宁省大连市普兰店区第二中学2020-2021学年高二下学期期中考试化学试题
名校
解题方法
3 . 我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”、“中国紫”,近年来,人们对这些颜料的成分进行了研究,发现其成分主要为BaCuSi4O10、BaCuSi2O6。
(1)“中国蓝”、“中国紫”中均有Cun+离子,n=___________ ,基态时该阳离子的价电子排布式为___________ 。
(2)“中国蓝”的发色中心是以Cun+为中心离子的配位化合物,其中提供孤对电子的是____ 元素。
(3)已知Cu、Zn的第二电离能分别为1957.9 kJ·mol-1、1733.3 kJ·mol-1,前者高于后者的原因是________________________________________ 。
(4)铜常用作有机反应的催化剂。例如,2CH3CH2OH+O2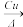 2CH3CHO+2H2O。
2CH3CHO+2H2O。
①乙醇的沸点高于乙醛,其主要原因是_________________________________ ;乙醛分子中π键与σ键的个数比为___________ 。
②乙醛分子中碳原子的杂化轨道类型是___________ 。
(5)铜的晶胞如图所示。铜银合金是优质的金属材料,其晶胞与铜晶胞类似,银位于顶点,铜位于面心。
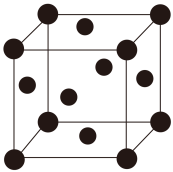
①该铜银合金的化学式是___________________ 。
②已知:该铜银晶胞参数为a cm,晶体密度为ρ g·cm-3。则阿伏加 德罗常数(NA)为_______ mol-1(用代数式表示,下同)。
③若Ag、Cu原子半径分别为b cm、c cm,则该晶胞中原子空间利用率φ为___________ 。(提示:晶胞中原子空间利用率=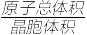 ×100%)
×100%)
(1)“中国蓝”、“中国紫”中均有Cun+离子,n=
(2)“中国蓝”的发色中心是以Cun+为中心离子的配位化合物,其中提供孤对电子的是
(3)已知Cu、Zn的第二电离能分别为1957.9 kJ·mol-1、1733.3 kJ·mol-1,前者高于后者的原因是
(4)铜常用作有机反应的催化剂。例如,2CH3CH2OH+O2
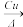 2CH3CHO+2H2O。
2CH3CHO+2H2O。①乙醇的沸点高于乙醛,其主要原因是
②乙醛分子中碳原子的杂化轨道类型是
(5)铜的晶胞如图所示。铜银合金是优质的金属材料,其晶胞与铜晶胞类似,银位于顶点,铜位于面心。

①该铜银合金的化学式是
②已知:该铜银晶胞参数为a cm,晶体密度为ρ g·cm-3。则阿伏加 德罗常数(NA)为
③若Ag、Cu原子半径分别为b cm、c cm,则该晶胞中原子空间利用率φ为
 ×100%)
×100%)
您最近一年使用:0次
2020-05-28更新
|
1376次组卷
|
6卷引用:河南省原阳县第一高级中学2021-2022学年高三上学期开学适应性考试理综化学试题
4 . 以黄铜矿(主要成分为铁、铜、硫三种元素组成的化合物)为基本原料,通过一系列的冶炼可得到铜、铁、SO2、SO3、H2SO4等物质,回答下列问题:
(1)基态铁原子价层电子排布式为____________ ,基态硫原子的核外电子共有_______ 种不同的能量。硫元素所在周期的非金属元素第一电离能由大到小的顺序为__________ 。
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是________ ,SO2的分子构型是____________ ,属于非极性分子的氧化物是___________ 。
(3)在溶液中Cu2+易与水形成[Cu(H2O)6]2+而显蓝色,向相应的溶液中加入足量的氨水可得到[Cu(NH3)4(H2O)2]2+,则[Cu(NH3)4(H2O)2]2+中Cu2+的配位数是________________ ,氧铜配位键与氮铜配位键相比,较稳定的是___________________ 。
(4)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,试解释导致这种差异最可能的原因是___________ 。
(5)由铁、铜、硫形成的某种化合物的晶胞是一个长方体,结构如图所示,则该化合物的化学式为____________ 。若晶体密度为dg·cm﹣3,则晶胞的高h=_______ pm(写出简化后的计算式即可)。

(1)基态铁原子价层电子排布式为
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是
(3)在溶液中Cu2+易与水形成[Cu(H2O)6]2+而显蓝色,向相应的溶液中加入足量的氨水可得到[Cu(NH3)4(H2O)2]2+,则[Cu(NH3)4(H2O)2]2+中Cu2+的配位数是
(4)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,试解释导致这种差异最可能的原因是
(5)由铁、铜、硫形成的某种化合物的晶胞是一个长方体,结构如图所示,则该化合物的化学式为

您最近一年使用:0次
2020-03-17更新
|
641次组卷
|
3卷引用:河南省确山县第二高级中学2021-2022学年高三上学期期中考试化学试题
名校
5 . 铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业。其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
(1)K3[Fe(CN)6]中所涉及的元素的基态原子核外未成对电子数最多的是_________ (填元素名称),各元素的第一电离能由大到小的顺序为___________________ 。
(2)(CN)2分子中存在碳碳键,则分子中σ键与π键数目之比为_______ 。
(3)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253 K,沸点为为376 K,其固体属于_________ 晶体。
(4)下图是金属单质常见的两种堆积方式的晶胞模型。

①铁采纳的是a堆积方式.铁原子的配位数为_____ ,该晶体中原子总体积占晶体体积的比值为_________ (用含π的最简代数式表示)。
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为__________ g·cm-3(用含有r、NA的最简代数式表示)。
(1)K3[Fe(CN)6]中所涉及的元素的基态原子核外未成对电子数最多的是
(2)(CN)2分子中存在碳碳键,则分子中σ键与π键数目之比为
(3)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253 K,沸点为为376 K,其固体属于
(4)下图是金属单质常见的两种堆积方式的晶胞模型。

①铁采纳的是a堆积方式.铁原子的配位数为
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为
您最近一年使用:0次
名校
6 . 氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过______ 方法区分晶体准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为______ 。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______ ,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是______ (各举一例)。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是______ ;氟化铵中存在______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图(a)计算相关键能。则F-F键的键能为______ kJ•mol-1,S-F键的键能为______ kJ•mol-1。
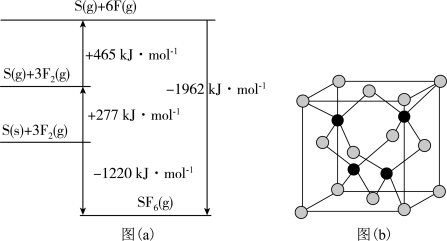
(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是______
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=______ nm(列出计算式)。
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态F原子的价层电子排布图(轨道表达式)为
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是
A.离子键 B.σ键 C.π键 D.氢键
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图(a)计算相关键能。则F-F键的键能为

(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=
您最近一年使用:0次
2019-10-28更新
|
351次组卷
|
2卷引用:河南省天一大联考2019学年高三年级上学期期末考试化学试题
名校
7 . 硼、磷元素在化学中有很重要的地位,硼、磷及其化合物广泛应用于开发新型储氢材料、超导材料、富燃料材料、复合材料等高新材料领域。回答下列问题。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有___ 个。
②LiBH4由Li+和BH4-构成,BH4-呈正四面体构型。LiBH4中不存在的作用力有___ (填标号)
A.离子键 B.共价键 C.金属键 D.配位键
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为____ ,写出一种与氨硼烷互为等电子体的分子___ (填化学式)。
(3)硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子间通过氢键相连[如图]。
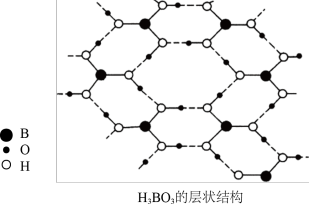
读图分析1mol H3BO3的晶体中有___ mol氢键。
(4)四(三苯基膦)钯分子结构如图:
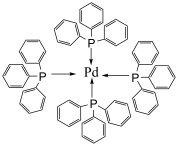
P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为___ ;判断该物质在水中___ (填写“易溶”或者“难溶”),并加以解释____ 。
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图所示:
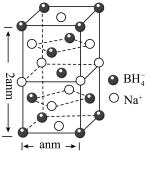
①该晶体中Na+的配位数为___ 。
②已知硼氢化钠晶体的密度为ρg/cm3,NA代表阿伏加 德罗常数的值,则a=___ (用含ρ、NA的最简式子表示)
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有
②LiBH4由Li+和BH4-构成,BH4-呈正四面体构型。LiBH4中不存在的作用力有
A.离子键 B.共价键 C.金属键 D.配位键
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为
(3)硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子间通过氢键相连[如图]。

读图分析1mol H3BO3的晶体中有
(4)四(三苯基膦)钯分子结构如图:

P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图所示:

①该晶体中Na+的配位数为
②已知硼氢化钠晶体的密度为ρg/cm3,NA代表阿伏加 德罗常数的值,则a=
您最近一年使用:0次
名校
8 . 离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
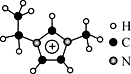
(1)碳原子价层电子的轨道表达式为__________ ,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________ 形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______ 。NH3比PH3的沸点高,原因是_________ 。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是____________ 。
(4)EMIM+离子中,碳原子的杂化轨道类型为______ 。分子中的大π键可用符号 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为________ 。
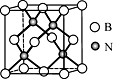
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______ 晶体,其中硼原子的配位数为_______ 。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏伽德罗常数的值为NA,则该晶胞中原子的空间利用率为________ (列出化简后的计算式)。

(1)碳原子价层电子的轨道表达式为
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是
(3)氮元素的第一电离能比同周期相邻元素都大的原因是
(4)EMIM+离子中,碳原子的杂化轨道类型为
 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+离子中的大π键应表示为
),则EMIM+离子中的大π键应表示为
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于
您最近一年使用:0次
2019-01-14更新
|
1543次组卷
|
5卷引用:【全国百强校】河南省许昌高级中学2019届高三下学期复习诊断(二)化学试题
名校
解题方法
9 . 中国炼丹家约在唐代或五代时期掌握了以炉甘石点化鍮石(即鍮石金)的技艺:将炉甘石(ZnCO3)、赤铜矿(主要成分Cu2O)和木炭粉混合加热至800℃左右可制得与黄金相似的鍮石金。回答下列问题:
(1)锌元素基态原子的价电子排布式为________________ ,铜元素基态原子中的未成对电子数为_________________ 。
(2)硫酸锌溶于过量氨水形成[ Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中,阴离子的立体构型是__________________ ,[Zn(NH3)4]2+中含有的化学键有__________________ 。
②NH3分子中,中心原子的轨道杂化类型为________________ ,NH3在H2O中的溶解度____________ (填“大”或“小”),原因是_____________________ 。
(3)铜的第一电离能为I1Cu=745.5kJ·mol-1,第二电离能为I2Cu=1957.9kJ·mol-1,锌的第一电离能为I1Zn=906.4kJ·mol-1,第二电离能为I2Zn=1733.3kJ·mol-1,I2Cu>I2Zn的原因是___________________ 。
(4)Cu2O晶体的晶胞结构如图所示。O2-的配位数为_______________ ;若Cu2O的密度为dg·cm-3,则晶胞参数a=____________ nm。
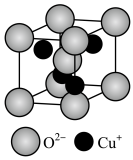
(1)锌元素基态原子的价电子排布式为
(2)硫酸锌溶于过量氨水形成[ Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中,阴离子的立体构型是
②NH3分子中,中心原子的轨道杂化类型为
(3)铜的第一电离能为I1Cu=745.5kJ·mol-1,第二电离能为I2Cu=1957.9kJ·mol-1,锌的第一电离能为I1Zn=906.4kJ·mol-1,第二电离能为I2Zn=1733.3kJ·mol-1,I2Cu>I2Zn的原因是
(4)Cu2O晶体的晶胞结构如图所示。O2-的配位数为

您最近一年使用:0次
2018-05-26更新
|
311次组卷
|
2卷引用:【市级联考】河南省南阳市2019届高三上学期期末考试理科综合化学试题
名校
10 . 锰及其化合物用途非常广泛。回答下列问题:
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是___________ 。
(2)基态Mn原子的价电子排布式为_________ ,未成对电子数为_____ 个。
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是____________ 。
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为________ 。
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是_____ ,该分子中碳原子的杂化方式为_______ ;C、H、N的电负性从大到小的顺序为________ 。
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是_________ 。
(6)某种含锰特殊材料的晶胞结构如下图所示:
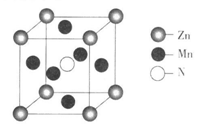
若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为____ ( 列出代数式即可)。
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是
(2)基态Mn原子的价电子排布式为
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是
(6)某种含锰特殊材料的晶胞结构如下图所示:

若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为
您最近一年使用:0次
2018-05-17更新
|
386次组卷
|
2卷引用:【全国市级联考】河南省安阳市2018届高三第三次模拟考试理综化学试题



