名校
1 . 甲乙酮肟(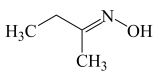 )中同周期三种元素电负性由大到小的顺序为
)中同周期三种元素电负性由大到小的顺序为
您最近一年使用:0次
名校
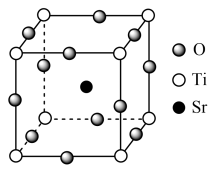
2 . 为降低成本,某些复合型物质也常用作催化剂。某复合型物质的晶胞结构如图所示。___________ 。若晶胞的参数为 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ 。
2.每个Ti原子周围距离最近的O原子的个数为___________。
3.Ti的四卤化物熔点如下表所示。
 熔点高于其他三种卤化物,而自
熔点高于其他三种卤化物,而自 至
至 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
4. 与光气
与光气 反应可用于制取
反应可用于制取 。
。 的空间构型为___________。
的空间构型为___________。
5. 的中心原子的杂化方式为
的中心原子的杂化方式为___________ 。
A.sp B. C.
C.
 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为2.每个Ti原子周围距离最近的O原子的个数为___________。
| A.2 | B.4 | C.6 | D.8 |
| 化合物 |  |  |  |  |
| 熔点/℃ | 377 | 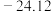 | 38.3 | 155 |
 熔点高于其他三种卤化物,而自
熔点高于其他三种卤化物,而自 至
至 熔点依次升高,原因是
熔点依次升高,原因是4.
 与光气
与光气 反应可用于制取
反应可用于制取 。
。 的空间构型为___________。
的空间构型为___________。| A.直线形 | B.角形 | C.三角锥形 | D.平面三角形 |
 的中心原子的杂化方式为
的中心原子的杂化方式为A.sp B.
 C.
C.
您最近一年使用:0次
名校
3 . 羰基铁[ ]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为
]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为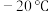 ,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。 晶体类型为___________。
晶体类型为___________。
2.下列说法正确的是___________。
 ]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为
]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为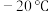 ,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
 晶体类型为___________。
晶体类型为___________。| A.分子晶体 | B.离子晶体 | C.金属晶体 | D.共价晶体 |
A.中心Fe原子可能采取 杂化 杂化 |
| B.配体与Fe原子所形成的配位键的键能相同 |
| C.Fe在周期表中位于VIII族,属于d区元素 |
D.制备 应在隔绝空气的条件下进行 应在隔绝空气的条件下进行 |
您最近一年使用:0次
4 . 缺电子化合物是指电子数不符合路易斯结构(路易斯结构是通过共用电子使原子价层电子数达到8,氢原子达到2所形成的稳定分子结构)要求的一类化合物,某科学小组依据 、
、 、
、 分子对此进行研究。
分子对此进行研究。
(1)写出B原子的价层电子轨道表示式_______ 。
(2) 中心原子的轨道杂化类型是
中心原子的轨道杂化类型是_______ ,其_______ (能/不能)提供孤对电子与Fe2+形成配位键。
(3)上述三种化合物中,是缺电子化合物的是_______ 。
(4)NH3分子极易溶于水,是说明理由_______ 。
 、
、 、
、 分子对此进行研究。
分子对此进行研究。(1)写出B原子的价层电子轨道表示式
(2)
 中心原子的轨道杂化类型是
中心原子的轨道杂化类型是(3)上述三种化合物中,是缺电子化合物的是
(4)NH3分子极易溶于水,是说明理由
您最近一年使用:0次
名校
5 . NH3分子的空间结构为_____ ,其中N原子的杂化轨道类型为_____ 。
您最近一年使用:0次
6 . 利用CH4超干重整CO2技术,可以得到富含CO和H2的化工原料气,对碳达峰和碳中和有重要意义,反应如下:CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)  =+247.4kJ·mol−1
=+247.4kJ·mol−1
(1)反应过程中断裂的化学键属于______。
(2)该反应的熵变∆S___________ 0(填“>”“=”或“<”),需要在___________ 条件下进行(填“低温”或“高温”)。
(3)CO2的电子式为___________ ;CO2分子中碳原子的杂化方式为___________ 杂化,1molCO2中含有___________ molπ键。
(4)已知部分化学键的键能如下:
由此计算断裂1molCO分子中的共价键需要吸收___________ kJ能量。
 2CO(g)+2H2(g)
2CO(g)+2H2(g)  =+247.4kJ·mol−1
=+247.4kJ·mol−1(1)反应过程中断裂的化学键属于______。
| A.离子键 | B.极性共价键 |
| C.非极性共价键 | D.氢键 |
(2)该反应的熵变∆S
(3)CO2的电子式为
(4)已知部分化学键的键能如下:
| 共价键 | C-H | H-H | C=O |
| 键能(kJ/mol) | 413 | 436 | 745 |
您最近一年使用:0次
7 . 在工业上次磷酸 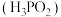 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: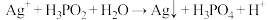 (未配平),已知
(未配平),已知 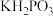 是次磷酸的正盐,请回答下列问题:
是次磷酸的正盐,请回答下列问题:
(1) 中,
中, 元素的化合价为
元素的化合价为_______ ;该反应中, 被
被_______ (填“氧化”或“还原”)。
(2)若该反应有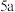 个电子转移,则镀件上银的质量为
个电子转移,则镀件上银的质量为_______  (已知每个银原子质量为
(已知每个银原子质量为 克)。
克)。
(3) 与足量
与足量  溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)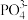 中
中 的价层电子对数为
的价层电子对数为_______ , 采取
采取_______ 杂化方式, 的空间结构为
的空间结构为_______ 。
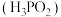 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: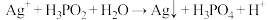 (未配平),已知
(未配平),已知 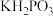 是次磷酸的正盐,请回答下列问题:
是次磷酸的正盐,请回答下列问题:(1)
 中,
中, 元素的化合价为
元素的化合价为 被
被(2)若该反应有
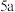 个电子转移,则镀件上银的质量为
个电子转移,则镀件上银的质量为 (已知每个银原子质量为
(已知每个银原子质量为 克)。
克)。(3)
 与足量
与足量  溶液反应的离子方程式:
溶液反应的离子方程式:(4)
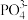 中
中 的价层电子对数为
的价层电子对数为 采取
采取 的空间结构为
的空间结构为
您最近一年使用:0次
8 . 甘氨酸(分子式C2H5NO2)分子中,共有___________ 个σ键。甘氨酸分子中C原子的杂化方式为___________ 。
A. sp B. sp2 C. sp3
甘氨酸钠中第一电离能最小的元素为___________ 。
A. C B. O C. Na D. N
A. sp B. sp2 C. sp3
甘氨酸钠中第一电离能最小的元素为
A. C B. O C. Na D. N
您最近一年使用:0次
9 . 2021年9月Science杂志发表了我国科学家利用CO2合成人工淀粉(ASAP)的论文。据介绍,该方法合成速率是玉米的8.5倍,能量转化效率是玉米的3.5倍。
已知人工合成淀粉的代谢途径(ASAP)可以简化表示为:
(2)写出符合下列条件的DHA的一种同分异构体_____ 。
①属于链状化合物②含有两种官能团③含有手性碳原子
已知人工合成淀粉的代谢途径(ASAP)可以简化表示为:
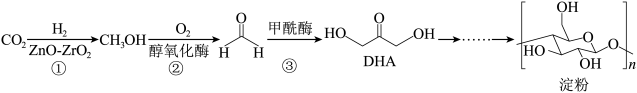
| A.碳原子采用sp3、sp2杂化 |
| B.每个链节含一个平面六边形 |
| C.每个链节中含有的官能团为羟基和醚键 |
| D.淀粉可以发生酯化反应 |
(2)写出符合下列条件的DHA的一种同分异构体
①属于链状化合物②含有两种官能团③含有手性碳原子
您最近一年使用:0次
名校
解题方法
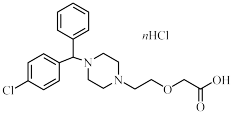
10 . 盐酸左西替利嗪是一种用于治疗荨麻疹的药物。其部分说明书如下:
(1)在左西替利嗪中添加盐酸的目的是___________ ;药品成分中n的值为___________ 。
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是___________ 。请在下图中用:“·”标出具有手性的碳原子。___________
| 盐酸左西替利嗪说明书 【成分】本品为西替利嗪的R型对映体,在过量盐酸中结晶制得。 【性状】本品外观是白色或类白色的片剂,易溶于水。
|
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是

| A.西替利嗪中,有9个碳原子与氮原子的杂化方式相同 |
| B.将西替利嗪溶于水,形成内盐 |
| C.两个苯环上的12个碳原子共平面 |
| D.分子内含有羧基和酯基 |
您最近一年使用:0次