解题方法
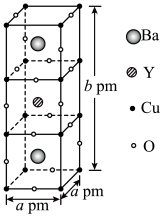
1 .  是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。
是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。_______ 。
(2)N、O、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为_______ , 的空间结构为
的空间结构为_______ 。
(3)固态硒代蛋氨酸晶体类型为_______ ,硒代蛋氨酸分子中 的杂化方式为
的杂化方式为_______ 。
(4)比较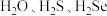 的沸点大小:
的沸点大小:_______ ,原因是_______ 。
(5)某种具有氧原子缺陷的超导材料的长方体晶胞结构如图所示。晶胞参数分别为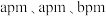 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。已知该晶体中
。已知该晶体中 为
为 价,Y为
价,Y为 价,O为
价,O为 价,则
价,则
_______ ,该晶体的密度为_______  。
。
 是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。
是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。
(2)N、O、
 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为 的空间结构为
的空间结构为(3)固态硒代蛋氨酸晶体类型为
 的杂化方式为
的杂化方式为(4)比较
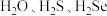 的沸点大小:
的沸点大小:(5)某种具有氧原子缺陷的超导材料的长方体晶胞结构如图所示。晶胞参数分别为
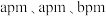 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。已知该晶体中
。已知该晶体中 为
为 价,Y为
价,Y为 价,O为
价,O为 价,则
价,则
 。
。
您最近一年使用:0次
2 . 根据抑制癌细胞增殖药物的恩杂鲁胺 的两条合成路线,回答下列问题。
的两条合成路线,回答下列问题。
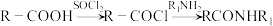 ;
;②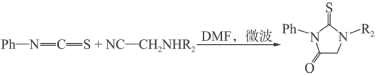 。
。
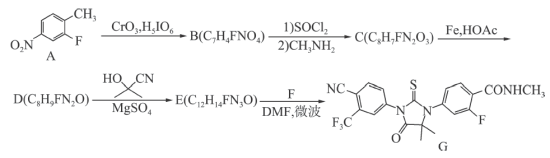
(2)
 反应的化学方程式为
反应的化学方程式为路线二:
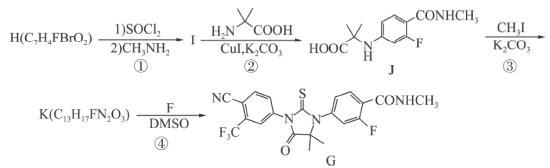
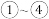 中仅发生取代反应的是
中仅发生取代反应的是
您最近一年使用:0次
名校
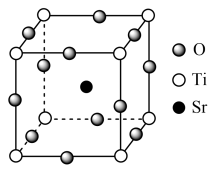
3 . 为降低成本,某些复合型物质也常用作催化剂。某复合型物质的晶胞结构如图所示。___________ 。若晶胞的参数为 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ 。
2.每个Ti原子周围距离最近的O原子的个数为___________。
3.Ti的四卤化物熔点如下表所示。
 熔点高于其他三种卤化物,而自
熔点高于其他三种卤化物,而自 至
至 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
4. 与光气
与光气 反应可用于制取
反应可用于制取 。
。 的空间构型为___________。
的空间构型为___________。
5. 的中心原子的杂化方式为
的中心原子的杂化方式为___________ 。
A.sp B. C.
C.
 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为2.每个Ti原子周围距离最近的O原子的个数为___________。
| A.2 | B.4 | C.6 | D.8 |
| 化合物 |  |  |  |  |
| 熔点/℃ | 377 | 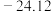 | 38.3 | 155 |
 熔点高于其他三种卤化物,而自
熔点高于其他三种卤化物,而自 至
至 熔点依次升高,原因是
熔点依次升高,原因是4.
 与光气
与光气 反应可用于制取
反应可用于制取 。
。 的空间构型为___________。
的空间构型为___________。| A.直线形 | B.角形 | C.三角锥形 | D.平面三角形 |
 的中心原子的杂化方式为
的中心原子的杂化方式为A.sp B.
 C.
C.
您最近一年使用:0次
名校
4 . 羰基铁[ ]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为
]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为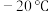 ,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。 晶体类型为___________。
晶体类型为___________。
2.下列说法正确的是___________。
 ]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为
]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为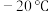 ,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
 晶体类型为___________。
晶体类型为___________。| A.分子晶体 | B.离子晶体 | C.金属晶体 | D.共价晶体 |
A.中心Fe原子可能采取 杂化 杂化 |
| B.配体与Fe原子所形成的配位键的键能相同 |
| C.Fe在周期表中位于VIII族,属于d区元素 |
D.制备 应在隔绝空气的条件下进行 应在隔绝空气的条件下进行 |
您最近一年使用:0次
名校
5 . NH3分子的空间结构为_____ ,其中N原子的杂化轨道类型为_____ 。
您最近一年使用:0次
6 . 在工业上次磷酸 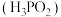 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: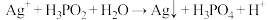 (未配平),已知
(未配平),已知 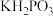 是次磷酸的正盐,请回答下列问题:
是次磷酸的正盐,请回答下列问题:
(1) 中,
中, 元素的化合价为
元素的化合价为_______ ;该反应中, 被
被_______ (填“氧化”或“还原”)。
(2)若该反应有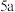 个电子转移,则镀件上银的质量为
个电子转移,则镀件上银的质量为_______  (已知每个银原子质量为
(已知每个银原子质量为 克)。
克)。
(3) 与足量
与足量  溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)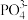 中
中 的价层电子对数为
的价层电子对数为_______ , 采取
采取_______ 杂化方式, 的空间结构为
的空间结构为_______ 。
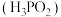 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: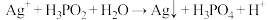 (未配平),已知
(未配平),已知 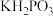 是次磷酸的正盐,请回答下列问题:
是次磷酸的正盐,请回答下列问题:(1)
 中,
中, 元素的化合价为
元素的化合价为 被
被(2)若该反应有
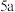 个电子转移,则镀件上银的质量为
个电子转移,则镀件上银的质量为 (已知每个银原子质量为
(已知每个银原子质量为 克)。
克)。(3)
 与足量
与足量  溶液反应的离子方程式:
溶液反应的离子方程式:(4)
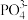 中
中 的价层电子对数为
的价层电子对数为 采取
采取 的空间结构为
的空间结构为
您最近一年使用:0次
名校
解题方法
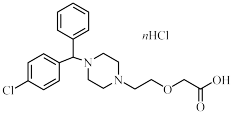
7 . 盐酸左西替利嗪是一种用于治疗荨麻疹的药物。其部分说明书如下:
(1)在左西替利嗪中添加盐酸的目的是___________ ;药品成分中n的值为___________ 。
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是___________ 。请在下图中用:“·”标出具有手性的碳原子。___________
| 盐酸左西替利嗪说明书 【成分】本品为西替利嗪的R型对映体,在过量盐酸中结晶制得。 【性状】本品外观是白色或类白色的片剂,易溶于水。
|
(2)市售的普通盐酸西替利嗪片也能治疗荨麻疹,而本品仍对西替利嗪的对映体进行分离,其可能原因是

| A.西替利嗪中,有9个碳原子与氮原子的杂化方式相同 |
| B.将西替利嗪溶于水,形成内盐 |
| C.两个苯环上的12个碳原子共平面 |
| D.分子内含有羧基和酯基 |
您最近一年使用:0次
解题方法
8 . 回答下列问题。
(1)N2H4是___________ (填“极性”或“非极性”)分子,N2H4中中心原子N杂化类型为___________ 。
(2)乙炔分子的碳原子采取什么杂化方式?___________ ;它的杂化轨道用于形成什么化学键?___________ ;怎样理解它存在碳碳三键?___________ 。
(3)向绿色的NiSO4溶液中滴加过量的氨水,溶液会变成深蓝色,其原因是溶液中生成了一种六配体的配离子,该配离子的化学式为___________ 。
(1)N2H4是
(2)乙炔分子的碳原子采取什么杂化方式?
(3)向绿色的NiSO4溶液中滴加过量的氨水,溶液会变成深蓝色,其原因是溶液中生成了一种六配体的配离子,该配离子的化学式为
您最近一年使用:0次
名校
9 . 我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、Ni等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填标号,下同)。
(2)B、C、N三种元素的电负性从大到小依次为___________ ,化合物 中的σ键和π键的比例是
中的σ键和π键的比例是___________ 。
(3) 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为 ,该配合物的配位原子为
,该配合物的配位原子为___________ (填序号),其中碳原子杂化方式为___________ 。写出一种与外界互为等电子体的分子___________ 。IMI中大π键可表示为___________ (已知苯中的大π键可表示为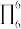 )。
)。
(4)镍能形成多种配合物,其中 是无色挥发性液体,而
是无色挥发性液体,而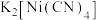 是红黄色单斜晶体。
是红黄色单斜晶体。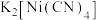 的熔点高于
的熔点高于 的原因是
的原因是___________ 。
(5)红银矿NiAs晶体结构如图所示:

①As原子的配位数是___________ 。
②已知 为阿伏加德罗常数的值,X射线光谱测算出的晶胞参数为
为阿伏加德罗常数的值,X射线光谱测算出的晶胞参数为 pm、
pm、 pm,则该晶体的密度为
pm,则该晶体的密度为___________ g/cm3(用含m、n的代数式表示)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填标号,下同)。
A. | B. |
C. | D. |
(2)B、C、N三种元素的电负性从大到小依次为
 中的σ键和π键的比例是
中的σ键和π键的比例是(3)
 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为 ,该配合物的配位原子为
,该配合物的配位原子为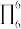 )。
)。(4)镍能形成多种配合物,其中
 是无色挥发性液体,而
是无色挥发性液体,而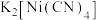 是红黄色单斜晶体。
是红黄色单斜晶体。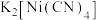 的熔点高于
的熔点高于 的原因是
的原因是(5)红银矿NiAs晶体结构如图所示:

①As原子的配位数是
②已知
 为阿伏加德罗常数的值,X射线光谱测算出的晶胞参数为
为阿伏加德罗常数的值,X射线光谱测算出的晶胞参数为 pm、
pm、 pm,则该晶体的密度为
pm,则该晶体的密度为
您最近一年使用:0次
名校
10 . S2Cl2和SCl2均为重要的化工产品。
(1)二氯化二硫是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。S2Cl2的结构式为______ ,其化学键类型有______ (填“极性键”或“非极性键”)。
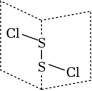
(2)S2Cl2中硫的化合价为______ ,S2Cl2分子中中心S原子的杂化轨道空间分布为______ ,S原子有______ 对孤电子对,S2Cl2是______ (填“极性”或“非极性”)分子。
(3)S2Cl2易发生水解反应,产生无色有刺激性气味的气体,同时生成淡黄色沉淀,该反应的化学方程式为______ 。
(4)实验室在111~140℃的温度下加热氯气和硫蒸气的混合物可制得S2Cl2,为检测所得物质中否纯净,某同学认为只要通过设计实验检测到有氯和硫两种元素存在,即可认为所得物质为纯净物的二氯化二硫。试从元素的价态分析并判断该同学的实验方案是否可行。______ 。
(1)二氯化二硫是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。S2Cl2的结构式为

(2)S2Cl2中硫的化合价为
(3)S2Cl2易发生水解反应,产生无色有刺激性气味的气体,同时生成淡黄色沉淀,该反应的化学方程式为
(4)实验室在111~140℃的温度下加热氯气和硫蒸气的混合物可制得S2Cl2,为检测所得物质中否纯净,某同学认为只要通过设计实验检测到有氯和硫两种元素存在,即可认为所得物质为纯净物的二氯化二硫。试从元素的价态分析并判断该同学的实验方案是否可行。
您最近一年使用:0次