名校
1 . 教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
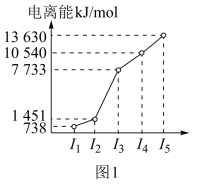
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有_______ 种不同运动状态的电子。
(2)如图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ 。

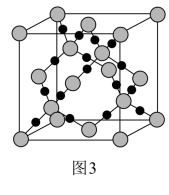
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于_______ 晶体。
(4)第一电离能介于Al、P之间的第三周期元素有_______ 种。 GaCl3原子的杂化方式为_______ 。写出与GaCl3结构相同的一种等电子体(写离子)_______ 。
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有_______ 个紧邻分子。D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是_______ (填字母标号)。
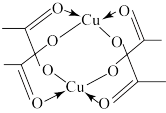
a.极性键 b.非极性键 c.配位键 d.金属键
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有

(2)如图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于

(4)第一电离能介于Al、P之间的第三周期元素有
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有

a.极性键 b.非极性键 c.配位键 d.金属键
您最近一年使用:0次
解题方法
2 . 据报道复旦大学修发贤教授课题组成功制备出砷化铌纳米带,并观测到其表面态具有百倍于金属铜薄膜和千倍于石墨烯的导电性。相关研究论文已在线发表于权威科学期刊《自然》。回答下列问题:
(1)铌元素(Nb)为一种金属元素,其基态原子的核外电子排布式为[Kr]4d55s1。下列是Nb的不同微粒的核外电子排布式,其中失去最外层1个电子所需能量最小的是___ (填标号)。
a.[Kr]4d35s15p1b.[Kr]4d45s1c.Kr]4d2d.Kr]4d3
(2)砷为第VA族元素,砷可以与某些有机基团形成有机化合物,如(ClCH=CH)2AsCl,其中As原子与2个C原子、1个Cl原子形成的VSEPR模型为____ 。
(3)英国曼彻斯特大学物理学家安德烈·盖姆和康斯坦丁诺沃肖洛夫用微机械剥离法成功从石墨中分离出石墨烯,因此共同获得2010年诺贝尔物理学奖;而石墨烯具有优异的光学、电学、力学特性在材料学、微纳加工、能源、生物医学和药物传递等方面具有重要的应用前景,被认为是一种未来革命性的材料。
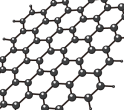
已知“石墨烯”的平面结构如图所示,一定条件下石墨烯与H2发生加成反应生成石墨烷,石墨烷中碳原子杂化类型是___ ,石墨烯导电的原因是____ 。
(4)石墨烯也可采用化学方法进行制备如采用六氯苯、六溴苯作为原料可制备石墨烯。下表给出了六氯苯、六溴苯、苯六酸俗名为蜜石酸的熔点和水溶性:
六溴苯的熔点比六氯苯高的原因是____ ,苯六酸与六溴苯、六氯苯的水溶性存在明显的差异本质原因是___ 。
(5)出于以更高效率利用太阳光等目的研制出金红石型铌氧氮化物(NbON),比以往的光学半导体更能够吸收长波长侧的光,作为光学半导体的新材料。该化合物的晶胞有如图所示的两种构型,若晶胞的边长为apm,该晶体的密度为__ g·cm-3。(NA是阿伏加 德罗常数的值,相关原子量:Nb—93)

(1)铌元素(Nb)为一种金属元素,其基态原子的核外电子排布式为[Kr]4d55s1。下列是Nb的不同微粒的核外电子排布式,其中失去最外层1个电子所需能量最小的是
a.[Kr]4d35s15p1b.[Kr]4d45s1c.Kr]4d2d.Kr]4d3
(2)砷为第VA族元素,砷可以与某些有机基团形成有机化合物,如(ClCH=CH)2AsCl,其中As原子与2个C原子、1个Cl原子形成的VSEPR模型为
(3)英国曼彻斯特大学物理学家安德烈·盖姆和康斯坦丁诺沃肖洛夫用微机械剥离法成功从石墨中分离出石墨烯,因此共同获得2010年诺贝尔物理学奖;而石墨烯具有优异的光学、电学、力学特性在材料学、微纳加工、能源、生物医学和药物传递等方面具有重要的应用前景,被认为是一种未来革命性的材料。
已知“石墨烯”的平面结构如图所示,一定条件下石墨烯与H2发生加成反应生成石墨烷,石墨烷中碳原子杂化类型是

(4)石墨烯也可采用化学方法进行制备如采用六氯苯、六溴苯作为原料可制备石墨烯。下表给出了六氯苯、六溴苯、苯六酸俗名为蜜石酸的熔点和水溶性:
| 物质 | 六氯苯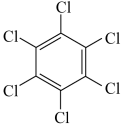 | 六溴苯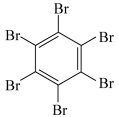 | 苯六酸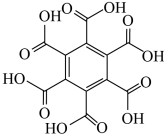 |
| 熔点/℃ | 231 | 325 | 287 |
| 水溶性 | 不溶 | 不溶 | 易溶 |
六溴苯的熔点比六氯苯高的原因是
(5)出于以更高效率利用太阳光等目的研制出金红石型铌氧氮化物(NbON),比以往的光学半导体更能够吸收长波长侧的光,作为光学半导体的新材料。该化合物的晶胞有如图所示的两种构型,若晶胞的边长为apm,该晶体的密度为

您最近一年使用:0次
名校
3 . 根据物质结构有关性质和特点,回答以下问题:
(1)过渡元素Co 基态原子价电子轨道表达式为_______________________________ 。第四电离能I4 (Co) < I4 (Fe) ,其原因是__________________________________________ 。
(2)磷的氯化物有两种:PCl3和PCl5 ,PCl3中磷原子的杂化类型为__________ ,PCl3的立体构型为__________ ,其中PCl3的沸点________ (填“大于”或“小于”)PCl5,原因是__________ 。
(3)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如下图所示,该分子中存在的化学键为___________ (填选项字母)
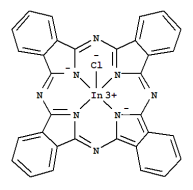
a.σ键 b.π键 c.离子键 d.配位键
(4)氯有多种含氧酸,其电离平衡常数如下:
从物质结构的角度解释以上含氧酸 Ka 依次减小的原因________________________ 。
(5)钴的一种化合物的晶胞结构如下图所示:
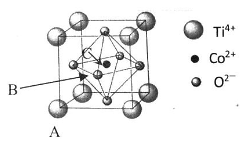
①已知A点的原子坐标参数为(0,0,0),C 点为(1/2,1/2,1/2),则B点的原子坐标参数为___________ 。
②已知晶胞参数 a = 0.5485 nm,则该晶体的密度为_______________ g/cm3。(列出计算表达式即可)
(1)过渡元素Co 基态原子价电子轨道表达式为
(2)磷的氯化物有两种:PCl3和PCl5 ,PCl3中磷原子的杂化类型为
(3)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如下图所示,该分子中存在的化学键为

a.σ键 b.π键 c.离子键 d.配位键
(4)氯有多种含氧酸,其电离平衡常数如下:
| 化学式 | HClO4 | HClO3 | HClO2 | HClO |
| Ka | 1×1010 | 1×10 | 1×10‾2 | 4×10‾8 |
从物质结构的角度解释以上含氧酸 Ka 依次减小的原因
(5)钴的一种化合物的晶胞结构如下图所示:


①已知A点的原子坐标参数为(0,0,0),C 点为(1/2,1/2,1/2),则B点的原子坐标参数为
②已知晶胞参数 a = 0.5485 nm,则该晶体的密度为
您最近一年使用:0次
2018-11-01更新
|
519次组卷
|
2卷引用:内蒙古巴彦淖尔一中2019届高三上学期第二次月考理综化学试题
名校
4 . A、B、C、D、E、F为前四周期原子序数依次增大的六种元素,A、C、D原子均有两个未成对电子,A、B、C同周期,A与D、B与F分别同主族,E是生活中用量最大的金属。请回答下列问题:
(1)E比较稳定的离子核外电子排布式_____________________________ .
(2)A、B、C的第一电离能由小到大的顺序为_________________  用元素符号表示
用元素符号表示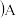 、B、C的简单氢化物中最易汽化的物质的化学式
、B、C的简单氢化物中最易汽化的物质的化学式___________ .
(3)C与D形成的物质的晶体类型是____________ ,IT产业中该晶体用于生产____________ .
(4)由A、B、C三种元素中的一种或两种元素形成的分子中,有的互为等电子体,写出其中一组等电子体的化学式:______  并写出对应的结构式
并写出对应的结构式_______________ .
(5)B的单质晶胞与 的相似,则一个晶胞中含B的原子个数为
的相似,则一个晶胞中含B的原子个数为____ 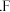 与氢形成的分子空间构型是
与氢形成的分子空间构型是_______ .
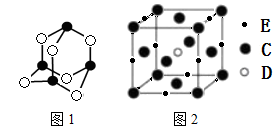
(6)“砒霜”是一种含C,F的化合物,其分子结构如图1所示,该化合物的分子式为F4C6,F原子采取______ 杂化;C,D,E组成的化合物的晶胞如图2,其晶胞参数为a pm,则其密度为___________________ g/cm3(列出式子即可,阿伏伽德罗常数为NAmol-1)。
(1)E比较稳定的离子核外电子排布式
(2)A、B、C的第一电离能由小到大的顺序为
 用元素符号表示
用元素符号表示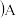 、B、C的简单氢化物中最易汽化的物质的化学式
、B、C的简单氢化物中最易汽化的物质的化学式(3)C与D形成的物质的晶体类型是
(4)由A、B、C三种元素中的一种或两种元素形成的分子中,有的互为等电子体,写出其中一组等电子体的化学式:
 并写出对应的结构式
并写出对应的结构式(5)B的单质晶胞与
 的相似,则一个晶胞中含B的原子个数为
的相似,则一个晶胞中含B的原子个数为 与氢形成的分子空间构型是
与氢形成的分子空间构型是(6)“砒霜”是一种含C,F的化合物,其分子结构如图1所示,该化合物的分子式为F4C6,F原子采取

您最近一年使用:0次



