名校
解题方法
1 . 晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、氮、钛、钴、钙等多种化学物质。请回答下列问题:
(1)科学家常利用仪器进行___________ 实验来区分晶体硼和无定形硼,二者之间的关系互为___________ 。第二周期元素的第一电离能按由小到大的顺序排列,B元素排在第___________ 位,其基态能量最高的能级电子云轮廓图为___________ 形。
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为___________ ,Si原子的杂化类型为___________ 。 的几何构型为正八面体形,Co在中心。
的几何构型为正八面体形,Co在中心。 中,1个Co提供
中,1个Co提供___________ 个空轨道。该配位离子的作用力为___________ (填序号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键
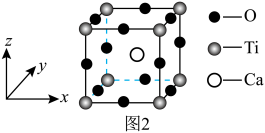
(4)一种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。与Ti紧邻的Ca有___________ 个。晶胞中Ca原子坐标参数为___________ 。
(1)科学家常利用仪器进行
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为

 的几何构型为正八面体形,Co在中心。
的几何构型为正八面体形,Co在中心。 中,1个Co提供
中,1个Co提供A.金属键 B.离子键 C.共价键 D.配位键 E.氢键
(4)一种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。与Ti紧邻的Ca有
您最近一年使用:0次
名校
2 . 按要求回答下列问题:
(1)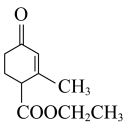 中含有的含氧官能团的名称为
中含有的含氧官能团的名称为___________ 。
(2)某有机物结构如图所示,下列说法正确的是___________ (填序号)。
③分子中C原子的杂化方式为 杂化 ④该分子是非极性分子
杂化 ④该分子是非极性分子
(3)TiO2是环境友好材料,能光催化降解有机物。纳米TiO2催化处理污水的一个实例如图所示。___________ ;化合物乙中有___________ 个手性碳原子。
(4)有A、B两种烃,已知:
( )B完全燃烧的产物
)B完全燃烧的产物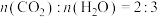 。
。
( )A是B分子中的氢原子全部被甲基取代后的产物;A遇
)A是B分子中的氢原子全部被甲基取代后的产物;A遇 的
的 溶液不褪色,其一氯代物只有一种。
溶液不褪色,其一氯代物只有一种。
①写出B与溴在光照下的反应方程式___________ (只写一取代)。
②A的结构简式为___________ ,系统命名为___________ 。
(1)
 中含有的含氧官能团的名称为
中含有的含氧官能团的名称为(2)某有机物结构如图所示,下列说法正确的是
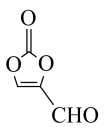
③分子中C原子的杂化方式为
 杂化 ④该分子是非极性分子
杂化 ④该分子是非极性分子(3)TiO2是环境友好材料,能光催化降解有机物。纳米TiO2催化处理污水的一个实例如图所示。

(4)有A、B两种烃,已知:
(
 )B完全燃烧的产物
)B完全燃烧的产物 。
。(
 )A是B分子中的氢原子全部被甲基取代后的产物;A遇
)A是B分子中的氢原子全部被甲基取代后的产物;A遇 的
的 溶液不褪色,其一氯代物只有一种。
溶液不褪色,其一氯代物只有一种。①写出B与溴在光照下的反应方程式
②A的结构简式为
您最近一年使用:0次
名校
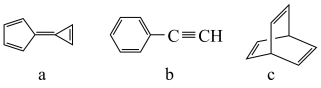
3 . 有机物a、b、c的结构如图所示:___________ 种(不考虑立体异构);
(2)b的名称为___________ ;
(3)c中碳原子的杂化方式为___________ 。
(2)b的名称为
(3)c中碳原子的杂化方式为
您最近一年使用:0次
4 . 铜的配合物在自然界中广泛存在,已知铜离子的配位数通常为4,请回答下列问题:
(1)基态29Cu的核外电子排布式为___________ 。
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子___________ (填化学式),配体中提供孤电子对的原子是___________ (填元素符号)。
②SO 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为___________ 。
(3)同学甲设计如图制备铜的配合物的实验:___________ 。
②由上述实验可得出以下结论:结论1:配合物的形成与___________ 、___________ 有关。
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:___________ >___________ (填化学式)。
(1)基态29Cu的核外电子排布式为
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子
②SO
 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为(3)同学甲设计如图制备铜的配合物的实验:

②由上述实验可得出以下结论:结论1:配合物的形成与
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:
您最近一年使用:0次
5 . 回答下列问题:
青蒿素为无色针状结晶,熔点156℃,沸点390℃;是一种能治疗疟疾的有机化合物。其分子结构如图所示:___________ (填字母)。
a.分子中含有过氧键、醚键和酯基 b.分子式为:C15H22O5
c.属于芳香族化合物 d.分子中碳原子杂化形式均为sp3杂化
(2)《肘后备急方》中记载“青蒿一握,以水二升渍,绞取汁”。涉及的分离提纯操作是___________ 。
a.固液萃取 b.液液萃取
(3)我国科学家屠呦呦受此启发,成功用有机溶剂A提取青蒿素。使用现代分析仪器对有机物A的分子结构进行测定,相关结果如图:___________ ;其结构简式为___________ 。
②已知有机溶剂A的沸点34.6℃,青蒿素易溶于有机溶剂A,屠呦呦选择有机溶剂A提取青蒿素的原因有___________ 。
③以黄花蒿提取青蒿素的实验方案:取一定量的黄花蒿,干燥(或晒干),粉碎,用一定量的有机溶剂A浸没黄花蒿一段时间后,___________ (选填“过滤”“萃取”或“蒸馏”),用有机溶剂A洗涤2-3次,取滤液于蒸馏烧瓶中用___________ ℃的热水浴进行蒸馏即得青蒿素。
青蒿素为无色针状结晶,熔点156℃,沸点390℃;是一种能治疗疟疾的有机化合物。其分子结构如图所示:
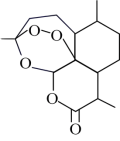
a.分子中含有过氧键、醚键和酯基 b.分子式为:C15H22O5
c.属于芳香族化合物 d.分子中碳原子杂化形式均为sp3杂化
(2)《肘后备急方》中记载“青蒿一握,以水二升渍,绞取汁”。涉及的分离提纯操作是
a.固液萃取 b.液液萃取
(3)我国科学家屠呦呦受此启发,成功用有机溶剂A提取青蒿素。使用现代分析仪器对有机物A的分子结构进行测定,相关结果如图:
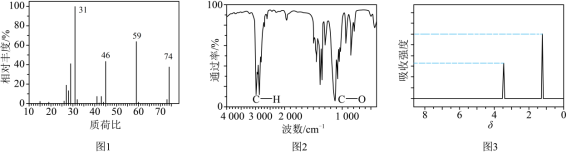
②已知有机溶剂A的沸点34.6℃,青蒿素易溶于有机溶剂A,屠呦呦选择有机溶剂A提取青蒿素的原因有
③以黄花蒿提取青蒿素的实验方案:取一定量的黄花蒿,干燥(或晒干),粉碎,用一定量的有机溶剂A浸没黄花蒿一段时间后,
您最近一年使用:0次
名校
6 . 按照要求填空:
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
(2)① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。
①既有 键,又有
键,又有 键的是
键的是_______ (用序号作答);既含有极性键又含有非极性键的极性分子的电子式为_______ ;既含有极性键又含有非极性键的非极性分子中碳原子的杂化方式为________ ;苯环中存在的大 键可表示为
键可表示为________ 。
②属于离子化合物的物质的电子式为______ ; 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为_____ ; 中
中 键和
键和 键之比为
键之比为______ 。
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
| 序号 | 化学式 | 分子的极性 | 空间构型 | 中心原子的杂化方式 |
| ① |  | |||
| ② |  | |||
| ③ |  | - |
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。①既有
 键,又有
键,又有 键的是
键的是 键可表示为
键可表示为②属于离子化合物的物质的电子式为
 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为 中
中 键和
键和 键之比为
键之比为
您最近一年使用:0次
名校
7 .  是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。
1. 的分子构型为
的分子构型为___________ ; 与
与 互为等电子体,等电子体的化学键类型和空间结构相同,则
互为等电子体,等电子体的化学键类型和空间结构相同,则 的中心原子杂化轨道类型为
的中心原子杂化轨道类型为___________ 。
2.已知拆开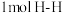 、
、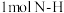 、
、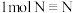 分别需要的能量是
分别需要的能量是 、
、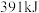 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为___________ 。若该反应的焓变和熵变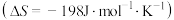 随温度变化很小,则该反应在常温下
随温度变化很小,则该反应在常温下___________ (填“能”或者“不能”)自发进行。合成氨反应加入催化剂后的反应历程示意图为下图中的___________ (填编号)。 左右高温的原因是
左右高温的原因是___________ 。
 是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。1.
 的分子构型为
的分子构型为 与
与 互为等电子体,等电子体的化学键类型和空间结构相同,则
互为等电子体,等电子体的化学键类型和空间结构相同,则 的中心原子杂化轨道类型为
的中心原子杂化轨道类型为2.已知拆开
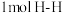 、
、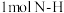 、
、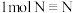 分别需要的能量是
分别需要的能量是 、
、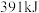 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为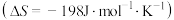 随温度变化很小,则该反应在常温下
随温度变化很小,则该反应在常温下
 左右高温的原因是
左右高温的原因是
您最近一年使用:0次
名校
8 . 钛能与卤素单质发生反应,生成用途多样的卤化钛。
(1)卤族元素(F、Cl、Br、I)随着原子序数的递增,相关性质逐渐增强或变大的是___________。
(2) 易与
易与 结合,下列关于
结合,下列关于 分子说法错误的是___________。
分子说法错误的是___________。
(1)卤族元素(F、Cl、Br、I)随着原子序数的递增,相关性质逐渐增强或变大的是___________。
| A.元素的电负性 | B.简单离子的还原性 |
| C.气态氢化物的热稳定性 | D.最高价氧化物对应水化物的酸性 |
 易与
易与 结合,下列关于
结合,下列关于 分子说法错误的是___________。
分子说法错误的是___________。A.键角为 | B.是极性分子 |
C.含有 键 键 | D.中心原子采取 杂化 杂化 |
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题
(1) 分子的中心原子的杂化类型
分子的中心原子的杂化类型___________ 。
(2) 分子中共价键的类型分别是_______。
分子中共价键的类型分别是_______。
(1)
 分子的中心原子的杂化类型
分子的中心原子的杂化类型(2)
 分子中共价键的类型分别是_______。
分子中共价键的类型分别是_______。A. 键、非极性健 键、非极性健 | B. 键、极性键 键、极性键 |
C. 键、非极性键 键、非极性键 | D. 键、极性键 键、极性键 |
您最近一年使用:0次
名校
解题方法
10 . 硫元素能形成多种微粒如 、
、 、
、 、
、 、
、 等,
等, 分子的立体构型为
分子的立体构型为___________ , 的中心原子的杂化类型是
的中心原子的杂化类型是___________ 。
 、
、 、
、 、
、 、
、 等,
等, 分子的立体构型为
分子的立体构型为 的中心原子的杂化类型是
的中心原子的杂化类型是
您最近一年使用:0次



