1 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:(已知: 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)
(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为___________ ;配合物 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是___________ (填元素符号)。
(2)现有下列实验:___________ ,溶剂X可以是___________ (填名称),继续添加氨水,沉淀溶解的离子方程式为___________ 。
②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是___________ 。
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为
 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是(2)现有下列实验:

②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | 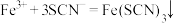 |
| B | 向由0.1mol CrCl3∙6H2O配成的溶液中加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知Cr3+的配位数为6,则CrCl3∙6H2O的化学式可表示为 |
| C | 向K2Cr2O7溶液中先滴加3滴浓硫酸,再改加10滴浓NaOH | 溶液先橙色加深,后变为黄色 | 溶液中存在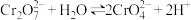 |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 配合物能定性可用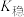 表示,对于配位反应:
表示,对于配位反应: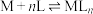
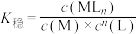 (M代表中心离子或原子,L代表配体)。
(M代表中心离子或原子,L代表配体)。 的配位化合物较稳定且应用广泛,
的配位化合物较稳定且应用广泛, 可与
可与 、
、 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的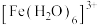 、红色的
、红色的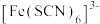 、无色的
、无色的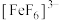 、黄色的
、黄色的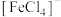 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的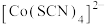 配离子;
配离子; 不能与
不能与 形成配离子。下列说法不正确的是
形成配离子。下列说法不正确的是
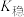 表示,对于配位反应:
表示,对于配位反应: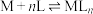
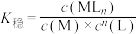 (M代表中心离子或原子,L代表配体)。
(M代表中心离子或原子,L代表配体)。 的配位化合物较稳定且应用广泛,
的配位化合物较稳定且应用广泛, 可与
可与 、
、 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的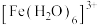 、红色的
、红色的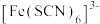 、无色的
、无色的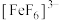 、黄色的
、黄色的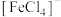 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: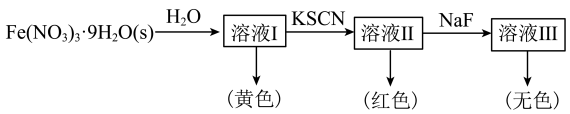
 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的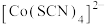 配离子;
配离子; 不能与
不能与 形成配离子。下列说法不正确的是
形成配离子。下列说法不正确的是A.为了能观察到溶液Ⅰ中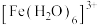 的颜色,可向该溶液中加入稀盐酸 的颜色,可向该溶液中加入稀盐酸 |
| B.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色 |
C.可用NaF和KSCN溶液检验 溶液中是否含有 溶液中是否含有 |
D.反应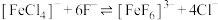 的平衡常数 的平衡常数 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法正确的是
A.配位能力 大于 大于 ,向 ,向 中加过量氨水生成 中加过量氨水生成 |
B. 的相对分子质量更大,所以 的相对分子质量更大,所以 的熔点高于 的熔点高于 |
C.可燃冰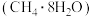 的形成是由于甲烷分子与水分子之间存在氢键 的形成是由于甲烷分子与水分子之间存在氢键 |
D.乳酸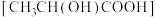 分子中存在2个手性碳原子 分子中存在2个手性碳原子 |
您最近一年使用:0次
名校
解题方法
4 . 从废旧CPU中回收Au、Ag、Cu的部分流程如下: ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.酸溶时,硝酸只体现氧化性 |
B.向过滤所得滤液中加入过量浓氨水,可以分离 、 、 |
| C.溶金时NaCl作用为增强硝酸的氧化性 |
D.向1mol 中加入过量Zn使其完全还原为Au,需消耗2mol Zn 中加入过量Zn使其完全还原为Au,需消耗2mol Zn |
您最近一年使用:0次
解题方法
5 . 某实验小组以粗镍(含少量 和
和 杂质)为原料制备
杂质)为原料制备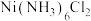 ,并测定相关组分的含量,制备流程示意图如下:
,并测定相关组分的含量,制备流程示意图如下: 为绿色难溶物;
为绿色难溶物;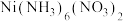 、
、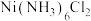 均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是
均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是
 和
和 杂质)为原料制备
杂质)为原料制备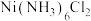 ,并测定相关组分的含量,制备流程示意图如下:
,并测定相关组分的含量,制备流程示意图如下:
 为绿色难溶物;
为绿色难溶物;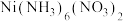 、
、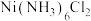 均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是
均为可溶于水的蓝紫色晶体,碱性条件下稳定存在,下列说法不正确的是A.试剂X的作用是调节 除去 除去 和 和 杂质,则试剂X可为 杂质,则试剂X可为 |
B.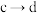 过程的转化离子方程式为 过程的转化离子方程式为 |
C.实验配制3.0 稀硝酸250 稀硝酸250 需要的玻璃仪器有烧杯、量筒、玻璃棒、250 需要的玻璃仪器有烧杯、量筒、玻璃棒、250 容量瓶 容量瓶 |
| D.步骤c、d中为防止氨水分解及降低固体溶解度需0~10℃冷水浴控温,则温度计应在水浴中 |
您最近一年使用:0次
解题方法
6 . 氮氧化物( )是硝酸和肼等工业的主要污染物。一种以沸石笼作为载体对氮氧化物进行催化还原的原理及A在沸石笼内转化为B、C、D等中间体的过程如图,下列说法不正确的是
)是硝酸和肼等工业的主要污染物。一种以沸石笼作为载体对氮氧化物进行催化还原的原理及A在沸石笼内转化为B、C、D等中间体的过程如图,下列说法不正确的是
 )是硝酸和肼等工业的主要污染物。一种以沸石笼作为载体对氮氧化物进行催化还原的原理及A在沸石笼内转化为B、C、D等中间体的过程如图,下列说法不正确的是
)是硝酸和肼等工业的主要污染物。一种以沸石笼作为载体对氮氧化物进行催化还原的原理及A在沸石笼内转化为B、C、D等中间体的过程如图,下列说法不正确的是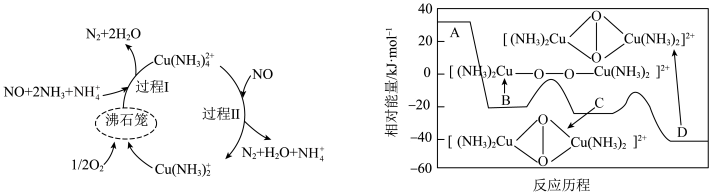
A.脱除 的总反应为 的总反应为 |
B.其他条件不变时,增大 , , 的平衡转化率下降 的平衡转化率下降 |
| C.A、B、C、D中比较稳定是D |
| D.沸石笼中的反应过程氧化剂与还原剂的物质的量比为1:2 |
您最近一年使用:0次
名校
7 . 银氨溶液不能储存,因为放置时会析出有强爆炸性的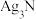 沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下:
沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下: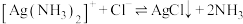 ;
; 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。下列说法正确的是
。下列说法正确的是
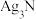 沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下:
沉淀。可通过加入盐酸转化为AgCl沉淀回收,还可利用羟胺回收银,反应如下: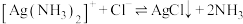 ;
; 。设阿伏加德罗常数值为
。设阿伏加德罗常数值为 。下列说法正确的是
。下列说法正确的是A.向银氨溶液中加入1mol HCl,可以回收AgCl为 |
B.1mol/L  溶液含有配位键数为2 溶液含有配位键数为2 |
C.等物质的量的 和羟胺均含有3 和羟胺均含有3 个氢原子 个氢原子 |
D.羟胺有强还原性,当反应中转移电子数为2 时,需消耗2mol 时,需消耗2mol  |
您最近一年使用:0次
名校
解题方法
8 . 根据实验目的设计方案并进行实验,其中方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
A |  水解过程的热效应 水解过程的热效应 | 取适量 溶液于试管中,测定pH然后加热一段时间,冷却至原温度,再次测定该溶液的pH 溶液于试管中,测定pH然后加热一段时间,冷却至原温度,再次测定该溶液的pH | pH变小 |  水解过程为放热过程 水解过程为放热过程 |
B | 检验淀粉的水解程度 | 向淀粉水解液中加入10% NaOH溶液至溶液显碱性,再加入少量碘水 | 溶液不变蓝 | 淀粉完全水解 |
C | 比较相同浓度的 溶液和 溶液和 溶液的酸碱性 溶液的酸碱性 | 用洁净干燥的玻璃棒分别蘸取同浓度的 溶液和 溶液和 溶液滴在pH试纸上,与标准比色卡比较 溶液滴在pH试纸上,与标准比色卡比较 |  溶液对应的pH更小 溶液对应的pH更小 |  溶液的酸性更强 溶液的酸性更强 |
D | 比较配离子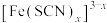 和 和 的稳定性 的稳定性 | 向盛有少量蒸馏水的试管里滴加2滴0.1molL  溶液,然后再滴加2滴0.6mol/L KSCN溶液 溶液,然后再滴加2滴0.6mol/L KSCN溶液 | 溶液颜色不变 |  较稳定 较稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 酞菁与钴酞菁的分子结构如图所示,已知酞菁分子中所有原子共平面。下列说法错误的是
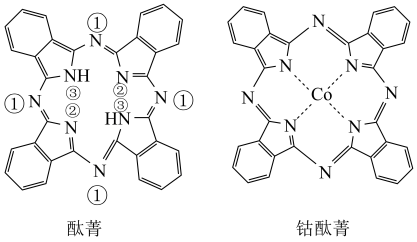
A.酞菁分子中三种N原子的杂化方式均为 |
| B.酞菁分子中p轨道能提供一对电子的N原子是② |
| C.钴酞菁中存在配位键 |
| D.钴酞菁中钴离子为+2价 |
您最近一年使用:0次
10 . 卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有________ ,其中能量较高的是________ 。(填标号)
A. B.
B. C.
C.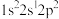 D.
D.
(2)基态Br原子的核外电子排布式为________ 。
(3) 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是________ ,中心离子的配位数为________ 。
(4)Kr是第四周期的稀有气体元素,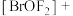 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为________ 。
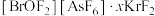 晶体中的微粒间作用力有
晶体中的微粒间作用力有________ (填标号)。
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在 形式,画出
形式,画出 的链状结构
的链状结构________ 。
(6)四氟乙烯 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为________ 和________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因________ 。
(1)氟原子激发态的电子排布式有
A.
 B.
B. C.
C.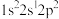 D.
D.
(2)基态Br原子的核外电子排布式为
(3)
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(4)Kr是第四周期的稀有气体元素,
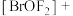 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为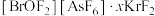 晶体中的微粒间作用力有
晶体中的微粒间作用力有a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在
 形式,画出
形式,画出 的链状结构
的链状结构(6)四氟乙烯
 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为
您最近一年使用:0次



