名校
解题方法
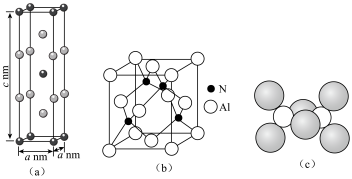
1 . Al元素可以形成多种类型的物质。例如AlCr2晶体具有体心四方结构,如图(a)所示;AlN晶胞结构如图(b)所示;气态AlCl3通常以二聚体Al2Cl6形式存在,其空间结构如图(c)所示。下列说法正确的是

A.基态铬原子的核外电子排布式为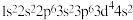 |
B.AlCr2晶体的密度为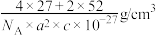 |
| C.AlN中各原子均未达到8电子稳定结构 |
D.二聚体Al2Cl6中Al的轨道杂化类型为 |
您最近一年使用:0次
名校
解题方法
2 . 以银锰精矿(主要含 、MnS、
、MnS、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取精银、Mn及
)为原料联合提取精银、Mn及 的一种流程示意图如下。
的一种流程示意图如下。
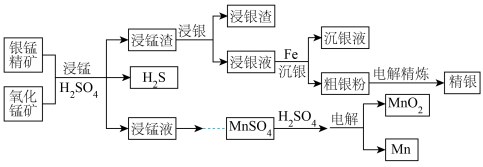
已知:酸性条件下, 的氧化性强于
的氧化性强于 。
。
(1)“浸锰”是在 溶液中使矿石中的锰元素浸出的过程,能同时去除
溶液中使矿石中的锰元素浸出的过程,能同时去除 ,且有利于后续银的浸出,矿石中的银以
,且有利于后续银的浸出,矿石中的银以 的形式残留于浸锰渣中。
的形式残留于浸锰渣中。
①“浸锰”过程中,发生反应 ,推断:
,推断: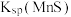
___________ 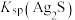 (填“>”或“<”)。
(填“>”或“<”)。
②在 溶液中,银锰精矿中的
溶液中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有___________ 。
(2)“浸银”时,使用过量 、HCl、
、HCl、 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出。
形式浸出。
①将“浸银”反应的离子方程式补充完整__________ 。
_______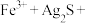 ________
________ ________
________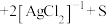
②结合平衡移动原理,解释浸出剂中 的作用:
的作用:___________ 。
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,

回答下列问题:
①___________ 极为“粗银电极”(填“a”或“b”)。
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为___________ ;当电路中通过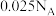 电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为
电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为___________ mL(保留三位有效数字)。
(4)电解 溶液提取Mn以及
溶液提取Mn以及 ,写出在阳极获取
,写出在阳极获取 的电极方程式
的电极方程式___________ 。
 、MnS、
、MnS、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取精银、Mn及
)为原料联合提取精银、Mn及 的一种流程示意图如下。
的一种流程示意图如下。
已知:酸性条件下,
 的氧化性强于
的氧化性强于 。
。(1)“浸锰”是在
 溶液中使矿石中的锰元素浸出的过程,能同时去除
溶液中使矿石中的锰元素浸出的过程,能同时去除 ,且有利于后续银的浸出,矿石中的银以
,且有利于后续银的浸出,矿石中的银以 的形式残留于浸锰渣中。
的形式残留于浸锰渣中。①“浸锰”过程中,发生反应
 ,推断:
,推断: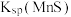
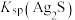 (填“>”或“<”)。
(填“>”或“<”)。②在
 溶液中,银锰精矿中的
溶液中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有(2)“浸银”时,使用过量
 、HCl、
、HCl、 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出。
形式浸出。①将“浸银”反应的离子方程式补充完整
_______
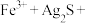 ________
________ ________
________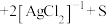
②结合平衡移动原理,解释浸出剂中
 的作用:
的作用:(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,

回答下列问题:
①
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为
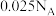 电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为
电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为(4)电解
 溶液提取Mn以及
溶液提取Mn以及 ,写出在阳极获取
,写出在阳极获取 的电极方程式
的电极方程式
您最近一年使用:0次
名校
解题方法
3 . 已知 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.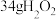 中含有共用电子对数目为 中含有共用电子对数目为 |
B. 与足量硝酸银溶液反应,生成 与足量硝酸银溶液反应,生成 为 为 |
C. 反应生成的 反应生成的 胶粒数小于 胶粒数小于 |
D. 和 和 的混合气体完全燃烧,消耗 的混合气体完全燃烧,消耗 分子数为 分子数为 |
您最近一年使用:0次
名校
解题方法
4 . 设NA为阿伏加德罗常数的值,下列有关说法错误的是
| A.46g乙醇中sp3杂化的原子数为3NA |
| B.0.2mol[Cu(NH3)4]2+中σ键的个数为2.4NA |
| C.40gSiC晶体中含有的共价键数为4NA |
| D.0.5mol羟基中含有的电子数为4.5NA |
您最近一年使用:0次
名校
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A. 的 的 溶液中 溶液中 数目为 数目为 |
B. 乙酸乙酯在酸催化条件下水解生成 乙酸乙酯在酸催化条件下水解生成 乙酸和 乙酸和 乙醇 乙醇 |
C. 的浓 的浓 与足量 与足量 反应,转移的电子数为 反应,转移的电子数为 |
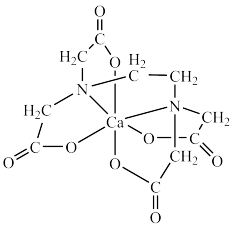
D.金属络合剂EDTA二钠与 形成配合物结构如图所示, 形成配合物结构如图所示, 该粒子含有的配位键数目为 该粒子含有的配位键数目为 ,五元环数目为 ,五元环数目为 |
您最近一年使用:0次
名校
6 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol羟基所含的电子的数目为0.7NA |
B.1mol环戊二烯(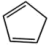 )中含有键的数目是11NA,键的数目为2NA )中含有键的数目是11NA,键的数目为2NA |
| C.1molK3[Fe(CN)6]中配位键的数目为9NA |
D.0.1mol·L−1CH3COOH溶液中CH3COOH和 数目之和为0.1NA 数目之和为0.1NA |
您最近一年使用:0次
名校
解题方法
7 . 下列反应的离子方程式书写正确的是
A.用硫酸铜溶液吸收硫化氢气体: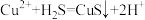 |
B.向过量的NaHSO3溶液中滴加少量“84”消毒液: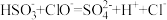 |
C.过量氨水与硫酸铝溶液反应: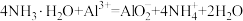 |
D.向CuSO4溶液中加入过量浓氨水: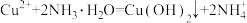 |
您最近一年使用:0次
名校
解题方法
8 . 含硼储氢材料(如 等)在生产中有着广泛的应用。一种新型含硼储氢材料的晶胞,晶胞参数如图所示,晶胞棱边夹角均为
等)在生产中有着广泛的应用。一种新型含硼储氢材料的晶胞,晶胞参数如图所示,晶胞棱边夹角均为 。设阿伏加德罗常数的值为
。设阿伏加德罗常数的值为 ,下列说法不正确的是
,下列说法不正确的是
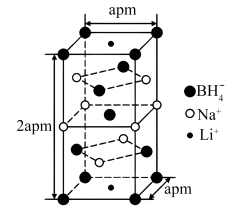
 等)在生产中有着广泛的应用。一种新型含硼储氢材料的晶胞,晶胞参数如图所示,晶胞棱边夹角均为
等)在生产中有着广泛的应用。一种新型含硼储氢材料的晶胞,晶胞参数如图所示,晶胞棱边夹角均为 。设阿伏加德罗常数的值为
。设阿伏加德罗常数的值为 ,下列说法不正确的是
,下列说法不正确的是
| A.在同周期元素中,第一电离能比B大的共有6种 |
B. 的VSEPR模型和离子的空间结构均为正四面体形 的VSEPR模型和离子的空间结构均为正四面体形 |
C.该晶体的化学式为 ,密度为 ,密度为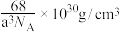 |
D. 分子中, 分子中, 化学键称为配位键,其电子对由B提供 化学键称为配位键,其电子对由B提供 |
您最近一年使用:0次
2023-09-10更新
|
429次组卷
|
2卷引用:重庆市第一中学校2022-2023学年高三上学期12月月考化学试题
9 . 某小组探究Cu与 在不同条件下的反应,实验结果如下表:
在不同条件下的反应,实验结果如下表:
下列说法不正确的是
 在不同条件下的反应,实验结果如下表:
在不同条件下的反应,实验结果如下表: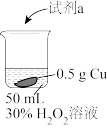 | 实验 | 试剂a | 现象与结果 |
| Ⅰ | 10h后,液体变为浅蓝色,将铜片取出、干燥,铜表面附着蓝色固体 | ||
| Ⅱ | 8mL5mol/L氨水 | 立即产生大量气泡,溶液变为深蓝色,将铜片取出、铜表面附着蓝色固体 | |
| Ⅲ | 8mL5mol/L氨水和1g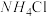 固体 固体 | 立即产生大量气泡,溶液变为深蓝色,且颜色比Ⅱ深,将铜片取出、干燥,铜片依然保持光亮 |
| A.已知Ⅰ为空白组,则此时试剂a为8mL蒸馏水 |
B.对比Ⅰ和Ⅱ可知,增大溶液中 可以增强 可以增强 的氧化性 的氧化性 |
C.增大 有利于 有利于 的生成 的生成 |
D. 可能是 可能是 分解的催化剂 分解的催化剂 |
您最近一年使用:0次
名校
10 . 以甲醇为溶剂, 可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是
可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是
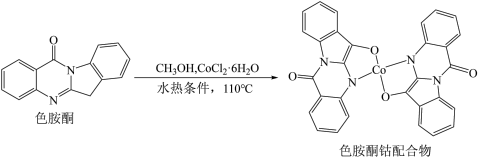
 可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是
可与色胺酮分子配位结合,形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示)。下列说法不正确的是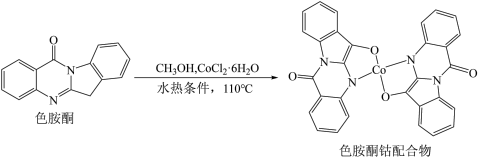
| A.色胺酮分子中所含元素电负性大小关系为:H<C<N<O |
B.色胺酮分子中的碳均采取 杂化 杂化 |
| C.色胺酮钴配合物中钴的配位数为4 |
D.色胺酮钴配合物晶胞中还含有一个 分子, 分子, 通过氢键与色胺酮钴配合物相结合 通过氢键与色胺酮钴配合物相结合 |
您最近一年使用:0次



