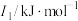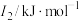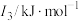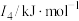名校
解题方法
1 . 联氨(N2H4)为二元弱碱,在水中性质与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。
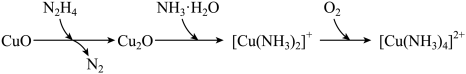
| A.N2H4中N的杂化类型为sp2 | B. 中配位原子是H 中配位原子是H |
| C.基态原子核外未成对电子数:N>O | D.第一电离能: |
您最近一年使用:0次
7日内更新
|
106次组卷
|
5卷引用:山西省运城市康杰中学2024-2025学年高三上学期一模考试 化学试题
名校
解题方法
2 . 亚铜配合物广泛用作催化剂。实验室制备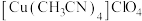 的反应原理如下:
的反应原理如下:
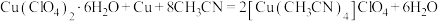
实验步骤如下: 和
和 粉置于
粉置于 乙腈(
乙腈( )中反应,回流装置图和蒸馏装置图(加热、夹持等装置略)如下:
)中反应,回流装置图和蒸馏装置图(加热、夹持等装置略)如下:
②相关物质的信息如下:
回答下列问题:
(1)装置 中仪器M的名称为
中仪器M的名称为___________ 。
(2)装置 中反应完全的现象是
中反应完全的现象是___________ 。
(3)装置 和
和 中N2气球的作用是
中N2气球的作用是___________ 。
(4)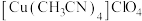 不能由步骤c直接获得,而是先蒸馏至接近饱和,再经步骤d冷却结晶获得。这样处理的目的是
不能由步骤c直接获得,而是先蒸馏至接近饱和,再经步骤d冷却结晶获得。这样处理的目的是___________ 。
(5)为了使母液中的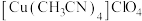 结晶,步骤e中向母液中加入的最佳溶剂是
结晶,步骤e中向母液中加入的最佳溶剂是___________ (填标号)。
A.水 B.乙醇 C.乙醚
(6)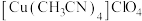 中存在的化学键有
中存在的化学键有___________ (填标号)。
A.离子键 B.共价键 C.氢键 D.配位键 E.金属键
(7)合并步骤d和e所得的产物,总质量为 ,则总收率为
,则总收率为___________ (用百分数表示,保留一位小数)。
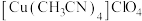 的反应原理如下:
的反应原理如下: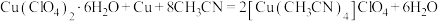
实验步骤如下:
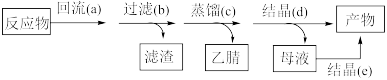
 和
和 粉置于
粉置于 乙腈(
乙腈( )中反应,回流装置图和蒸馏装置图(加热、夹持等装置略)如下:
)中反应,回流装置图和蒸馏装置图(加热、夹持等装置略)如下: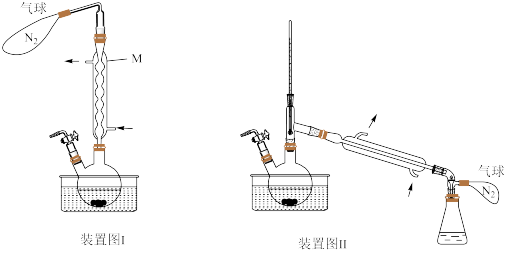
②相关物质的信息如下:
| 化合物 | 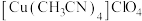 | 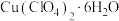 |
| 相对分子质量 | 327.5 | 371 |
| 在乙腈中颜色 | 无色 | 蓝色 |
(1)装置
 中仪器M的名称为
中仪器M的名称为(2)装置
 中反应完全的现象是
中反应完全的现象是(3)装置
 和
和 中N2气球的作用是
中N2气球的作用是(4)
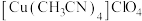 不能由步骤c直接获得,而是先蒸馏至接近饱和,再经步骤d冷却结晶获得。这样处理的目的是
不能由步骤c直接获得,而是先蒸馏至接近饱和,再经步骤d冷却结晶获得。这样处理的目的是(5)为了使母液中的
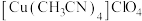 结晶,步骤e中向母液中加入的最佳溶剂是
结晶,步骤e中向母液中加入的最佳溶剂是A.水 B.乙醇 C.乙醚
(6)
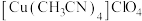 中存在的化学键有
中存在的化学键有A.离子键 B.共价键 C.氢键 D.配位键 E.金属键
(7)合并步骤d和e所得的产物,总质量为
 ,则总收率为
,则总收率为
您最近一年使用:0次
3 . 离子化合物 是一种高活性氮物种,可以作为合成子用于多种高附加值含氮化合物的合成,其晶胞结构如图甲所示,沿z轴方向
是一种高活性氮物种,可以作为合成子用于多种高附加值含氮化合物的合成,其晶胞结构如图甲所示,沿z轴方向 的投影如图乙所示(设
的投影如图乙所示(设 为阿伏加德罗常数的值)。下列叙述正确的是
为阿伏加德罗常数的值)。下列叙述正确的是
 是一种高活性氮物种,可以作为合成子用于多种高附加值含氮化合物的合成,其晶胞结构如图甲所示,沿z轴方向
是一种高活性氮物种,可以作为合成子用于多种高附加值含氮化合物的合成,其晶胞结构如图甲所示,沿z轴方向 的投影如图乙所示(设
的投影如图乙所示(设 为阿伏加德罗常数的值)。下列叙述正确的是
为阿伏加德罗常数的值)。下列叙述正确的是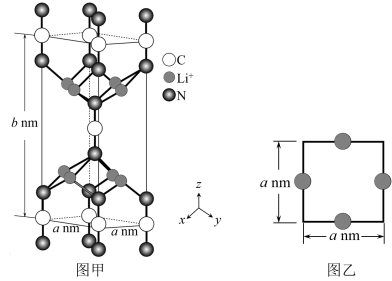
A.电负性: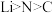 | B. 的电子式为 的电子式为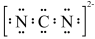 |
C. 的配位数是8 的配位数是8 | D.该晶胞的密度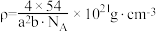 |
您最近一年使用:0次
2024-09-07更新
|
82次组卷
|
3卷引用:专题5 物质结构与性质 元素周期律-晶体结构与性质
解题方法
4 . 利用氢气作为能源的前提是安全有效地解决储存氢气的问题。化学家已研究出多种储存氢气的方法。回答下列问题:
(1)某金属R的储氢材料可以通过化学反应将氢吸附和排放,已知R为短周期金属元素,其部分电离能数据如表所示:
该金属元素R是__________ (填元素符号),其位于元素周期表__________ 区;基态R原子的最高能级电子云轮廓图为__________ 形。
(2) (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
氨硼烷( )中N、B都达到稳定结构,
)中N、B都达到稳定结构, 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是__________ (填元素符号),用化学键表示出( )分子的结构式:
)分子的结构式:__________ 。
(3)有储氢功能的铜银合金晶体具有立方堆积结构,晶胞中Cu原子位于面心,Ag原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的全部四面体空隙中。该晶体储氢后的化学式为__________ 。
(4)过渡金属Q与镧(La)形成的合金是一种储氢材料,其中基态Q原子的价层电子排布式为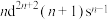 ,该合金的晶胞结构和
,该合金的晶胞结构和 轴方向的投影图如图所示:
轴方向的投影图如图所示:__________ ,该合金的密度为__________  (用含
(用含 、
、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)某金属R的储氢材料可以通过化学反应将氢吸附和排放,已知R为短周期金属元素,其部分电离能数据如表所示:
|
|
|
|
|
578 | 1817 | 2745 | 11577 | 14842 |
(2)
 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。氨硼烷(
 )中N、B都达到稳定结构,
)中N、B都达到稳定结构, 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是 )分子的结构式:
)分子的结构式:(3)有储氢功能的铜银合金晶体具有立方堆积结构,晶胞中Cu原子位于面心,Ag原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的全部四面体空隙中。该晶体储氢后的化学式为
(4)过渡金属Q与镧(La)形成的合金是一种储氢材料,其中基态Q原子的价层电子排布式为
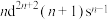 ,该合金的晶胞结构和
,该合金的晶胞结构和 轴方向的投影图如图所示:
轴方向的投影图如图所示: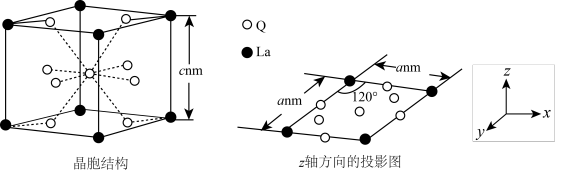
 (用含
(用含 、
、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解题方法
5 . 化合物 是一种新型超分子晶体材料。
是一种新型超分子晶体材料。 可以
可以 为溶剂,由
为溶剂,由 、
、 (18-冠-6)、
(18-冠-6)、 反应制得(已知:超分子的自组装是分子与分子在一定条件下,依赖非共价键分子间作用力自发连接成结构稳定的分子聚集体的过程)。结构如图所示:
反应制得(已知:超分子的自组装是分子与分子在一定条件下,依赖非共价键分子间作用力自发连接成结构稳定的分子聚集体的过程)。结构如图所示:
 是一种新型超分子晶体材料。
是一种新型超分子晶体材料。 可以
可以 为溶剂,由
为溶剂,由 、
、 (18-冠-6)、
(18-冠-6)、 反应制得(已知:超分子的自组装是分子与分子在一定条件下,依赖非共价键分子间作用力自发连接成结构稳定的分子聚集体的过程)。结构如图所示:
反应制得(已知:超分子的自组装是分子与分子在一定条件下,依赖非共价键分子间作用力自发连接成结构稳定的分子聚集体的过程)。结构如图所示: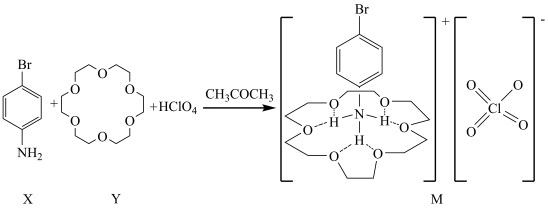
| A.组成M的元素位于元素周期表的s区和p区 |
| B.M中阳离子通过形成氢键体现了超分子的自组装 |
| C.超分子是分子聚集体,不包括离子 |
D. (18-冠-6)具有分子识别功能 (18-冠-6)具有分子识别功能 |
您最近一年使用:0次
名校
6 . EDTA( )是一种重要的络合剂,易与
)是一种重要的络合剂,易与 、
、 、
、 等离子形成稳定的配合物。
等离子形成稳定的配合物。
(1)Mg位于元素周期表中
 的价电子排布式为
的价电子排布式为(2)EDTA中碳原子的杂化方式为
(3)EDTA分子中键角:∠HCH
(4)EDTA中能与
 形成配位键的原子有
形成配位键的原子有(5)
 的立方晶胞结构如图所示。其中a、b原子的分数坐标分别为
的立方晶胞结构如图所示。其中a、b原子的分数坐标分别为 和
和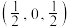 ,晶胞参数为a pm,设
,晶胞参数为a pm,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
②该晶体的密度为
 。
。
您最近一年使用:0次
2024-07-17更新
|
39次组卷
|
2卷引用:山西省晋城市部分高中学校2023-2024学年高二下学期7月期末联考化学试题
解题方法
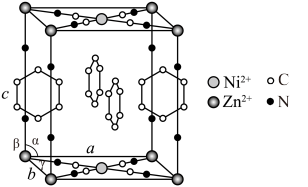
7 . 研究笼形包合物结构和性质具有重要意义。化学式为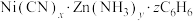 的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数
的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数 ,
, 。
。
(1)①基态 的核外电子排布式为
的核外电子排布式为___________ 。
② 的电子式为
的电子式为___________ 。
③ 的空间结构名称为
的空间结构名称为___________ 。
(2)已知晶胞中N原子均参与形成配位键,则 与
与 的配位数之比为
的配位数之比为___________ ;x:y:z=___________ 。
(3)吡啶(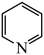 )替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:
)替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:
①___________ ;②___________ 。
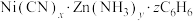 的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数
的笼形包合物四方晶胞结构如下图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数 ,
, 。
。
(1)①基态
 的核外电子排布式为
的核外电子排布式为②
 的电子式为
的电子式为③
 的空间结构名称为
的空间结构名称为(2)已知晶胞中N原子均参与形成配位键,则
 与
与 的配位数之比为
的配位数之比为(3)吡啶(
 )替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:
)替代苯也可形成类似的笼形包合物。吡啶在水中的溶解度远大于苯,主要原因是:①
您最近一年使用:0次
2024-07-13更新
|
58次组卷
|
2卷引用:山西省太原市2023-2024学年高二下学期7月期末考试化学试题
解题方法
8 .  可与丁二酮肟反应生成M,M的结构如图所示。下列有关说法正确的是
可与丁二酮肟反应生成M,M的结构如图所示。下列有关说法正确的是
 可与丁二酮肟反应生成M,M的结构如图所示。下列有关说法正确的是
可与丁二酮肟反应生成M,M的结构如图所示。下列有关说法正确的是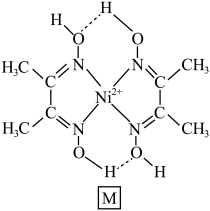
A. 提供孤电子对形成配位键 提供孤电子对形成配位键 |
B. 的配位数为4 的配位数为4 |
| C.M分子中只含有极性键 |
D.丁二酮肟的结构简式为 |
您最近一年使用:0次
名校
解题方法
9 . 下列化学用语或表述正确的是
| A.冰酷酸中的氢键:C—H……O |
B. 中存在的化学键类型:离子键、配位键、共价键 中存在的化学键类型:离子键、配位键、共价键 |
C. 中Cl-Cl键的形成过程: 中Cl-Cl键的形成过程: |
D. 的空间结构名称:平面三角形 的空间结构名称:平面三角形 |
您最近一年使用:0次
10 . 科学家研究发现铁的配合物在常温下可以催化甲酸的还原反应,其反应机理如图所示。下列说法不正确的是
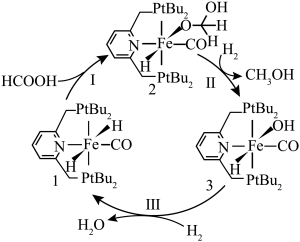
A.该反应的总化学方程式为 |
B.1,2,3三种物质中 的配位数相同 的配位数相同 |
| C.反应中存在非极性键的断裂和形成 |
D.可以用新制的 悬浊液鉴别 悬浊液鉴别 和 和 |
您最近一年使用:0次