1 . 氯亚铂酸钾(K2PtCl4)广泛用作制造各种铂配合物和药物的起始原料,—种以氯亚铂酸钾为原料制备有机物iv的合成路线如图所示,[PtCl4]2-为平面结构,下列说法正确的是
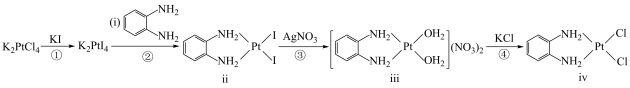
| A.ii的配体为Pt2+ |
| B.iii中Pt2+和O的杂化方式均为sp3 |
C.1mol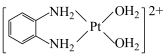 的非金属原子中共含有6mol孤电子对 的非金属原子中共含有6mol孤电子对 |
D.反应3的离子方程式为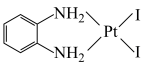 +2H2O+2Ag+→ +2H2O+2Ag+→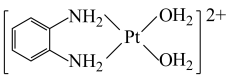 +2AgI↓ +2AgI↓ |
您最近一年使用:0次
2 . 液晶高分子光响应形变材料在柔性机器人等领域有广阔的应用前景。我国科学家合成了一种光响应高分子M,其合成路线如图。下列说法正确的是
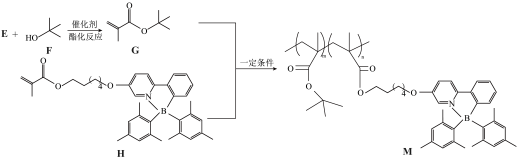
| A.G存在反式异构体 | B.F能被酸性 溶液氧化 溶液氧化 |
| C.G和H生成M的反应类型为加聚反应 | D.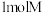 中配位键的数目为 中配位键的数目为 |
您最近一年使用:0次
名校
解题方法
3 . 一种含Se的新型AIE分子(IV)的合成路线如图:_______ 。
(2)IV中具有孤电子对的原子有_______ 。
| A.I中仅有σ键 |
| B.I中的Se-Se为非极性共价键 |
| C.II易溶于水 |
| D.II中原子的杂化轨道类型只有sp、sp2、sp3 |
| A.C | B.O | C.S | D.Se |
您最近一年使用:0次
解题方法
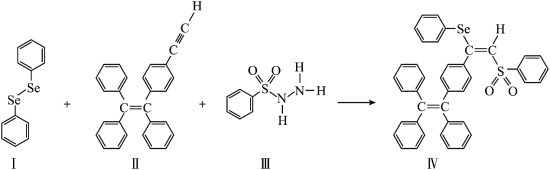
4 . 氧杂环丁基叠氮聚合物是一种新型的高分子材料,具有较好的光学、电学和磁学性质,其合成路线如下。
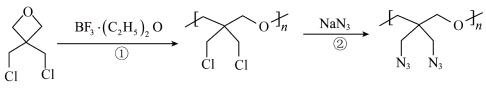
下列说法错误的是

下列说法错误的是
A. 中含有配位键 中含有配位键 |
| B.反应①中碳原子的杂化方式发生了改变 |
| C.可用红外光谱仪检测叠氮聚合物的生成 |
D.生成1mol叠氮聚合物理论上需要消耗 |
您最近一年使用:0次
5 . 镁、铝及其合金是中学常见金属材料,被广泛应用于生产生活中。回答下列问题:
(1)B、Al、Ga、In、Tl为同一主族从上至下的相邻元素,则Tl元素的价层电子排布式为___________ 。
(2)金属铝的冶炼过程中常需要冰晶石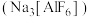 作助熔剂,已知冰晶石可通过下列原理制备:
作助熔剂,已知冰晶石可通过下列原理制备:
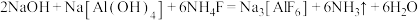 。
。
①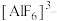 中Al的杂化类型为
中Al的杂化类型为___________ (填选项字母)。
A. B.
B. C.
C. D.
D.
②冰晶石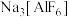 的熔点为1000℃左右,高于NaOH的熔点(318℃)的原因为
的熔点为1000℃左右,高于NaOH的熔点(318℃)的原因为___________ 。
(3)铝硫电池常用熔融氯铝酸盐(由NaCl、KCl和 形成熔点为93℃的共熔物)作电解质,在放电和充电过程中氯铝酸根起到结合或释放
形成熔点为93℃的共熔物)作电解质,在放电和充电过程中氯铝酸根起到结合或释放 的作用。图甲为初始状态共熔物中铝元素的存在形式,放电时
的作用。图甲为初始状态共熔物中铝元素的存在形式,放电时 会进入到电解质中并结合游离的
会进入到电解质中并结合游离的 和
和 形成有限长单链聚合体(如图乙),则该单链聚合体的化学式为
形成有限长单链聚合体(如图乙),则该单链聚合体的化学式为___________ (Al的数目用n表示)。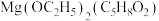 是用于制备纳米级MgO粉体的重要原料,可通过乙醇、乙酰丙酮(
是用于制备纳米级MgO粉体的重要原料,可通过乙醇、乙酰丙酮( )与Mg在一定条件下反应合成,其结构简式如图丙所示。
)与Mg在一定条件下反应合成,其结构简式如图丙所示。___________ ,氧原子提供孤对电子与镁形成___________ 键。
②乙醇镁配合物中,各元素电负性由大到小的顺序为___________ 。
③乙醇的沸点高于乙酰丙酮的原因为___________ 。
(5)已知 晶体存在两种晶胞结构,如图丁所示。该晶胞参数
晶体存在两种晶胞结构,如图丁所示。该晶胞参数 ,阿伏加德罗常数的值以
,阿伏加德罗常数的值以 表示。
表示。 的配位数之比为a:b=
的配位数之比为a:b=___________ 。
②晶胞b中两个最近的 间的距离为x nm,该晶体的密度为
间的距离为x nm,该晶体的密度为___________  。
。
(1)B、Al、Ga、In、Tl为同一主族从上至下的相邻元素,则Tl元素的价层电子排布式为
(2)金属铝的冶炼过程中常需要冰晶石
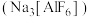 作助熔剂,已知冰晶石可通过下列原理制备:
作助熔剂,已知冰晶石可通过下列原理制备: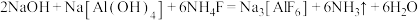 。
。①
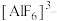 中Al的杂化类型为
中Al的杂化类型为A.
 B.
B. C.
C. D.
D.
②冰晶石
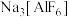 的熔点为1000℃左右,高于NaOH的熔点(318℃)的原因为
的熔点为1000℃左右,高于NaOH的熔点(318℃)的原因为(3)铝硫电池常用熔融氯铝酸盐(由NaCl、KCl和
 形成熔点为93℃的共熔物)作电解质,在放电和充电过程中氯铝酸根起到结合或释放
形成熔点为93℃的共熔物)作电解质,在放电和充电过程中氯铝酸根起到结合或释放 的作用。图甲为初始状态共熔物中铝元素的存在形式,放电时
的作用。图甲为初始状态共熔物中铝元素的存在形式,放电时 会进入到电解质中并结合游离的
会进入到电解质中并结合游离的 和
和 形成有限长单链聚合体(如图乙),则该单链聚合体的化学式为
形成有限长单链聚合体(如图乙),则该单链聚合体的化学式为
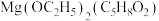 是用于制备纳米级MgO粉体的重要原料,可通过乙醇、乙酰丙酮(
是用于制备纳米级MgO粉体的重要原料,可通过乙醇、乙酰丙酮( )与Mg在一定条件下反应合成,其结构简式如图丙所示。
)与Mg在一定条件下反应合成,其结构简式如图丙所示。
②乙醇镁配合物中,各元素电负性由大到小的顺序为
③乙醇的沸点高于乙酰丙酮的原因为
(5)已知
 晶体存在两种晶胞结构,如图丁所示。该晶胞参数
晶体存在两种晶胞结构,如图丁所示。该晶胞参数 ,阿伏加德罗常数的值以
,阿伏加德罗常数的值以 表示。
表示。
 的配位数之比为a:b=
的配位数之比为a:b=②晶胞b中两个最近的
 间的距离为x nm,该晶体的密度为
间的距离为x nm,该晶体的密度为 。
。
您最近一年使用:0次
名校
6 .  (三氯化六氨合钴)是合成其他含钴配合物的重要原料,实验中可由金属钴及其他原料制备
(三氯化六氨合钴)是合成其他含钴配合物的重要原料,实验中可由金属钴及其他原料制备 。
。
已知:① 在
在 时恰好完全沉淀为
时恰好完全沉淀为 ;
;
②不同温度下 在水中的溶解度如图所示。
在水中的溶解度如图所示。

(一) 的制备
的制备
 易潮解,
易潮解,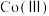 的氧化性强于
的氧化性强于 ,可用金属钻与氯气反应制备
,可用金属钻与氯气反应制备 。实验中利用如图装置(连接用橡胶管省略)进行制备。
。实验中利用如图装置(连接用橡胶管省略)进行制备。
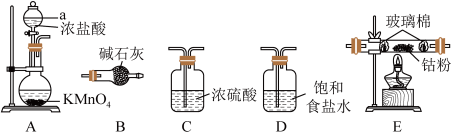
(1)用图中的装置组合制备 ,仪器a的名称为
,仪器a的名称为______ ,仪器连接顺序为______ (填标号)。装置B的作用是______ 。
(2)装置A中发生反应的离子方程式为______ 。
(二) 的制备步骤如下:
的制备步骤如下:
Ⅰ.在100mL锥形瓶内加入4.5g研细的 ,3g
,3g 和5mL水,加热溶解后加入0.3g活性炭作催化剂。
和5mL水,加热溶解后加入0.3g活性炭作催化剂。
Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下,并缓慢加入10mL 溶液。
溶液。
Ⅲ.在60℃下反应一段时间后,经过______、冷却结晶、过滤、洗涤、干燥等操作,得到 晶体。
晶体。
根据以上步骤,回答下列问题:
(3)在步骤Ⅱ加入浓氨水前,需在步骤Ⅰ中加入 ,请从平衡移动的角度解释加入
,请从平衡移动的角度解释加入 的目的
的目的______ 。
(4)步骤Ⅱ中在加入 溶液时,控制温度在10℃以下并缓慢加入的目的是
溶液时,控制温度在10℃以下并缓慢加入的目的是______ 。
(5)步骤Ⅲ中的操作名称为______ 。
(6) 的配位数为
的配位数为______ 。1L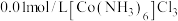 溶液和足量硝酸银反应,生成AgCl的物质的量为
溶液和足量硝酸银反应,生成AgCl的物质的量为______ mol。
 (三氯化六氨合钴)是合成其他含钴配合物的重要原料,实验中可由金属钴及其他原料制备
(三氯化六氨合钴)是合成其他含钴配合物的重要原料,实验中可由金属钴及其他原料制备 。
。已知:①
 在
在 时恰好完全沉淀为
时恰好完全沉淀为 ;
;②不同温度下
 在水中的溶解度如图所示。
在水中的溶解度如图所示。
(一)
 的制备
的制备 易潮解,
易潮解,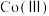 的氧化性强于
的氧化性强于 ,可用金属钻与氯气反应制备
,可用金属钻与氯气反应制备 。实验中利用如图装置(连接用橡胶管省略)进行制备。
。实验中利用如图装置(连接用橡胶管省略)进行制备。
(1)用图中的装置组合制备
 ,仪器a的名称为
,仪器a的名称为(2)装置A中发生反应的离子方程式为
(二)
 的制备步骤如下:
的制备步骤如下:Ⅰ.在100mL锥形瓶内加入4.5g研细的
 ,3g
,3g 和5mL水,加热溶解后加入0.3g活性炭作催化剂。
和5mL水,加热溶解后加入0.3g活性炭作催化剂。Ⅱ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下,并缓慢加入10mL
 溶液。
溶液。Ⅲ.在60℃下反应一段时间后,经过______、冷却结晶、过滤、洗涤、干燥等操作,得到
 晶体。
晶体。根据以上步骤,回答下列问题:
(3)在步骤Ⅱ加入浓氨水前,需在步骤Ⅰ中加入
 ,请从平衡移动的角度解释加入
,请从平衡移动的角度解释加入 的目的
的目的(4)步骤Ⅱ中在加入
 溶液时,控制温度在10℃以下并缓慢加入的目的是
溶液时,控制温度在10℃以下并缓慢加入的目的是(5)步骤Ⅲ中的操作名称为
(6)
 的配位数为
的配位数为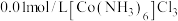 溶液和足量硝酸银反应,生成AgCl的物质的量为
溶液和足量硝酸银反应,生成AgCl的物质的量为
您最近一年使用:0次
7 . 中南大学刘又年、黄健涵、李嘉伟团队提出发展炔烃、醛、胺等工业大宗原料和炉烟二氧化碳的四组分串联反应,来实现恶唑烷酮及其衍生物的高效合成,反应历程如图所示,已知:Ph为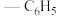 ,Bn为
,Bn为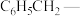 ,Path a为途径a。下列叙述正确的是
,Path a为途径a。下列叙述正确的是
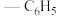 ,Bn为
,Bn为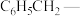 ,Path a为途径a。下列叙述正确的是
,Path a为途径a。下列叙述正确的是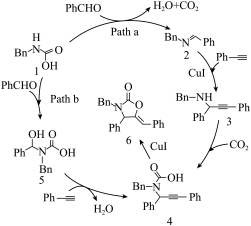
A.总反应的原子利用率为 | B.Path a中 是副产物 是副产物 |
C.Path b断裂了 键和 键和 键 键 | D.产物6的分子中含2个手性碳原子 |
您最近一年使用:0次
名校
解题方法
8 . 氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示,下列叙述正确的是


| A.NH3与BF3都是由极性键构成的极性分子 |
| B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,立方氮化硼晶胞中含有8个氮原子、8个硼原子 |
| C.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1molNH4BF4含有配位键的数目为2NA |
| D.立方氮化硼和半导体材料氮化铝的结构均类似于金刚石,立方氮化硼的熔点小于氮化铝 |
您最近一年使用:0次
2024-03-21更新
|
239次组卷
|
2卷引用:河北省石家庄市第二十四中学2023-2024高二上学期期末考试化学试题
名校
解题方法
9 . 一种比率光声探针M与 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:_______ ,基态 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为_______ 。
(2)均为平面结构的吡咯( )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为_______ ,原因是_______ 。
(3) 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角_______  中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。
(4) (
( )中
)中 比
比 中的更
中的更_______ (填“难”或“易”)断裂。其原因是_______ 。
元素周期表中,第四周期元素单质及其化合物在化工生产和研究中有重要的应用。
(5)在浓 的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为
的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为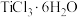 的晶体,该晶体中两种配体的物质的量之比为
的晶体,该晶体中两种配体的物质的量之比为 ,则由该配合离子组成的晶体化学式还可以写为
,则由该配合离子组成的晶体化学式还可以写为_______ 。
(6)硒氧化铋是一类全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的 层与带负电的
层与带负电的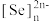 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为_______ 。晶胞棱边夹角均为 ,则晶体密度的计算式为
,则晶体密度的计算式为_______  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
 的价电子中,两种自旋状态的电子数之比为
的价电子中,两种自旋状态的电子数之比为(2)均为平面结构的吡咯(
 )和吡啶(
)和吡啶( )是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为
)是合成该探针的原料,吡咯和吡啶在盐酸中溶解度较小的为(3)
 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角 中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。(4)
 (
( )中
)中 比
比 中的更
中的更元素周期表中,第四周期元素单质及其化合物在化工生产和研究中有重要的应用。
(5)在浓
 的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为
的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为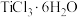 的晶体,该晶体中两种配体的物质的量之比为
的晶体,该晶体中两种配体的物质的量之比为 ,则由该配合离子组成的晶体化学式还可以写为
,则由该配合离子组成的晶体化学式还可以写为(6)硒氧化铋是一类全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的
 层与带负电的
层与带负电的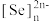 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为 ,则晶体密度的计算式为
,则晶体密度的计算式为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
10 . 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图一所示。下列叙述错误的是
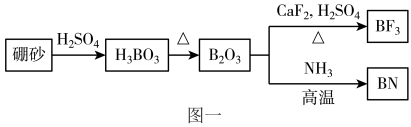


A.H3BO3在水溶液中发生反应: ,可知H3BO3是一元弱酸 ,可知H3BO3是一元弱酸 |
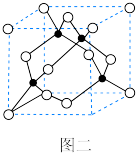
| B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其晶胞结构如图二,立方氮化硼晶胞中含有4个氮原子、4个硼原子 |
| C.由B2O3可制备晶体硼,晶体硼的熔点2573K,沸点2823K,硬度大,属于共价晶体 |
| D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH4BF4含有配位键的数目为NA |
您最近一年使用:0次



