解题方法
1 . ClO2可用作消毒剂。ClO2的水溶液在较高温度与光照下会生成 、
、 。下列关于ClO2、
。下列关于ClO2、 和
和 的说法正确的是
的说法正确的是
 、
、 。下列关于ClO2、
。下列关于ClO2、 和
和 的说法正确的是
的说法正确的是| A.ClO2为非极性分子 | B. 中Cl原子的杂化类型为sp3杂化 中Cl原子的杂化类型为sp3杂化 |
C. 的VSEPR模型为三角锥形 的VSEPR模型为三角锥形 | D. 与 与 的键角相等 的键角相等 |
您最近一年使用:0次
23-24高二下·全国·课后作业
名校
2 . 下列对分子性质的解释中,正确的是
| A.NH3极易溶于水而CH4难溶于水只是因为NH3是极性分子,CH4是非极性分子 |
B.乳酸(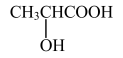 )具有光学活性,因为其分子中含有一个手性碳原子 )具有光学活性,因为其分子中含有一个手性碳原子 |
| C.水很稳定(1000℃以上才会部分分解)是因为水分子间存在大量的氢键 |
| D.PH3分子与NH3分子的构型关系完全相同 |
您最近一年使用:0次
2024-03-05更新
|
619次组卷
|
4卷引用:新疆阿克苏市实验中学2022-2023学年高二下学期第二次月考化学试题
名校
解题方法
3 . 某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的五种短周期非金属元素,Z的原子序数等于X、Y原子序数之和,Q为非金属性最强的元素。

A. 的键角大于 的键角大于 的键角 的键角 | B.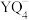 的VSEPR模型为正四面体形 的VSEPR模型为正四面体形 |
C.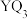 是极性分子, 是极性分子, 是非极性分子 是非极性分子 | D.M2的键能小于Q2的键能 |
您最近一年使用:0次
2024-02-08更新
|
148次组卷
|
2卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高二下学期3月月考化学试题
4 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
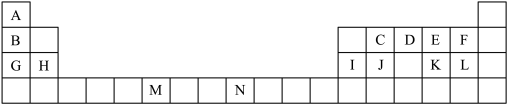
试回答下列问题:
(1)表中元素,电负性最强的是_______ (填元素符号),J的元素名称为_______ 。N基态原子核外能级上有_______ 未成对电子。
(2)D元素原子的价电子排布图为_______ ,核外有_______ 种不同运动状态的电子。该元素形成的常见单质分子中σ键和π键个数比为_______
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是_______ (填“极性”或“非极性”)分子。
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是_______ (填字母)。
a. b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH

试回答下列问题:
(1)表中元素,电负性最强的是
(2)D元素原子的价电子排布图为
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
a.
 b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
您最近一年使用:0次
5 . 回答下列问题:
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2,光气(COCl2)分子的立体构型是_______ 形。
(2)某有机物的结构简式为 。该有机物分子是
。该有机物分子是_______ (填“极性”或“非极性”)分子,该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为_______ 。
(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为_______ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因_______
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3.HN3的酸性和醋酸相近,可微弱电离出H+和N 。
。
①叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,根据价层电子对互斥理论判断SO 的空间构型为
的空间构型为_______ 。
②下列有关说法正确的是_______ (填序号)。
A.HN3中含有5个σ键
B.HN3中的三个氮原子均采用sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.肼(N2H4)的沸点高达113.5℃,说明肼分子间可形成氢键
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2,光气(COCl2)分子的立体构型是
(2)某有机物的结构简式为
 。该有机物分子是
。该有机物分子是(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3.HN3的酸性和醋酸相近,可微弱电离出H+和N
 。
。①叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,根据价层电子对互斥理论判断SO
 的空间构型为
的空间构型为②下列有关说法正确的是
A.HN3中含有5个σ键
B.HN3中的三个氮原子均采用sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.肼(N2H4)的沸点高达113.5℃,说明肼分子间可形成氢键
您最近一年使用:0次
6 . 下列说法正确的是
A.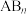 型分子中,若中心原子没有孤对电子,则 型分子中,若中心原子没有孤对电子,则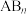 为空间对称结构,属于非极性分子 为空间对称结构,属于非极性分子 |
B.水分子中含有 键 键 |
C. 、 、 、 、 分子中的O、N、C分别形成2个、3个、4个键,故O、N、C分别采取sp、 分子中的O、N、C分别形成2个、3个、4个键,故O、N、C分别采取sp、 、 、 杂化 杂化 |
| D.卤素的氢化物中,HF的沸点最低 |
您最近一年使用:0次
7 . 生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、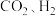 等)与
等)与 混合,催化合成甲醇是生物质能利用的方法之一。
混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态锌原子的核外电子排布式:_______ 。该元素位于元素周期表_______ 区。
(2)甲醇催化氧化可得到甲醛,甲醛与新制 的碱性溶液反应生成
的碱性溶液反应生成 沉淀。
沉淀。
①甲醇的沸点比甲醛的高,其主要原因是_______ ;甲醛分子中碳原子轨道的杂化类型为_______ 。
②甲醛_______ 分子(极性或非极性);1mol甲醛分子中σ键的数目为_______ 。
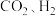 等)与
等)与 混合,催化合成甲醇是生物质能利用的方法之一。
混合,催化合成甲醇是生物质能利用的方法之一。(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态锌原子的核外电子排布式:
(2)甲醇催化氧化可得到甲醛,甲醛与新制
 的碱性溶液反应生成
的碱性溶液反应生成 沉淀。
沉淀。①甲醇的沸点比甲醛的高,其主要原因是
②甲醛
您最近一年使用:0次
8 . 某化合物的分子式为AB2,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为3.44和3.98,已知AB2分子的键角为1.3.3°。下列推断不正确的是
| A.AB2分子的立体构型为V形 |
| B.A-B键为极性共价键,AB2分子为非极性分子 |
| C.AB2与H2O相比,AB2的熔点、沸点比H2O的低 |
| D.AB2分子中无氢原子,分子间不能形成氢键,而H2O分子间能形成氢键 |
您最近一年使用:0次
2024-03-05更新
|
58次组卷
|
2卷引用:新疆阿克苏市实验中学2022-2023学年高二下学期第二次月考化学试题
名校
解题方法
9 . 下列叙述中正确的是
| A.以非极性键结合起来的分子一定是非极性分子 |
| B.键角:NH3>PH3 |
| C.NCl3与BF3均为三角锥形结构,均为极性分子 |
| D.非极性分子中一定含有非极性键 |
您最近一年使用:0次
2023-08-25更新
|
95次组卷
|
2卷引用:新疆石河子第一中学2023-2024学年高三上学期第二次月考化学试题
名校
解题方法
10 . 已知CO2、BF3、CH4、SO3都是非极性分子,NH3、H2S、H2O、SO2都是极性分子,由此可推知ABn型分子是非极性分子的经验规律是
| A.分子中不能含有氢原子 |
| B.在ABn分子中A原子没有孤电子对(或A原子最外层电子均已成键) |
| C.在ABn分子中每个共价键的键长和键能都相等 |
| D.分子中所有原子在同一平面内 |
您最近一年使用:0次
2023-08-21更新
|
82次组卷
|
2卷引用:新疆石河子第一中学2023-2024学年高三上学期第二次月考化学试题



