名校
1 . 下列变化规律正确的是
A.键能: | B.极性: |
C.键长: | D.键角: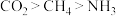 |
您最近一年使用:0次
2023-12-26更新
|
180次组卷
|
4卷引用:青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题
名校
2 . 已知H与O可以形成 H2O和H2O2两种化合物。请完成下列空白:
(1)H2O内的O−H、水分子间的范德华力和氢键,从强到弱依次为___________ 。
(2)H+可与 H2O 形成H3O+,H3O+中O采用___________ 杂化。H3O+中H−O−H键角比H2O中的___________ ,原因为___________ 。
(3)H2O2是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。H2O2的电子式是___________ ,结构式是___________ 。H2O2是含有___________ 键和___________ 键的___________ 分子(填"极性"或"非极性")。H2O2能与水混溶,却不溶于CCl4。请予以解释:___________ 。

(1)H2O内的O−H、水分子间的范德华力和氢键,从强到弱依次为
(2)H+可与 H2O 形成H3O+,H3O+中O采用
(3)H2O2是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。H2O2的电子式是

您最近一年使用:0次
2023-03-31更新
|
216次组卷
|
2卷引用:青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题
3 . 下列各组物质的分类正确的是
①混合物:氯水、氨水、水银、福尔马林、聚乙烯;
②电解质:明矾、冰醋酸、纯碱;
③非极性分子:CO2、CCl4、CH2Cl2;
④同位素:1H+、2H2、3H;
⑤同素异形体:C60、C80、金刚石、石墨;
⑥有机化合物:乙醇、乙烯、碳酸、苯;
⑦醇类: 、CH3COOH、HCHO、
、CH3COOH、HCHO、
①混合物:氯水、氨水、水银、福尔马林、聚乙烯;
②电解质:明矾、冰醋酸、纯碱;
③非极性分子:CO2、CCl4、CH2Cl2;
④同位素:1H+、2H2、3H;
⑤同素异形体:C60、C80、金刚石、石墨;
⑥有机化合物:乙醇、乙烯、碳酸、苯;
⑦醇类:
 、CH3COOH、HCHO、
、CH3COOH、HCHO、
| A.②⑤ | B.①④⑤⑦ | C.②③⑥⑦ | D.全部正确 |
您最近一年使用:0次
4 . 观察下列模型并结合有关信息,判断有关说法不正确的是
| B12结构单元 | SF6分子 | S8分子 | HCN | |
| 结构示意图 |  |  |  |  |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
| A.单质B结构单元中含有30个B﹣B键,含20个正三角形 |
| B.HCN为直线形 |
| C.SF6是由极性键构成的非极性分子 |
| D.固态硫S8中S原子为sp2杂化 |
您最近一年使用:0次
2021-03-18更新
|
354次组卷
|
5卷引用:青海省湟川中学2019-2020学年高二下学期期中考试化学试题
名校
解题方法
5 . 下列说法中正确的是
①在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
②同一周期从左到右,元素的第一电离能、电负性都是越来越大
③PCl3和光气(COCl2)分子中所有原子的最外层都达到8电子稳定结构
④所有的配合物都存在配位键,所有含配位键的化合物都是配合物
⑤所有含极性键的分子都是极性分子
⑥熔融状态下能导电的化合物一定是离子化合物
⑦所有的原子晶体都不导电
①在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
②同一周期从左到右,元素的第一电离能、电负性都是越来越大
③PCl3和光气(COCl2)分子中所有原子的最外层都达到8电子稳定结构
④所有的配合物都存在配位键,所有含配位键的化合物都是配合物
⑤所有含极性键的分子都是极性分子
⑥熔融状态下能导电的化合物一定是离子化合物
⑦所有的原子晶体都不导电
| A.①② | B.④⑥ | C.③⑥ | D.③⑦ |
您最近一年使用:0次
2021-03-18更新
|
365次组卷
|
2卷引用:青海省湟川中学2019-2020学年高二下学期期中考试化学试题
名校
解题方法
6 . 叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定方面越来越引起人们的重视,其中氢叠氮酸(HN3)是一种弱酸,可表示为 ,下列有关说法正确的是
,下列有关说法正确的是
 ,下列有关说法正确的是
,下列有关说法正确的是| A.HN3中含有5个σ键 |
| B.HN3中三个氮原子采用的都是sp2杂化 |
| C.HN3不能与Cu2+形成配合物 |
| D.HN3、HNO2、H2O、N2H4都是极性分子 |
您最近一年使用:0次



